Atrésie de l'œsophage
| Spécialité | Génétique médicale |
|---|
| CIM-10 | Q39.0, Q39.1 |
|---|---|
| CIM-9 | 750.3 |
| DiseasesDB | 30035 |
| MedlinePlus | 000961 |
| eMedicine |
414368 radio/704 |
| MeSH | D004933 |
L'atrésie de l'œsophage est une malformation congénitale (c'est-à-dire présente dès la naissance) qui consiste en l'interruption de l'œsophage[1].

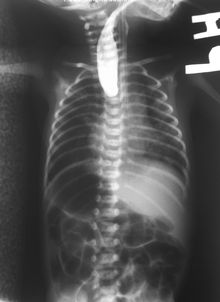

L'œsophage présente donc deux culs-de-sac[2] :
- cul-de-sac supérieur pour la partie de l'œsophage qui est reliée à la bouche ;
- cul-de-sac inférieur pour la partie de l'œsophage qui est reliée à l'estomac.
Ni les aliments ni la salive ou le mucus nasal ne peuvent être conduits vers l’estomac. Cette malformation est en outre fréquemment associée à une connexion anormale (fistule) œsophage-trachée. Le lait maternel (ou non) absorbé par le nouveau-né au lieu de rejoindre l'estomac passe alors de la trachée dans les poumons (phénomène dit de « fausse route »). Le bébé s'étouffe et/ou « recrache » le lait et sa salive. L'introduction d'aliments et de salive dans les poumons peut être source d'infection respiratoire grave (pneumonie...)[3]
C'est une urgence chirurgicale[4] qui implique le transfert du bébé vers un service de chirurgie néonatale et de soins intensifs où, si le bébé n'est pas né prématuré[5] et s'il est indemne d'infections le rendant vulnérable à une opération (ex : pneumonie), il sera généralement nourri par perfusion puis opéré dans les jours suivants. Si l'opération doit attendre, le bébé est nourri par gastrostomie.
-Une nouvelle méthode peu invasive, diminuant significativement les risques et la mortalité, se fait avec le système d'anastomose magnétique pour atrésie œsophagienne pédiatrique Flourish (Cook Medical)
Prévalence et épidémiologie
[modifier | modifier le code]C'est une anomalie rare qui touche un enfant sur 2500 à 3500 (avec ou sans fistule)[6]. Le risque est le même pour les deux sexes, dans toutes les populations[3]. Elle est 2 à 3 fois plus fréquente chez les vrais jumeaux[3].
Selon Maynard & Bouin (2011) au Québec où environ 3 % des nouveau-nés sont porteurs d'une anomalie congénitale l'atrésie de l'œsophage est rare mais est l'anomalie congénitale de l'œsophage la plus fréquente[7]
Des pics d'incidence géographique ou temporelle ont été repérés mais qui sont encore mal compris[8],[9]
Causes
[modifier | modifier le code]L'étiologie de la maladie n'est pas identifiée avec certitude.
Il ne semble pas s'agir d'une maladie génétique car les cas sont presque toujours sporadiques dans la famille, avec un très faible risque de récurrence dans la famille (1 % environ[3]). Si d'autres anomalies sont associées à une atrésie, une consultation de génétique est néanmoins recommandée[3].
On sait que la malformation survient en début de grossesse[3], au moment de l'embryogenèse où l'œsophage se construit, ce qui laisse suspecter une cause environnementale (ex : exposition de la mère à un produit tératogène à ce moment). Une étude cas-témoins[10] récemment faite en Caroline du Nord (publication 2016) a conclu à une association significative entre le fait de résider pour la mère près d'une zone agricole utilisant des pesticides et certaines malformations, « en particulier, les atrésies de l'œsophage »[11]. Le Fluconazole[12] et le glyphosate (ou le roundup, c'est-à-dire le glyphosate associé à ses additifs) et d'autres produits pesticides font partie des produits suspectés de pouvoir induire cette malformation[13].
Complications
[modifier | modifier le code]Après un traitement chirurgical (qui peut nécessiter plusieurs opérations) les enfants touchés présentent dans environ la moitié des cas un reflux gastro-œsophagien (RGO), c'est-à-dire des remontées acides dans l’œsophage à partir de l’estomac qui entraînent, après les repas, des brûlures (avec ou sans régurgitations acides), phénomène assez courant chez les bébés, mais qui ici peut persister plus longtemps que dans la moyenne de la population[3],[14].
Diagnostic
[modifier | modifier le code]Diagnostic anténatal (DAN)
[modifier | modifier le code]Il permet de prévenir et préparer les parents[15] et de dresser avant la naissance « un bilan complémentaire à la recherche de formes associées de plus mauvais pronostic (échographie de référence, IRM et amniocentèse) et d’organiser la naissance dans un centre disposant de l’aval pédiatrique médicochirurgical adapté ». Les deux signes qui alerteront le médecin sont :
- l'hydramnios (ou polyhydramnios) : liquide amniotique présent en quantité excessive lors de la grossesse car le fœtus ne peut pas déglutir) ; il peut aussi avoir d'autres causes[3].
- une échographie qui (dès le second trimestre montrant parfois estomac anormalement petit ou un œsophage dilaté ou mal formé, mais dans la moitié des cas, l'anomalie n'est pas visible [3].
Diagnostic est post-natal
[modifier | modifier le code]Juste après l'accouchement, deux types de tests peuvent être faits :
- une sonde « naso-gastrique » très fine peut être introduite dans l'œsophage du nouveau-né. Si elle est bloquée après quelques cm, c'est qu'il y a atrésie[3].
- test à la seringue
- l'IRM permet un diagnostic précis, mais est rarement utilisé chez les nouveau-nés[16]
Dans presque tous les cas une anomalie de la trachée est associée, et dans la moitié des cas environ[3], l'atrésie de l'œsophage est associée à d'autres malformations, comme dans le cadre du syndrome de VATER (présent dans 10 % des cas[3]) ou de VACTERL. Il convient donc de rapidement rechercher activement d'autres malformations associées qui peuvent toucher le cœur (dans 30 % des cas), mais aussi le squelette (25 % des cas), les reins, les membres, le système digestif (25 % des cas) ou urinaire[3].... Une échographie et une radiographie de l'abdomen confirme le type d'atrésie et des examens complémentaires portent notamment sur le cœur (échocardiographie) et l'anus (une sonde recherche une éventuelle perforation)[3].
Diagnostic tardif
[modifier | modifier le code]Dans les heures qui suivent la naissance, les parents ou l'équipe médical peuvent être alertés par trois symptômes :
- hypersialorrhée ;
- cyanose et dyspnée lors de la première tétée ;
- pneumopathies.
Classification de Ladd
[modifier | modifier le code]les différents types d'atrésie
- Type I
- Sans fistule. 7 à 10 %
- Aucun des culs de sac œsophagien n'est relié à la trachée. Les deux culs de sac sont souvent très éloignés l'un de l'autre.
- Type II
- Avec fistule. 1 %
- Fistule entre la trachée et le cul de sac supérieur de l'œsophage.
- Type III
- Avec fistule. 80 %
- Fistule entre la trachée et le cul de sac inférieur de l'œsophage. Les 2 culs de sac sont assez proches l'un de l'autre.
- Type IV
- Avec fistule : 4 %
- Fistule entre la carène de la trachée (ou la bronche droite) et le cul de sac inférieur de l'œsophage.
- Type V
- Avec fistule : 3 %
- Plusieurs fistules entre la trachée et le cul de sac supérieur de l'œsophage. Les 2 culs de sac sont le plus souvent très proches l'un de l'autre.
Prise en charge
[modifier | modifier le code]À la maternité
[modifier | modifier le code]- à jeun
- proclive (sauf type I : déclive)
- pose d'une perfusion : sérum glucosé (G10) et correction des troubles hydroélectrolytiques
- pose d'une sonde au niveau du cul de sac supérieur de l'œsophage
- intubation naso-trachéale si encombrement bronchique
Intervention chirurgicale
[modifier | modifier le code]Trois situations possibles :
- Les 2 culs de sac œsophagiens sont assez proches : les 2 extrémités sont rapprochables et la continuité de l'œsophage est facilement rétablie sans tension.
- Les 2 culs de sac œsophagiens sont rapprochables mais sous tension, car pas assez proches l'un de l'autre. Risque de suites opératoires plus difficiles.
- Les 2 culs de sac œsophagiens sont trop éloignés l'un de l'autre. Il faut attendre 9 mois à 1 an pour rétablir la continuité en utilisant une autre partie du tube digestif [17] :
- plastie colique si un morceau du côlon (gros intestin) est utilisé ;
- plastie gastrique si c'est un morceau de l'estomac qui est utilisé[3] ;
chacune de ces deux méthodes ayant ses avantages et inconvénients, qui sont pesés par le chirurgien en fonction du type de malformation[3].
Quand la continuité oesophagienne est reconstituée, un reflux gastro-oesophagique acide survient fréquemment ; certains médicaments peuvent atténuer ses effets, ils sont efficaces dans environ 50 % des cas[3].
Suites
[modifier | modifier le code]Le bébé peut être nourri normalement 7 jours après l’opération, en petites quantités successives pour limiter les problèmes de reflux, ou la convalescence est allongée chez les prématurés ou à la suite d'une ou des opération(s) complexe(s). Généralement les enfants opérés ont des difficultés à les aliments ou certains aliments car l'œsophage reconstitué est moins contractile et ne pousse pas les aliments correctement vers l'estomac, gênant la déglutition[3]. Plus bas une sténose (rétrécissement) peut apparaitre plus ou moins tardivement (quelques mois ou années après l'opération, parfois causée ou exacerbée par les reflux acides[3]) et persister au niveau de la suture, qui gêne également la descente d'aliments durs. Très rarement, une fistule se reforme mettant à nouveau l’œsophage en communication avec la trachée, nécessitant une nouvelle opération[3]. Troubles du comportements alimentaires[18], ainsi que toux, bronchites et asthme sont plus fréquent chez l'enfant puis s'atténuent avec l'âge[3].
La sévérité de la maladie et son retentissement sur la vie du patient sera surtout liée aux éventuelles anomalies associées, particulièrement en cas d'anomalie cardiaque grave[3].
L'enfant sera suivi en consultations spécialisées (gastro-entérologie pédiatrique / chirurgie pédiatrique)[3]
Pronostic
[modifier | modifier le code]- poids de naissance > 1 500 g : 100 % de survie en l'absence d'autre malformation[3].
- poids de naissance < 1 500 g ou association à une autre malformation (notamment cardiaque) : 65 % de survie.
Recherche médicale
[modifier | modifier le code]Elle vise actuellement
- à comprendre l'épidémiologie (via notamment les registres de malformations congéniatles dans les territoires où ils existent[19]) ou les cause(s) de cette maladie. Des souris génétiquement porteuses d'une anomalie semblable sont étudiées pour comprendre le rôle éventuel ou supputé de certains gènes (gène Sonic hedgehog notamment)[3] ;
- à explorer de nouveaux moyens plus efficaces de dilatation[20] des sténoses[3].
- a améliorer la chirurgie reconstructrice de l'œsophage, via l'ingénierie tissulaire notamment[21],[22].
Notes et références
[modifier | modifier le code]- Leflot, L., Pietrera, P., Brun, M., & Chateil, J. F. (2005). Pathologie de l'œsophage chez l'enfant. EMC-Radiologie, 2(5), 494-526.
- schéma
- Encyclopédie Orphanet Grand Public (2008) "L’atrésie de l’œsophage" | Maladies Rares Info Services 01 56 53 81 36 |rédigé avec la participation du Professeur Frédéric Gottrand |URL:www.orpha.net/data/patho/Pub/fr/AtresieOesophage-FRfrPub724v01.pdf | Juin 2008
- Fievet, L., Faure, A., Panait, N., Coze, S., & Merrot, T. (2017). Urgences chirurgicales du nouveau-né et du nourrisson. Journal de Pédiatrie et de Puériculture |résumé.
- Sapin, E., Kurzenne, J. Y., Bargy, F., Wakim, A., Esteve, C., Egu, J. F., & Helardot, P. G. (1988). Atrésie de l'œsophage chez les nouveau-nés de moins de 2000 grammes. À propos de 37 observations. Chirurgie pédiatrique, 29(5), 247-251.
- Garabedian, C., Vaast, P., Bigot, J., Sfeir, R., Michaud, L., Gottrand, F., ... & Debarge, V. H. (2014). Atrésie de l’œsophage: prévalence, diagnostic anténatal et pronostic. Journal de Gynécologie Obstétrique et Biologie de la Reproduction, 43(6), 424-430
- Maynard, S., & Bouin, M. (2011). L’atrésie de l’œsophage: une nouvelle maladie de l’adulte. Le clinicien, 51-4.
- Danzon, A., Robert, E., Collet, J. P., & Robert, J. M. (1988). Atrésies de l'œsophage. Étude d'un pic d'incidence observé en 1984 dans la région Rhône-Alpes. Archives françaises de pédiatrie, 45(4), 231-235.
- Depaepe, A., Dolk, H., & Lechat, M. F. (1993). The epidemiology of tracheo-oesophageal fistula and oesophageal atresia in Europe. EUROCAT Working Group. Archives of disease in childhood, 68(6), 743-748.
- Rappazzo, K. M., Warren, J. L., Meyer, R. E., Herring, A. H., Sanders, A. P., Brownstein, N. C., & Luben, T. J. (2016). Maternal residential exposure to agricultural pesticides and birth defects in a 2003 to 2005 North Carolina birth cohort. Birth Defects Research Part A: Clinical and Molecular Teratology, 106(4), 240-249 et illustration/schéma .
- Amar E (2017). [ Malformations et facteurs environnementaux]. Revue de médecine périnatale, 9(2), 73-80 |accès à l'étude.
- Howley, M. M., Carter, T. C., Browne, M. L., Romitti, P. A., Cunniff, C. M., Druschel, C. M., & Study, N. B. D. P. (2016). Fluconazole use and birth defects in the National Birth Defects Prevention Study. American journal of obstetrics and gynecology, 214(5), 657-e1 |résumé.
- Robin M.M (2017). Le Roundup face à ses juges. Ed. La Découverte.
- Mercier, C., Robert, M., Lacombe, A., Martin, L., Gold, F., & Laugier, J. (1984). Le reflux gastro-oesophagien après cure d'atrésie de l'œsophage. Archives françaises de pédiatrie, 41(7), 459-465 |résumé.
- Garabedian, C., Sfeir, R., Langlois, C., Bonnard, A., Khen-Dunlop, N., Gelas, T., ... & Fouquet, V. (2015). Le diagnostic anténatal modifie-t-il la prise en charge néonatale et le devenir à 1 an des enfants suivis pour atrésie de l’œsophage de type III?. Journal de Gynécologie Obstétrique et Biologie de la Reproduction, 44(9), 848-854.
- Chaumoitre, K., Amous, Z., Bretelle, F., Merrot, T., D’Ercole, C., & Panuel, M. (2004). https://www.academia.edu/download/43920632/Diagnostic_prnatal_datrsie_de_lsophage_p20160320-8536-11q3exl.pdf Diagnostic prénatal d’atrésie de l’œsophage par IRM]. Journal de Radiologie, 85(12), 2029-2031.
- reconstruction d'un œsophage
- Dubedout, S., Cascales, T., Mas, E., Bion, A., Vignes, M., Raynaud, J. P., & Olives, J. P. (2016). Troubles du comportement alimentaire restrictifs du nourrisson et du jeune enfant: situations à risque et facteurs favorisants. Archives de Pédiatrie, 23(6), 570-576
- Robert-Gnansia, E., Amar, E., Francannet, C., Patouraux, M. H., Bethenod, I., Desvignes, G., ... & Laborier, J. C. (2005). Le registre France Centre-Est de malformations congénitales. Environnement, Risques & Santé, 4(6), 385-393.
- Heresbach, D., Boustière, C., Michaud, L., Lachaux, A., Dabadie, A., Prat, F., & Laugier, R. (2010). des sténoses bénignes de l’œsophage chez l’adulte et l’enfant. Acta endoscopica, 40(4), 282-286.
- Arakelian, L., Vanneaux, V., Poghosyan, T., Catry, J., Luong-Nguyen, M., & Larghero, J. (2016). Reconstruction œsophagienne par ingénierie tissulaire-l’expérience de l’hôpital Saint-Louis. e-mémoires de l'Académie Nationale de Chirurgie, 15(2), 066-068.
- Poghosyan, T., Catry, J., Luong-Nguyen, M., Bruneval, P., Domet, T., Arakelian, L., ... & Larghero, J. (2016). L’ingénierie tissulaire de l’œsophage: états des lieux et perspectives. Journal de Chirurgie Viscérale, 153(1), 21-30|résumé.
Voir aussi
[modifier | modifier le code]Articles connexes
[modifier | modifier le code]Liens externes
[modifier | modifier le code]- HAS : Recommandations de la Haute Autorité de Santé pour le suivi des opérés de l'atrésie de l'œsophage.
- AFAO Association Française de l'Atrésie de l'Oesophage
- Page spécifique sur Orphanet.
Bibliographie
[modifier | modifier le code]- Bastard, F., Bonnard, A., Rousseau, V., Gelas, T., Michaud, L., Irtan, S., ... & Lamireau, T. (2017). Thoracic skeletal anomalies following surgical treatment of esophageal atresia. Lessons from a national cohort. Journal of Pediatric Surgery |résumé.
- Garabedian, C., Vaast, P., Bigot, J., Sfeir, R., Michaud, L., Gottrand, F., ... & Debarge, V. H. (2014). Atrésie de l’œsophage: prévalence, diagnostic anténatal et pronostic. Journal de Gynécologie Obstétrique et Biologie de la Reproduction, 43(6), 424-430
- Gottrand, F., Sfeir, R., Thumerelle, C., Gottrand, L., Fayoux, P., Storme, L., ... & Michaud, L. (2012). Devenir à moyen et long terme des enfants atteints d’atrésie de l’œsophage. Archives de pédiatrie, 19(9), 932-938.
- Schneider, A., Gottrand, F., Bellaiche, M., Becmeur, F., Lachaux, A., Dabadie, A., ... & Dupont, C. (2016). O-10 (11: 50 to 12: 02): Prevalence of Barrett Esophagus in Adolescents and Young Adults With Esophageal Atresia. Diseases of the Esophagus, 29(3), 288-288|résumé.


