« Virus Zika » : différence entre les versions
Bob Saint Clar a déplacé la page Virus Zika vers Infection à virus Zika : L'article traite de la maladie, pas du virus. Balise : Nouvelle redirection |
Création de l'article à partir d'une redirection. Balise : Redirection supprimée |
||
| Ligne 1 : | Ligne 1 : | ||
{{Autre4|le [[virus]]|la maladie provoquée par ce virus|Infection à virus Zika}} |
|||
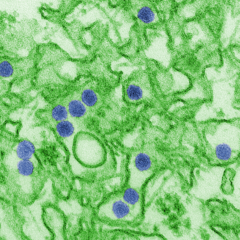
{{Taxobox début | virus | Virus Zika | Zika EM CDC 20541.png | [[Microscopie électronique en transmission]] colorisée montrant des particules virales Zika en violet, d'un diamètre d'environ {{unité|40|nm}}. }} |
|||
{{Taxobox | domaine | Riboviria }} |
|||
{{Taxobox | famille | Flaviviridae }} |
|||
{{Taxobox | genre | Flavivirus }} |
|||
{{Taxobox taxon | virus | espèce | ''Virus Zika'' | [[International Committee on Taxonomy of Viruses|ICTV]]<ref name="ICTV"> |
|||
{{Lien web |
|||
| langue = en |
|||
| url = https://talk.ictvonline.org/taxonomy/ |
|||
| titre = Virus Taxonomy: 2018b Release |
|||
| date = juillet 2018 |
|||
| éditeur = [[International Committee on Taxonomy of Viruses|ICTV]] |
|||
| consulté le = 14 juillet 2019 |
|||
}}.</ref> }} |
|||
{{Taxobox fin}} |
|||
Le '''virus Zika''' est l'[[agent infectieux]] à l'origine, chez l'[[Homo sapiens|homme]], de l'[[infection à virus Zika]]. Il s'agit d'un [[virus à ARN]] [[monocaténaire]] de [[Polarité (acide nucléique)|polarité]] positive, relevant donc du groupe {{IV}} de la [[classification Baltimore]], et appartenant au [[Genre (biologie)|genre]] ''[[Flavivirus]]''. Il est notamment apparenté aux [[virus de la dengue]], de la [[Virus de la fièvre jaune|fièvre jaune]], de l'[[Virus de l'encéphalite japonaise|encéphalite japonaise]] et du [[Virus du Nil occidental|Nil occidental]]<ref name="10.4103/0974-777X.176140"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Veronica Sikka, Vijay Kumar Chattu, Raaj K. Popli, Sagar C. Galwankar, Dhanashree Kelkar, Stanley G. Sawicki, Stanislaw P. Stawicki et Thomas J. Papadimos |
|||
| titre = The emergence of zika virus as a global health security threat: A review and a consensus statement of the INDUSEM Joint working Group (JWG) |
|||
| périodique = Journal of Global Infectious Diseases |
|||
| volume = 8 |
|||
| numéro = 1 |
|||
| jour = |
|||
| mois = janvier-mars |
|||
| année = 2016 |
|||
| pages = 3-15 |
|||
| url texte = |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.4103/0974-777X.176140 |
|||
| pmid = 27013839 |
|||
| pmc = 4785754 |
|||
}}</ref>. Il appartient au même [[sérogroupe]] que le [[virus Spondweni]]<ref name="10.1371/journal.pntd.0002636"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Oumar Faye, Caio C. M. Freire, Atila Iamarino, Ousmane Faye, Juliana Velasco C. de Oliveira, Mawlouth Diallo, Paolo M. A. Zanotto et Amadou Alpha Sall |
|||
| titre = Molecular Evolution of Zika Virus during Its Emergence in the 20{{exp|th}} Century |
|||
| périodique = PLoS Neglected Tropical Diseases |
|||
| volume = 8 |
|||
| numéro = 1 |
|||
| jour = |
|||
| mois = janvier |
|||
| année = 2014 |
|||
| numéro article = e2636 |
|||
| url texte = https://journals.plos.org/plosntds/article/file?id=10.1371/journal.pntd.0002636&type=printable |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.1371/journal.pntd.0002636 |
|||
| pmid = 24421913 |
|||
| bibcode = 3888466 |
|||
}}</ref>{{,}}<ref name="10.3201/eid1509.090442"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Edward B. Hayes |
|||
| titre = Zika Virus Outside Africa |
|||
| périodique = Emerging Infectious Diseases |
|||
| volume = 15 |
|||
| numéro = 9 |
|||
| jour = |
|||
| mois = septembre |
|||
| année = 2009 |
|||
| pages = 1347-1350 |
|||
| url texte = https://wwwnc.cdc.gov/eid/article/15/9/pdfs/09-0442.pdf |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.3201/eid1509.090442 |
|||
| pmid = 19788800 |
|||
| pmc = 2819875 |
|||
}}</ref>. |
|||
Ce [[virus enveloppé]] présente un [[génome]] non segmenté long de {{unité|10|[[kilobase]]s}}<ref name="10.1007/s00705-006-0903-z"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = G. Kuno et G.-J. J. Chang |
|||
| titre = Full-length sequencing and genomic characterization of Bagaza, Kedougou, and Zika viruses |
|||
| périodique = Archives of Virology |
|||
| volume = 152 |
|||
| numéro = 4 |
|||
| jour = |
|||
| mois = avril |
|||
| année = 2007 |
|||
| pages = 687-696 |
|||
| url texte = https://link.springer.com/content/pdf/10.1007%2Fs00705-006-0903-z.pdf |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.1007/s00705-006-0903-z |
|||
| pmid = 17195954 |
|||
| bibcode = |
|||
}}</ref> qui [[Code génétique|code]] trois [[protéine]]s structurelles et sept protéines non structurelles<ref name="10.1177/2040206616653873"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Bryan D. Cox, Richard A. Stanton et Raymond F. Schinazi |
|||
| titre = Predicting Zika virus structural biology: Challenges and opportunities for intervention |
|||
| périodique = Antiviral Chemistry and Chemotherapy |
|||
| volume = 24 |
|||
| numéro = 3-4 |
|||
| jour = |
|||
| mois = août |
|||
| année = 2015 |
|||
| pages = 118-126 |
|||
| url texte = https://journals.sagepub.com/doi/pdf/10.1177/2040206616653873 |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.1177/2040206616653873 |
|||
| pmid = 27296393 |
|||
| pmc = 5890524 |
|||
}}</ref>. L'une de ces protéines structurelles, la [[glycoprotéine]] d'[[Enveloppe virale|enveloppe]], encapsule le virus et se lie à la [[Système endomembranaire|membrane]] de l'[[endosome]] de la [[Cellule (biologie)|cellule]] [[Hôte (biologie)|hôte]] pour déclencher l'[[endocytose]]<ref name="10.1016/j.chom.2016.04.013"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Lianpan Dai, Jian Song, Xishan Lu, Yong-Qiang Deng, Abednego Moki Musyoki, Huijun Cheng, Yanfang Zhang, Yuan Yuan, Hao Song, Joel Haywood, Haixia Xiao, Jinghua Yan, Yi Shi, Cheng-Feng Qin, Jianxun Qi et George F. Gao |
|||
| titre = Structures of the Zika Virus Envelope Protein and Its Complex with a Flavivirus Broadly Protective Antibody |
|||
| périodique = Cell Host Microbe |
|||
| volume = 19 |
|||
| numéro = 5 |
|||
| jour = 11 |
|||
| mois = mai |
|||
| année = 2016 |
|||
| pages = 696-704 |
|||
| url texte = https://www.cell.com/action/showPdf?pii=S1931-3128%2816%2930149-4 |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.1016/j.chom.2016.04.013 |
|||
| pmid = 27158114 |
|||
| bibcode = |
|||
}}</ref>. L'[[Acide ribonucléique|ARN]] vérial forme une [[nucléocapside]] avec la protéine de [[capside]] de {{unité|12|[[Kilodalton|kDa]]}}. Cette nucléocapside est enveloppée dans une membrane dérivée de la [[membrane plasmique]] de la cellule hôte, modifiée avec deux glycoprotéines virales<ref name="10.1016/j.coviro.2012.02.011"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Theodore C. Pierson et Michael S. Diamond |
|||
| titre = Degrees of maturity: the complex structure and biology of flaviviruses |
|||
| périodique = Current Opinion in Virology |
|||
| volume = 2 |
|||
| numéro = 2 |
|||
| jour = |
|||
| mois = avril |
|||
| année = 2012 |
|||
| pages = 168-175 |
|||
| url texte = https://www.sciencedirect.com/science/article/pii/S1879625712000387 |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.1016/j.coviro.2012.02.011 |
|||
| pmid = 22445964 |
|||
| pmc = 3715965 |
|||
}}</ref>. La [[Réplication virale|réplication]] nécessite une [[ARN polymérase ARN-dépendante]]. |
|||
Une étude a montré que six heures après l'infection de cellules par le virus Zika, les [[vacuole]]s et les [[mitochondrie]]s de ces cellules commencent à enfler. Ce gonflement devient suffisamment sévère pour déclencher la {{Lien|langue=en|trad=Paraptosis|fr=paraptose}} des cellules. Cette forme de mort cellulaire programmée requiert l'[[Expression génétique|expression]] de certains [[gène]]s. |
|||
l'{{Lien|langue=en|trad=IFITM3|fr=IFITM3}} est une [[protéine transmembranaire]] des cellules capable de protéger ces dernière de l'infection virale en bloquant l'attachement du virus. Les cellules les plus sensibles à l'infection au virus Zika sont celles qui ont un faible taux de protéine IFITM3. Une fois les cellules infectées, le virus réorganise le [[réticulum endoplasmique]] en formant de grandes vacuoles, ce qui tue la cellule<ref name="10.15252/embj.201695597"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Blandine Monel, Alex A Compton, Timothée Bruel, Sonia Amraoui, Julien Burlaud‐Gaillard, Nicolas Roy, Florence Guivel‐Benhassine, Françoise Porrot, Pierre Génin, Laurent Meertens, Laura Sinigaglia, Nolwenn Jouvenet, Robert Weil, Nicoletta Casartelli, Caroline Demangel, Etienne Simon‐Lorière, Arnaud Moris, Philippe Roingeard, Ali Amara et Olivier Schwartz |
|||
| titre = Zika virus induces massive cytoplasmic vacuolization and paraptosis‐like death in infected cells |
|||
| périodique = The EMBO Journal |
|||
| volume = 36 |
|||
| numéro = 12 |
|||
| jour = 14 |
|||
| mois = juin |
|||
| année = 2017 |
|||
| pages = 1653-1668 |
|||
| url texte = https://www.embopress.org/doi/pdf/10.15252/embj.201695597 |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.15252/embj.201695597 |
|||
| pmid = 28473450 |
|||
| bibcode = 5470047 |
|||
}}</ref>. |
|||
Il existe deux lignées de virus Zika, l'une originaire d'[[Afrique]] et l'autre d'[[Asie]]<ref name="10.1016/S0140-6736(16)00003-9"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Antoine Enfissi, John Codrington, Jimmy Roosblad, Mirdad Kazanji et Dominique Rousset |
|||
| titre = Zika virus genome from the Americas |
|||
| périodique = The Lancet |
|||
| volume = 387 |
|||
| numéro = 10015 |
|||
| jour = 16 |
|||
| mois = janvier |
|||
| année = 2016 |
|||
| pages = 227-228 |
|||
| url texte = https://www.thelancet.com/action/showPdf?pii=S0140-6736%2816%2900003-9 |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.1016/S0140-6736(16)00003-9 |
|||
| pmid = 26775124 |
|||
| bibcode = |
|||
}}</ref>. Des études [[Phylogénie|phylogénétiques]] indique que le virus qui se propage sur le continent américain est identique à 89 % aux [[génotype]] africains mais est apparenté plus étroitement aux souches asiatiques qui ont circulé en [[Polynésie française]] au cours de l'épidémie de 2013-2014<ref name="10.1590/0074-02760150192"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Camila Zanluca, Vanessa Campos Andrade de Melo, Ana Luiza Pamplona Mosimann, Glauco Igor Viana dos Santos, Claudia Nunes Duarte dos Santos et Kleber Luz |
|||
| titre = First report of autochthonous transmission of Zika virus in Brazil |
|||
| périodique = Memórias do Instituto Oswaldo Cruz |
|||
| volume = 110 |
|||
| numéro = 4 |
|||
| jour = |
|||
| mois = juin |
|||
| année = 2015 |
|||
| pages = 569-572 |
|||
| url texte = http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0074-02762015000400569&lng=en&tlng=en |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.1590/0074-02760150192 |
|||
| pmid = 26061233 |
|||
| pmc = 4501423 |
|||
}}</ref>{{,}}<ref name="10.3201/eid2205.160065"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Robert S. Lanciotti, Amy J. Lambert, Mark Holodniy, Sonia Saavedra et Leticia del Carmen Castillo Signor |
|||
| titre = Phylogeny of Zika Virus in Western Hemisphere, 2015 |
|||
| périodique = Emerging Infectious Diseases |
|||
| volume = 22 |
|||
| numéro = 5 |
|||
| jour = |
|||
| mois = mai |
|||
| année = 2016 |
|||
| pages = 933-935 |
|||
| url texte = https://wwwnc.cdc.gov/eid/article/22/5/pdfs/16-0065.pdf |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.3201/eid2205.160065 |
|||
| pmid = 27088323 |
|||
| pmc = 4861537 |
|||
}}</ref>. |
|||
La souche asiatique semble s'être différentiée aux alentours de 1928<ref name="10.1016/j.meegid.2017.03.012"> |
|||
{{Article |
|||
| langue = en |
|||
| nom1 = Arunachalam Ramaiaha, Lei Dai, Deisy Contreras, Sanjeev Sinha, Ren Sun, Vaithilingaraja Arumugaswami |
|||
| titre = Comparative analysis of protein evolution in the genome of pre-epidemic and epidemic Zika virus |
|||
| périodique = Infection, Genetics and Evolution |
|||
| volume = 51 |
|||
| numéro = |
|||
| jour = |
|||
| mois = juillet |
|||
| année = 2017 |
|||
| pages = 74-85 |
|||
| url texte = https://www.sciencedirect.com/science/article/pii/S1567134817300837 |
|||
| consulté le = 14 juillet 2019 |
|||
| doi = 10.1016/j.meegid.2017.03.012 |
|||
| pmid = 28315476 |
|||
| bibcode = |
|||
}}</ref>. |
|||
== Notes et références == |
|||
{{Références}} |
|||
{{Portail|virologie}} |
|||
[[Catégorie:Flavivirus|Zika]] |
|||
[[Catégorie:Arbovirus]] |
|||
Version du 14 juillet 2019 à 23:30
| Domaine | Riboviria |
|---|---|
| Famille | Flaviviridae |
| Genre | Flavivirus |
Le virus Zika est l'agent infectieux à l'origine, chez l'homme, de l'infection à virus Zika. Il s'agit d'un virus à ARN monocaténaire de polarité positive, relevant donc du groupe IV de la classification Baltimore, et appartenant au genre Flavivirus. Il est notamment apparenté aux virus de la dengue, de la fièvre jaune, de l'encéphalite japonaise et du Nil occidental[2]. Il appartient au même sérogroupe que le virus Spondweni[3],[4].
Ce virus enveloppé présente un génome non segmenté long de 10 kilobases[5] qui code trois protéines structurelles et sept protéines non structurelles[6]. L'une de ces protéines structurelles, la glycoprotéine d'enveloppe, encapsule le virus et se lie à la membrane de l'endosome de la cellule hôte pour déclencher l'endocytose[7]. L'ARN vérial forme une nucléocapside avec la protéine de capside de 12 kDa. Cette nucléocapside est enveloppée dans une membrane dérivée de la membrane plasmique de la cellule hôte, modifiée avec deux glycoprotéines virales[8]. La réplication nécessite une ARN polymérase ARN-dépendante.
Une étude a montré que six heures après l'infection de cellules par le virus Zika, les vacuoles et les mitochondries de ces cellules commencent à enfler. Ce gonflement devient suffisamment sévère pour déclencher la paraptose (en) des cellules. Cette forme de mort cellulaire programmée requiert l'expression de certains gènes.
l'IFITM3 (en) est une protéine transmembranaire des cellules capable de protéger ces dernière de l'infection virale en bloquant l'attachement du virus. Les cellules les plus sensibles à l'infection au virus Zika sont celles qui ont un faible taux de protéine IFITM3. Une fois les cellules infectées, le virus réorganise le réticulum endoplasmique en formant de grandes vacuoles, ce qui tue la cellule[9].
Il existe deux lignées de virus Zika, l'une originaire d'Afrique et l'autre d'Asie[10]. Des études phylogénétiques indique que le virus qui se propage sur le continent américain est identique à 89 % aux génotype africains mais est apparenté plus étroitement aux souches asiatiques qui ont circulé en Polynésie française au cours de l'épidémie de 2013-2014[11],[12].
La souche asiatique semble s'être différentiée aux alentours de 1928[13].
Notes et références
- (en) « Virus Taxonomy: 2018b Release », ICTV, (consulté le ).
- (en) Veronica Sikka, Vijay Kumar Chattu, Raaj K. Popli, Sagar C. Galwankar, Dhanashree Kelkar, Stanley G. Sawicki, Stanislaw P. Stawicki et Thomas J. Papadimos, « The emergence of zika virus as a global health security threat: A review and a consensus statement of the INDUSEM Joint working Group (JWG) », Journal of Global Infectious Diseases, vol. 8, no 1, , p. 3-15 (PMID 27013839, PMCID 4785754, DOI 10.4103/0974-777X.176140)
- (en) Oumar Faye, Caio C. M. Freire, Atila Iamarino, Ousmane Faye, Juliana Velasco C. de Oliveira, Mawlouth Diallo, Paolo M. A. Zanotto et Amadou Alpha Sall, « Molecular Evolution of Zika Virus during Its Emergence in the 20th Century », PLoS Neglected Tropical Diseases, vol. 8, no 1, , article no e2636 (PMID 24421913, DOI 10.1371/journal.pntd.0002636, Bibcode 3888466, lire en ligne)
- (en) Edward B. Hayes, « Zika Virus Outside Africa », Emerging Infectious Diseases, vol. 15, no 9, , p. 1347-1350 (PMID 19788800, PMCID 2819875, DOI 10.3201/eid1509.090442, lire en ligne)
- (en) G. Kuno et G.-J. J. Chang, « Full-length sequencing and genomic characterization of Bagaza, Kedougou, and Zika viruses », Archives of Virology, vol. 152, no 4, , p. 687-696 (PMID 17195954, DOI 10.1007/s00705-006-0903-z, lire en ligne)
- (en) Bryan D. Cox, Richard A. Stanton et Raymond F. Schinazi, « Predicting Zika virus structural biology: Challenges and opportunities for intervention », Antiviral Chemistry and Chemotherapy, vol. 24, nos 3-4, , p. 118-126 (PMID 27296393, PMCID 5890524, DOI 10.1177/2040206616653873, lire en ligne)
- (en) Lianpan Dai, Jian Song, Xishan Lu, Yong-Qiang Deng, Abednego Moki Musyoki, Huijun Cheng, Yanfang Zhang, Yuan Yuan, Hao Song, Joel Haywood, Haixia Xiao, Jinghua Yan, Yi Shi, Cheng-Feng Qin, Jianxun Qi et George F. Gao, « Structures of the Zika Virus Envelope Protein and Its Complex with a Flavivirus Broadly Protective Antibody », Cell Host Microbe, vol. 19, no 5, , p. 696-704 (PMID 27158114, DOI 10.1016/j.chom.2016.04.013, lire en ligne)
- (en) Theodore C. Pierson et Michael S. Diamond, « Degrees of maturity: the complex structure and biology of flaviviruses », Current Opinion in Virology, vol. 2, no 2, , p. 168-175 (PMID 22445964, PMCID 3715965, DOI 10.1016/j.coviro.2012.02.011, lire en ligne)
- (en) Blandine Monel, Alex A Compton, Timothée Bruel, Sonia Amraoui, Julien Burlaud‐Gaillard, Nicolas Roy, Florence Guivel‐Benhassine, Françoise Porrot, Pierre Génin, Laurent Meertens, Laura Sinigaglia, Nolwenn Jouvenet, Robert Weil, Nicoletta Casartelli, Caroline Demangel, Etienne Simon‐Lorière, Arnaud Moris, Philippe Roingeard, Ali Amara et Olivier Schwartz, « Zika virus induces massive cytoplasmic vacuolization and paraptosis‐like death in infected cells », The EMBO Journal, vol. 36, no 12, , p. 1653-1668 (PMID 28473450, DOI 10.15252/embj.201695597, Bibcode 5470047, lire en ligne)
- (en) Antoine Enfissi, John Codrington, Jimmy Roosblad, Mirdad Kazanji et Dominique Rousset, « Zika virus genome from the Americas », The Lancet, vol. 387, no 10015, , p. 227-228 (PMID 26775124, DOI 10.1016/S0140-6736(16)00003-9, lire en ligne)
- (en) Camila Zanluca, Vanessa Campos Andrade de Melo, Ana Luiza Pamplona Mosimann, Glauco Igor Viana dos Santos, Claudia Nunes Duarte dos Santos et Kleber Luz, « First report of autochthonous transmission of Zika virus in Brazil », Memórias do Instituto Oswaldo Cruz, vol. 110, no 4, , p. 569-572 (PMID 26061233, PMCID 4501423, DOI 10.1590/0074-02760150192, lire en ligne)
- (en) Robert S. Lanciotti, Amy J. Lambert, Mark Holodniy, Sonia Saavedra et Leticia del Carmen Castillo Signor, « Phylogeny of Zika Virus in Western Hemisphere, 2015 », Emerging Infectious Diseases, vol. 22, no 5, , p. 933-935 (PMID 27088323, PMCID 4861537, DOI 10.3201/eid2205.160065, lire en ligne)
- (en) Arunachalam Ramaiaha, Lei Dai, Deisy Contreras, Sanjeev Sinha, Ren Sun, Vaithilingaraja Arumugaswami, « Comparative analysis of protein evolution in the genome of pre-epidemic and epidemic Zika virus », Infection, Genetics and Evolution, vol. 51, , p. 74-85 (PMID 28315476, DOI 10.1016/j.meegid.2017.03.012, lire en ligne)