Syndrome de Stevens-Johnson
| Spécialité | Dermatologie |
|---|
| CIM-10 | L51.1 |
|---|---|
| CIM-9 | 695.13 |
| OMIM | 608579 |
| DiseasesDB | 4450 |
| MedlinePlus | 000851 |
| eMedicine | 1197450 |
| MeSH | D013262 |
| Patient UK | Stevens-johnson-syndrome |
Le syndrome de Stevens-Johnson (ectodermosis erosiva pluriorificialis ou dermatostomatite ou ectodermose érosive pluriorificielle de Fiessinger-Rendu) est une maladie orpheline grave, de survenue brutale, et potentiellement mortelle (15 % des cas).
C'est une maladie souvent provoquée par des médicaments, surtout les sulfamides, touchant la peau et les membranes muqueuses, forme grave d'érythème polymorphe (on l'appelle également erythema multiforme major).
Il est caractérisé par plusieurs symptômes, pouvant ou non être associés : de la fièvre, l'atteinte simultanée de plusieurs muqueuses (une conjonctivite purulente, des efflorescences dans la bouche, le nez, le pénis ou la vulve, l'anus...), la destruction par nécrose de la couche superficielle de la peau, l'atteinte de certains organes internes, des myalgies et un méléna.
Symptômes[modifier | modifier le code]
Ils surviennent entre 4 et 28 jours après la prise médicamenteuse[1].
Le syndrome de Stevens-Johnson est caractérisé par de la fièvre, une altération de l'état général et des céphalées.
Le premier symptôme est généralement une atteinte simultanée de plusieurs muqueuses (bouche, gorge, nez, yeux, pénis, vulve et/ou anus). Rapidement apparaissent des lésions cutanées polymorphes appelées lésions en cocarde (macule érythémateuse circulaire, en anglais target lesions = lésions en cible) qui peuvent recouvrir la plus grande partie de la peau mais se concentrent au niveau du thorax, du visage et de la racine des membres[1]. Ces lésions commencent sous forme de macules et peuvent devenir des papules, des vésicules, des plaques d'urticaire ou des plaques purpuriques. Un signe de Nikolsky peut être présent. On note également des lésions bulleuses et érosives, pouvant saigner et être douloureuses, des muqueuses au niveau de certains orifices naturels tel les narines et la bouche, des muqueuses génitales et les conjonctives. Les bulles peuvent se rejoindre et ainsi aboutir à un décollement plus ou moins étendu de la peau. La surface de la peau atteinte par la maladie est inférieure à 10 %[1]. Les cas les plus extrêmes sont appelés syndrome de nécrolyse épidermique toxique ou syndrome de Lyell : dans ces cas, plus de 30 % la surface de la peau est atteinte.
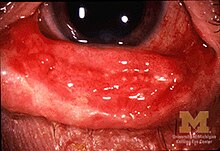
L'atteinte de la muqueuse oro-pharyngée est fréquente[2].
L'atteinte oculaire est présente dans trois quarts des cas[3] avec des lésions conjonctivales pouvant évoluer vers des ulcères, une uvéite, une conjonctivite purulente.
Les organes internes sont parfois atteints. Une atteinte bronchique existe dans un quart des cas, nécessitant souvent une ventilation assistée avec une mortalité importante[4].
Diagnostic[modifier | modifier le code]
Il repose sur la biopsie de la peau lésée[1].
Causes[modifier | modifier le code]
La cause principale reste très majoritairement une toxidermie médicamenteuse, même si certaines bactéries et virus peuvent aussi en être à l’origine. Tous les médicaments peuvent a priori être à l’origine de ces réactions, mais on retrouve très souvent impliquées dans ces accidents la même demi-douzaine de molécules bien connues : ces molécules sont considérées « à risques » ou « à très hauts risques ».
Les médicaments à risques identifiés sont : les sulfamides antibactériens, les anticomitiaux, certains anti-inflammatoires non stéroïdiens, l’allopurinol, la névirapine (un anti-VIH), la duloxétine (un antidépresseur). On observe en moyenne un cas pour 100 000 nouveaux utilisateurs d’une molécule à risque. Pour certaines molécules, ce risque monte au-delà d’un sur 10 000. Ainsi, la névirapine provoque un accident tous les 300 utilisateurs et la lamotrigine, un sur 50, lorsqu’elle est utilisée chez les enfants. Le risque est beaucoup plus faible pour de nombreux antibiotiques. Une origine médicamenteuse est retrouvée dans deux tiers des cas[5].
Ce syndrome est également une complication possible des affections pulmonaires à Mycoplasma pneumoniae[6].
Il existe des facteurs favorisants génétiques : présence d'un HLA B*5801[7] ou B*1502[8].
Physiopathologie[modifier | modifier le code]
Le syndrome est une réaction allergique de type cellulaire impliquant les lymphocytes T[1]. La molécule médicamenteuse en cause peut interagir avec certains antigènes de type HLA B ce qui permet l'activation des cellules T[9].
Traitement[modifier | modifier le code]
La prise en charge du syndrome a fait l'objet de recommandations. Celles de l'HAS datent de 2010[10]. Les recommandations anglaises datent de 2016[11].
Il n'existe à l'heure actuelle aucun traitement spécifique.
Malgré tout, certaines mesures peuvent être prises :
- l'éviction du médicament responsable, avec un meilleur pronostic si cet arrêt est rapide[12] ;
- les soins locaux des lésions érosives limitant les risques infectieux secondaires, avec application de produits hydratants sur les muqueuses atteintes[1] ;
- la surveillance des paramètres de l'hydratation et de la nutrition.
Les corticoïdes[13], ainsi que l'injection de fortes doses d'immunoglobuline[1], n'ont pas fait la preuve de leur efficacité. La ciclosporine pourrait avoir un intérêt mais le niveau de preuve reste faible[14], de même que pour l'étanercept[15].
Séquelles[modifier | modifier le code]
Une majorité de survivants doit vivre avec de multiples séquelles douloureuses et invalidantes, tant sur le plan sensoriel (cécité), moteur (baisse de la capacité respiratoire) qu'esthétique (séquelles dermatologiques…).
Les séquelles oculaires, dont souffrent plus de la moitié des survivants, sont dues à des atteintes sévères de la cornée souvent par un ectropion séquellaire, et de la conjonctive et dégradent petit à petit la vision, souvent jusqu’à la cécité. La chirurgie réparatrice est impuissante à ce jour. Elles se traduisent par une photophobie sévère et douloureuse (obligeant au port de lunettes noires) et à une sécheresse oculaire prononcée (nécessitant l’instillation régulière, parfois toutes les 5 minutes, de larmes artificielles).
La phobie des médicaments, bien compréhensible, est une autre séquelle de ces syndromes, qui peut gêner gravement le traitement de maladies ultérieures. Les autres séquelles sont :
- des troubles psychologiques (chocs post-traumatiques), qui touchent non seulement les survivants mais aussi leur entourage ;
- des troubles et incapacités respiratoires sévères (asthme, bronchites chroniques, insuffisance respiratoire…) ;
- des cicatrices disgracieuses et des troubles de la pigmentation esthétiquement invalidants ;
- des problèmes buccodentaires (caries à répétition, ulcérations buccales, troubles de la salivation…) ;
- des séquelles gynécologiques : cicatrices génitales et muqueuses hypersensibles gênant les rapports sexuels, infertilité féminine, troubles hormonaux…
Et aussi : des anomalies de la sueur, des anomalies immunitaires, des troubles de la circulation (phlébites), des troubles digestifs, des risques d’hépatites médicamenteuses, de la fatigue chronique, etc.
Ces séquelles ne bénéficient pas de traitements curatifs à ce jour. Nombre d’entre elles sont de nature à dégrader les conditions de vie et à réduire l’espérance de vie.
Étymologie[modifier | modifier le code]
Ce syndrome doit son nom à deux pédiatres américains, Albert Mason Stevens et Frank Chambliss Johnson. En France, cette affection fut décrite par Noël Fiessinger et Henri Rendu[16].
Notes et références[modifier | modifier le code]
- Duong TA, Valeyrie-Allanore, L, Wolkenstein P, Chosidow O, Severe cutaneous adverse reactions to drugs, Lancet, 2017;390:1996–2011
- Bequignon E, Duong TA, Sbidian E et al. Stevens-Johnson syndrome and toxic epidermal necrolysis: ear, nose, and throat description at acute stage and after remission, JAMA Dermatol, 2015;151:302–307
- Gueudry J, Roujeau J-C, Binaghi M, Soubrane G, Muraine M, Risk factors for the development of ocular complications of Stevens-Johnson syndrome and toxic epidermal necrolysis, Arch Dermatol, 2009;145:157–162
- Lebargy F, Wolkenstein P, Gisselbrecht M et al. Pulmonary complications in toxic epidermal necrolysis: a prospective clinical study, Intensive Care Med, 1997;23:1237–1244
- Sassolas B, Haddad C, Mockenhaupt M et al. ALDEN, an algorithm for assessment of drug causality in Stevens-Johnson Syndrome and toxic epidermal necrolysis: comparison with case-control analysis, Clin Pharmacol Ther, 2010;88:60–68
- « Mycoplasma pneumoniae infection is associated with Stevens-Johnson syndrome, not erythema multiforme (von Hebra) »
- Hung SI, Chung WH, Liou LB et al. HLA–B*58:01 allele as a genetic marker for severe cutaneous adverse reactions caused by allopurinol, Proc Natl Acad Sci USA, 2005;102:4134–4139
- Cheng CY, Su SC, Chen CH, Chen -L, Deng ST, Chung WH. HLA associations and clinical implications in T-cell mediated drug hypersensitivity reactions: an updated review, J Immunol Res, 2014;2014:565320
- Wei CY, Chung WH, Huang HW, Chen YT, Hung SI, Direct interaction between HLA-B and carbamazepine activates T cells in patients with Stevens-Johnson syndrome, J Allergy Clin Immunol, 2012;129:1562 (69.e5)
- Haute Autorité de la Santé, Necrolyse epidermique toxique syndrome de Stevens Johnson et de Lyell. Protocole national de soins
- Creamer D, Walsh SA, Dziewulski P et al. UK guidelines for the management of Stevens-Johnson syndrome/toxic epidermal necrolysis in adults 2016, Br J Dermatol, 2016;174:1194–1227
- Garcia-Doval I, LeCleach L, Bocquet H, Otero XL, Roujeau JC. Toxic epidermal necrolysis and Stevens-Johnson syndrome: does early withdrawal of causative drugs decrease the risk of death?, Arch Dermatol, 2000;136:323–327
- Schneck J, Fagot JP, Sekula P, Sassolas B, Roujeau JC, Mockenhaupt M, Effects of treatments on the mortality of Stevens-Johnson syndrome and toxic epidermal necrolysis: a retrospective study on patients included in the prospective EuroSCAR Study, J Am Acad Dermatol, 2008;58:33–40
- Kirchhof MG, Miliszewski MA, Sikora S, Papp A, Dutz JP, Retrospective review of Stevens-Johnson syndrome/toxic epidermal necrolysis treatment comparing intravenous immunoglobulin with cyclosporine, J Am Acad Dermatol, 2014;71:941–947
- Paradisi A, Abeni D, Bergamo F, Ricci F, Didona D, Didona B, Etanercept therapy for toxic epidermal necrolysis, J Am Acad Dermatol, 2014;71:278–283
- « medicopedia.net/term/22463,1,x… »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?).

