Pentoxifylline
| Pentoxifylline | |
| |
| Identification | |
|---|---|
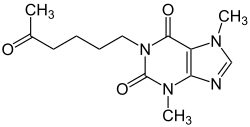
| Nom UICPA | 3,7-diméthyl-1-(5-oxohexyl)-3,7-dihydro-1H-purine-2,6-dione |
| No CAS | |
| No ECHA | 100.026.704 |
| Code ATC | C04 |
| DrugBank | APRD00121 |
| PubChem | |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C13H18N4O3 [Isomères] |
| Masse molaire[1] | 278,307 ± 0,013 4 g/mol C 56,1 %, H 6,52 %, N 20,13 %, O 17,25 %, |
| Données pharmacocinétiques | |
| Biodisponibilité | ~100 % PO, |
| Liaison protéique | 65 % |
| Métabolisme | hépatique et érythrocytaire |
| Demi-vie d’élim. | 0,4 à 0,8 h |
| Excrétion |
essentiellement dans les urines |
| Considérations thérapeutiques | |
| Classe thérapeutique | vasodilatateur périphérique |
| Voie d’administration | PO, IV |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La pentoxifylline est un médicament dérivé de la xanthine. Disponible sous forme générique, c'est une molécule initialement produite par Aventis et vendue sous les noms commerciaux de Torental (en France, ne se fait plus), Trental, Pentox, Pentoxil et Flexital. Son nom chimique est 1-(5-oxohexyl)-3, 7-diméthylxanthine.
| pentoxifylline | |
| Informations générales | |
|---|---|
| Princeps |
|
| Classe | Vasodilatateurs périphériques, dérivés purinniques, ATC code C04AD03 |
| Forme | comprimés à libération prolongée dosés à 400 mg, sachet de 2 grammes pour la forme vétérinaire |
| Administration | per os |
| Laboratoire | AA Pharma Inc., Biogaran, European Generics (EG), Mylan, Qualimed, Ratiopharm, RPG, Sandoz, Teva, Vetoquinol, |
| Identification | |
| No CAS | |
| No ECHA | 100.026.704 |
| Code ATC | C04AD03 |
| DrugBank | 00806 |
| modifier |
|
Indications AMM en France[modifier | modifier le code]
- Manifestation douloureuse des artériopathies en poussée ischémique de stade II[2]
- Déficit pathologique cognitif et neurosensoriel chronique du sujet âgé[2]
Devant le peu d'efficacité dans ces indications, ce traitement n'est plus remboursé en France depuis le [3].
Évaluation de l'efficacité[modifier | modifier le code]
Dans l'AOMI[modifier | modifier le code]
La commission de transparence de la HAS donne un service médical rendu (SMR) insuffisant. Le traitement de l'artériopathie oblitérante des membres inférieurs (AOMI) avec cette molécule rentre dans le cadre d'un traitement symptomatique. D'après elle, les études sont de mauvaise qualité, aucune comparaison n'a été faite contre l'antalgique de référence, le paracétamol. L'impact sur la morbidité ou la mortalité n'a pas été mesuré. Le rapport efficacité/effets indésirables est mal établi. Il n'y a pas d'étude montrant un effet des vasodilatateurs sur les complications systémiques de la maladie athéromateuse ni sur le caractère préventif. Une différence significative du périmètre de arche a été observée par rapport au placebo. Elle n'est pas recommandée par les recommandations hollandaises, canadiennes ni par l'American College of Clinical Pharmacy[4].
Dans le déficit pathologique cognitif et neurosensoriel chronique du sujet âgé[modifier | modifier le code]
La commission de transparence de la HAS donne un service médical rendu (SMR) insuffisant. Cette entité est mal définie. Le traitement des troubles cognitifs et neurosensoriel avec cette molécule rentre dans le cadre d'un traitement symptomatique. Aucune étude clinique dans cette indication n'a été faite. L'efficacité n'est pas établie. Il n'a pas été retrouvé de recommandation européenne ou internationale préconisant cette prescription[4].
Recherche et histoire de l'utilisation[modifier | modifier le code]
Elle était utilisée pour traiter l'artériopathie oblitérante des membres inférieurs résultant d'artères obstruées dans les membres, et la démence vasculaire.
Elle a été utilisée pour le traitement conservateur de la maladie de La Peyronie et les lésions neuropathiques. Elle aiderait aussi à prévenir les accidents vasculaires cérébraux, elle a été utilisée dans la drépanocytose et améliorerait la circulation sanguine vers le cerveau.
Elle a également été utilisée pour traiter les nausées et maux de tête en montagne (mal d'altitude) et a montré une réduction de la mortalité dans l'hépatite alcoolique aiguë et non-alcoolique, sans doute grâce à sa capacité à inhiber le TNF-alpha.
Par ses propriétés anti-TNF, elle serait utile pour le traitement des maladies du foie liées à l'alcool.
Une étude a montré l'utilisation possible de la pentoxifylline en association avec la vitamine E pour réduire l'étendue des lésions de fibrose induites par la radiothérapie pour le cancer du sein[5].
Un prétraitement oral ou IV avec la pentoxifylline a été tenté pour le traitement du syndrome de relargage des cytokines mais elle n'empêche pas les symptômes dans la plupart des études.
La pentoxifylline a aussi été étudiée dans le traitement de l'endométriose. Elle a aussi été utilisée dans le traitement de l'insuffisance veineuse.
L'association de la pentoxifylline avec la rispéridone pendant 8 semaines s'est avérée prometteuse pour atténuer les symptômes négatifs chez les patients atteints de schizophrénie chronique[6].
Mécanisme[modifier | modifier le code]
Comme les autres dérivés méthylés de la xanthine, la pentoxifylline est un inhibiteur compétitif non sélectif de la phosphodiestérase PDE4 augmentant l'AMPc intracellulaire et en stimulant l'activité PKA, inhibe la synthèse de TNF et de leukotriène et réduit l'inflammation et l'immunité innée.
Par ailleurs, la pentoxifylline augmente la déformabilité des globules rouges, réduit la viscosité sanguine et diminue le potentiel d'agrégation plaquettaire et la formation de thrombus. Elle a donc un effet hémorragique.
La pentoxifylline est aussi connue comme antagoniste des récepteurs à l'adénosine 2.
Interactions médicamenteuses[modifier | modifier le code]
La coadministration de pentoxifylline et de thiopental de sodium pourrait causer la mort par œdème aigu du poumon chez les rats. La molécule passe dans le lait maternel. Des études animales n'ont montré aucune preuve de risque tératogène à fortes doses.
Effets indésirables[modifier | modifier le code]
- Réaction anaphylactique avec choc[7]
- Augmentation du risque hémorragique surtout sous anticoagulant[7]
- Méningite aseptique[7]
- Nausées transitoires, vomissements, brûlures gastriques, diarrhée[4]
- Thrombopénie, cytolyse hépatique[4]
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Base Claude Bernard consultée le 27 juin 2012
- Prescrire, avril 2012, vol. 32, no 342, p. 260.
- Avis de la commission de transparence de la HAS du 31 mai 2006
- http://www.cea-technologies.com/articles/article/45/fr
- Mahmoud S. Abdallah, Esraa M. Mosalam, Ahmed Hassan et Ahmed N. Ramadan, « Pentoxifylline as an adjunctive in treatment of negative symptoms in chronic schizophrenia: A double-blind, randomized, placebo-controlled trial », CNS neuroscience & therapeutics, (ISSN 1755-5949, PMID 36341700, DOI 10.1111/cns.14010, lire en ligne, consulté le )
- Revue Prescrire juin 2003 tome 23 no 240 p. 432
Liens externes[modifier | modifier le code]
- Page spécifique dans la base de données sur les produits pharmaceutiques (Canada)
- Page spécifique sur le Répertoire Commenté des Médicaments, par le Centre belge d'information pharmacothérapeutique
- Page spécifique sur le Vidal.fr
- Trental information from Aventis
- Reprinted article on veterinary use
