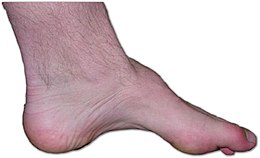
Maladie de Charcot-Marie-Tooth
| Causes | Mutation |
|---|---|
| Symptômes | Faiblesse musculaire (en), fonte musculaire, pied creux, déficit sensoriel (en), hyporéflexie (en) et scoliose |
| Traitement | Inconnu (d) et physiothérapie |
|---|---|
| Spécialité | Neurologie |
| OMIM | 311860 |
|---|---|
| DiseasesDB | et 2343.htm 5815 et 2343 |
| MedlinePlus | 000727 |
| eMedicine | 1232386 |
| MeSH | D002607 |
Les maladies de Charcot-Marie-Tooth, ou CMT, sont un ensemble de maladies neurologiques génétiques parmi les plus fréquentes. Ces maladies génétiques rares concernent environ 1 naissance sur 2 500 en France.
Les CMT ne doivent pas être confondues avec la maladie de Charcot ou sclérose latérale amyotrophique qui est beaucoup plus grave.
Décrite en 1886 par le neurologue français Jean-Martin Charcot et son étudiant Pierre Marie, puis par le neurologue britannique Howard Henry Tooth (en), la CMT est une neuropathie héréditaire sensitivo-motrice qui n’affecte pas l’espérance de vie et n’entraîne pas de retard mental. Elle touche indifféremment l’homme ou la femme. Schématiquement, la CMT est liée à l’atteinte des nerfs périphériques, reliant la moelle épinière aux muscles, ce qui perturbe la conduction de l’influx nerveux. Elle entraîne des troubles de la marche et une déformation fréquente des pieds (pieds creux). Cette maladie peut se déclarer dès l'enfance, mais également se développer assez tard, à l’âge adulte[1]. En général, la CMT évolue lentement mais elle peut aussi progresser par poussées.
Principaux symptômes
[modifier | modifier le code]Les principaux symptômes sont :
- une faiblesse musculaire progressive touchant en priorité les extrémités des membres ;
- une atrophie musculaire pouvant entraîner une déformation des pieds et des mains ;
- une perte de la sensibilité[2].
Classification
[modifier | modifier le code]Les différents types de maladies de Charcot-Marie-Tooth (CMT) sont classés selon trois critères[3] :
- la partie du nerf atteinte (myéline ou axone). Le critère utilisé est basé sur la vitesse de conduction de l'influx nerveux déterminée par électromyogramme. Dans le cas de l'atteinte de la myéline, cette vitesse est bien plus faible que dans le cas de l'atteinte de l'axone. Il existe également des CMT ayant une vitesse de conduction intermédiaire, classées à part ;
- le mode de transmission génétique (dominante ou récessive ou lié au chromosome X). La détermination de ce mode par le médecin résulte en grande partie d'un questionnement du patient sur l'historique de la maladie au sein de sa famille ;
- l'anomalie génétique cause de la maladie (en 2017, une soixantaine de gènes ont été identifiés).
Les deux premiers critères permettent de classer les CMT en six grands types (CMT1, CMT2, CMT4, CMTX, DI-CMT, RI-CMT), chaque type étant divisé en sous-types en fonction du troisième critère.
La variante la plus fréquente de la CMT est la CMT1A (48% des personnes atteintes), suivie de la CMT2A (6 %), la CMT1B (3 %), la CMT4C (2,5 %), la CMTX1 (2 %). Les symptômes les plus fréquents sont une instabilité des chevilles (52 %), des chutes (42 %) et une faiblesse de la main (42 %). L'atteinte est plus sévère pour la CMT2A, la CMT1B et la CMT4C que pour la CMT1A ou la CMTX1[3].
Formes démyélinisantes de la CMT
[modifier | modifier le code]Dans ces types de CMT, c'est la myéline, gaine isolante entourant les nerfs, qui est atteinte. Il en résulte une baisse caractéristique de la vitesse de transmission de l'influx nerveux, souvent inférieure à 20 m/s. Ce type de CMT se traduit souvent dès la petite enfance par des difficultés en gymnastique.
On distingue :
- les CMT1, dont la transmission est autosomique dominante[4] ;
- les CMT4, dont la transmission est autosomique récessive[5].
Formes axonales de la CMT
[modifier | modifier le code]Dans ces types de CMT, c'est l'axone conduisant l'influx nerveux, qui est atteint. La vitesse de conduction de l'influx nerveux n'est pas affectée (de l'ordre de 40 m/s), mais c'est l'intensité du signal électrique qui est diminuée. Elles constituent le type CMT2. On y distingue :
- les CMT2 proprement dites, dont la transmission est autosomique dominante ;
- les AR-CMT2, dont la transmission est autosomique récessive.
Formes intermédiaires de la CMT
[modifier | modifier le code]On y regroupe des formes de CMT, où la vitesse de conduction de l'influx nerveux est comprise entre 25 m/s et 40 m/s. On distingue :
- les DI-CMT, dont la transmission est autosomique dominante ;
- les RI-CMT, dont la transmission est autosomique récessive ;
- les CMTX dont la transmission se fait par l'intermédiaire du chromosome X, soit sous forme dominante, soit sous forme récessive.
Notes et références
[modifier | modifier le code]- La maladie de Charcot-Marie-Tooth sur afm-telethon.fr
- (en) Linda Crabtree, « Charcot-Marie-Tooth Disease as a Disabling Disorder », Canadian Family Physician, vol. 35, , p. 361-367 (ISSN 0008-350X, PMID 21248895, lire en ligne [PDF], consulté le )
- AFM-Téléthon, « Avancées dans la maladie de Charcot-Marie-Tooth », sur www.afm-telethon.fr, (consulté le )
- (en) Thomas D T D Bird, Karen K Stephens, Roberta A R A Pagon, Cynthia R C R Dolan, Margaret P M P Adam (eds.), GeneReviews™, Seattle (WA), University of Washington, Seattle, (PMID 20301548, lire en ligne)
- (en) Thomas D T D Bird, Karen K Stephens, Roberta A R A Pagon, Cynthia R C R Dolan, Margaret P M P Adam (eds.), GeneReviews™, Seattle (WA), University of Washington, Seattle, (PMID 20301711, lire en ligne)
Voir aussi
[modifier | modifier le code]Liens externes
[modifier | modifier le code]- Notice dans un dictionnaire ou une encyclopédie généraliste :
- Ressources relatives à la santé :
- « CMT-France » : Association des malades de la CMT en France.
- « CMT-Québec » : Association des malades de la CMT au Québec.
- « Maladie de Charcot-Marie-Tooth », sur www.afm-france.org
- « Classification des maladies de Charcot-Marie-Tooth », sur Orphanet
- « Neuropathies héréditaires sensitivomotrice de Charcot-Marie-Tooth », sur www.has-sante.fr