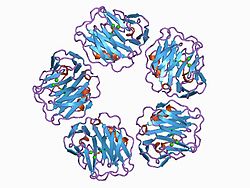
Protéine C réactive
La protéine C réactive (abrégée CRP, de l'anglais C-reactive protein) est une protéine de phase aiguë synthétisée principalement par le foie mais aussi par le tissu adipeux[5]. Elle joue un rôle important dans les réactions inflammatoires, et sert de marqueur biologique à celles-ci.
Historique et nomenclature[modifier | modifier le code]
La protéine C réactive a été isolée par Tilett (en) et Francis en 1930 à Rockefeller University, dans le sérum de patients présentant une inflammation aiguë[6].
Cette protéine réagissait au polysaccharide C du pneumocoque.
Description et rôle[modifier | modifier le code]
La CRP est une protéine constituée de cinq sous-unités comportant chacune 206 acides aminés[7]. Elle fait partie de la famille des pentraxines. Elle joue un rôle dans le système immunitaire, pouvant se fixer sur les immunoglobulines G et pouvant activer le système du complément. Sa demi-vie est de 18 h et elle se trouve essentiellement dans le sérum sanguin[8].
La CRP est un marqueur précoce, sensible et spécifique de la réaction inflammatoire, et proportionnel à son intensité.
Elle apparaît dans les six heures suivant l'inflammation aiguë. Son taux augmente et est maximal après deux jours. Il peut baisser en moins de 6 heures après éradication de la source d'inflammation.
En présence de calcium, la CRP se lie spécifiquement aux résidus phosphocholine. On trouve la phosphocholine dans les polysaccharides microbiens.
Sa forme monomérique, par dissociation du pentamère par les plaquettes sanguines à l'aide du lysophosphatidylcholine (après activation par la phospholipase A2[9]) et des liposomes[10], se dépose dans les plaques d'athérome et aurait un effet pro-inflammatoire[11].
La CRP active par ce biais la voie classique du complément en l'absence d'anticorps, et opsonise les ligands, en vue de leur phagocytose.
La phosphocholine étant également présente dans le PAF (facteur d'activation plaquettaire) et les polynucléaires, la CRP atténue la voie de la coagulation et l'activation des cellules inflammatoires.
Le gène responsable de sa synthèse est situé sur le chromosome 1 humain (long bras proximal)[12]. Ce gène a de nombreuses mutations décrites, pouvant être responsables en partie de la variation inter-individuelle de sa concentration basale[13]. Il existe, par ailleurs, 18 autres gènes, dont les mutations entraînent une modification du taux de CRP[14].
Dosage[modifier | modifier le code]
La concentration sanguine de CRP est normalement inférieure à 6 mg/l. Elle varie cependant selon l'ethnicité, sa valeur étant sensiblement plus basse chez les Asiatiques[15].
Marqueur inflammatoire[modifier | modifier le code]
La CRP est considérée comme bon marqueur biologique de l'inflammation. Au-delà de 5 mg/l (détection par une méthode analytique classique), elle peut indiquer une infection comme une pyélonéphrite, une maladie autoinflammatoire comme une polyarthrite rhumatoïde, ou une maladie néoplasique comme un cancer du poumon.
Elle est utilisée depuis 1977 dans le diagnostic et la surveillance de l'évolution des infections, la normalisation de son taux étant un indice que le phénomène infectieux est maîtrisé. La CRP joue un rôle important dans le myélome multiple : son augmentation est un marqueur important de prolifération tumorale.
Marqueur cardiovasculaire[modifier | modifier le code]
L'élévation de la CRP est un facteur de risque de l'athérome, maladie obstruant les vaisseaux[16]. D'après certains auteurs, quand son taux (à mesurer par méthodes « ultrasensibles » permettant de détecter des taux de 0,2 à 5 mg/l) augmente et dépasse 3 mg/l dans le plasma sanguin[17], elle serait l'un des marqueurs les plus fiables[18] tandis que pour d'autres la corrélation semble faible[19]. Des arguments indirects semblent montrer que cette élévation n'est qu'un marqueur et n'interviendrait pas directement dans la genèse de l'athérome[20]. Selon d'autres études, en revanche, la CRP réduirait la synthèse d'oxyde nitrique et empêcherait l'angiogenèse, jouant ainsi un rôle direct dans les maladies cardiovasculaires[21]. Il a aussi été montré qu'un taux de CRP inférieur à 2 mg/l sous statine diminue le risque d'infarctus du myocarde et de morts par accident coronarien[22].
Marqueur métabolique[modifier | modifier le code]
Le taux de CRP peut être discrètement augmenté en cas d'obésité et cette élévation semble être un marqueur de risque de la survenue d'un diabète de type 2[23].
Interactions[modifier | modifier le code]
La supplémentation en vitamine C peut réduire de manière significative le taux de CRP, voire l'annuler[24],[25].
Notes et références[modifier | modifier le code]
- GRCh38: Ensembl release 89: ENSG00000132693 - Ensembl, May 2017
- GRCm38: Ensembl release 89: ENSMUSG00000037942 - Ensembl, May 2017
- « Publications PubMed pour l'Homme », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- « Publications PubMed pour la Souris », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- Noriyuki Ouchi, Shinji Kihara, Tohru Funahashi, Tadashi Nakamura, Makoto Nishida, Masahiro Kumada, Yoshihisa Okamoto, Koji Ohashi, Hiroyuki Nagaretani, Ken Kishida, Hitoshi Nishizawa, Norikazu Maeda, Hideki Kobayashi, Hisatoyo Hiraoka, and Yuji Matsuzawa Reciprocal Association of C-Reactive Protein With Adiponectin in Blood Stream and Adipose Tissue Circulation. 2003;107:671-674
- Tillett W, Francis T, Serological reactions in pneumonia with non-protein somatic fraction of pneumococcus, J Exp Med, 1930;52:561–571
- Volanakis JE, Human C-reactive protein: expression, structure, and function, Mol Immunol, 2001;38:189–197
- Vigushin DM, Pepys MB, Hawkins PN, Metabolic and scintigraphic studies of radioiodinated human C-reactive protein in health and disease, J Clin Invest, 1993;91:1351–1357
- Thiele JR, Habersberger J, Braig D et al. Dissociation of pentameric to monomeric C-Reactive Protein localizes and aggravates inflammation: In vivo proof of a powerful proinflammatory mechanism and a new anti-inflammatory strategy, Circulation, 2014;130:35-50
- Ji SR, Wu Y, Zhu L, Potempa LA, Sheng FL, Lu W, Zhao J, Cell membranes and liposomes dissociate C-reactive protein (CRP) to form a new, biologically active structural intermediate: mCRP(m), FASEB J, 2007;21:284–294
- Eisenhardt SU, Habersberger J, Murphy A et al. Dissociation of pentameric to monomeric C-reactive protein on activated platelets localizes inflammation to atherosclerotic plaques, Circ Res, 2009;105:128–137
- Whitehead AS, Bruns GA, Markham AF et Als. Isolation of human C-reactive protein complementary DNA and localization of the gene to chromosome 1, Science, 1983;221:69–71
- Pankow JS, Folsom AR, Cushman M et als. Familial and genetic determinants of systemic markers of inflammation: the NHLBI family heart study, Atherosclerosis, 2001;154:681–689
- Dehghan A, Dupuis J, Barbalic M, Meta-analysis of genome-wide association studies in >80 000 subjects identifies multiple loci for C-Reactive Protein levels, Circulation, 2011;123:731-738
- Kelley-Hedgepeth A, Lloyd-Jones DM, Colvin A et als. SWAN Investigators, Ethnic differences in C-reactive protein concentrations, Clin Chem, 2008;54:1027–1037
- Pierre Allain (2005) Protéine C réactive ou CRP et accidents cardiovasculaires, Pharmacorama, 2005-01-23
- Jennifer K. Pai, M.H.S., Tobias Pischon, M.D., M.P.H., Jing Ma, M.D., Ph.D., JoAnn E. Manson, M.D., Dr.P.H., Susan E. Hankinson, Sc.D., Kaumudi Joshipura, B.D.S., Sc.D., Gary C. Curhan, M.D., Sc.D., Nader Rifai, Ph.D., Carolyn C. Cannuscio, Sc.D., Meir J. Stampfer, M.D., Dr.P.H., and Eric B. Rimm, Sc.D. (2004) Inflammatory Markers and the Risk of Coronary Heart Disease in Men and Women, N Engl J Med ; 351:2599-2610December 16, DOI: 10.1056/NEJMoa040967
- Paul M. Ridker, Nader Rifai: C-Reactive Protein and Cardiovascular Disease MediEdition Inc. (27 février 2006) (ISBN 0978009002)
- Assessment of C-Reactive Protein in Risk Prediction for Cardiovascular Disease, D Lloyd-Jones, K Liu, L Tian, P Greenland, Ann Intern Med. 2006;145:35-42
- Zacho J, Tybjærg-Hansen A, Skov Jensen J, Grande P, Sillesen H, Nordestgaard BG, Genetically elevated C-Reactive Protein and ischemic vascular disease, New Eng J Med, 2008;359:1897-1908
- Verma, Subodh MD, PhD; Wang, Chao-Hung MD; Li, Shu-Hong MSc; Dumont, Aaron S. MD; Fedak, Paul W.M. MD; Badiwala, Mitesh V. BSc; Dhillon, Bikramjit BSc; Weisel, Richard D. MD; Li, Ren-Ke MD, PhD; Mickle, Donald A.G. MD; Stewart, Duncan J. MD. A Self-Fulfilling Prophecy C-Reactive Protein Attenuates Nitric Oxide Production and Inhibits Angiogenesis, Circulation, 2002;106:913-919
- Paul M Ridker, M.D., Christopher P. Cannon, M.D., David Morrow, M.D., Nader Rifai, Ph.D., Lynda M. Rose, M.S., Carolyn H. McCabe, B.S., Marc A. Pfeffer, M.D., Ph.D., and Eugene Braunwald, M.D. (2005) [C-Reactive Protein Levels and Outcomes after Statin Therapy] ; for the Pravastatin or Atorvastatin Evaluation and Infection Therapy–Thrombolysis in Myocardial Infarction 22 (PROVE IT–TIMI 22) Investigators ; N Engl J Med 2005; 352:20-28January 6, 2005DOI: 10.1056/NEJMoa042378 (résumé)
- Pradhan AD, Manson JE, Rifai N et Als. C-reactive protein, interleukin 6, and risk of developing type 2 diabetes mellitus, JAMA, 2001;286:327–334
- Gladys Block, Christopher D. Jensen, Tapashi B. Dalvi et Edward P. Norkus, « Vitamin C treatment reduces elevated C-reactive protein », Free radical biology & medicine, vol. 46, no 1, , p. 70–77 (ISSN 0891-5849, PMID 18952164, PMCID PMC2631578, DOI 10.1016/j.freeradbiomed.2008.09.030, lire en ligne, consulté le )
- Vajihe Biniaz, Mehdi Sadeghi Shermeh, Abbas Ebadi et Ali Tayebi, « Effect of Vitamin C Supplementation on C-reactive Protein Levels in Patients Undergoing Hemodialysis: A Randomized, Double Blind, Placebo-Controlled Study », Nephro-urology Monthly, vol. 6, no 1, (ISSN 2251-7006, PMID 24719806, PMCID PMC3968960, DOI 10.5812/numonthly.13351, lire en ligne, consulté le )
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
- Syndrome inflammatoire | inflammation | infection
- Vitesse de sédimentation
- Immunologie
- Procalcitonine
Lien externe[modifier | modifier le code]