Ipilimumab
| Ipilimumab | |
| |
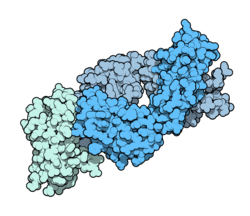
| Fab fragment (en) d'ipilimumab (en bleu) et de CTLA-4 (en vert). Entrée 5TRU de la Protein Data Bank. | |
| Identification | |
|---|---|
| No CAS | |
| Code ATC | |
| DrugBank | DB06186 |
| Propriétés chimiques | |
| Formule | C6742H9972N1732O2004S40 |
| Masse molaire[1] | 148 632,319 ± 7,239 g/mol C 54,48 %, H 6,76 %, N 16,32 %, O 21,57 %, S 0,86 %, |
| Considérations thérapeutiques | |
| Classe thérapeutique | anticorps monoclonal pour immunothérapie |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'ipilimumab (commercialisé sous le nom de Yervoy) est un anticorps monoclonal utilisé dans le traitement du mélanome. C'est un anticorps inhibiteur du point de contrôle CTLA-4 des lymphocytes T, point de contrôle qu’activent certains cancers pour diminuer l'efficacité du lymphocyte.
L'ipilimumab est un anticorps monoclonal humain de type IgG1 dirigé contre la protéine CTLA-4 (Cytotoxic T-Lymphocyte Antigen 4). L'inhibition de ce récepteur présent sur les lymphocytes T a pour conséquence l'activation du lymphocyte T.
Historique de découverte[modifier | modifier le code]
En 1987, des chercheurs français découvrent la protéine CTLA-4 présente à la surface des lymphocytes T. James Allison chercheur au Sloan Kettering à New york a ensuite poussé le développement d'anticorps anti-CTLA-4. La société Medarex rachetée par la suite par le laboratoire américain Bristol Myers Squibb ont poursuivi le développement de l'ipilimumab[2].
Indications, posologies et modalités d'administration[modifier | modifier le code]
Le traitement d’induction se fait à la dose de 3 mg/kg en perfusion intraveineuse sur une période de 90 minutes, toutes les 3 semaines pour un total de 4 doses[3].
Effets secondaires[modifier | modifier le code]
Ils peuvent être de mécanisme immunologique, l'activation des lymphocytes pouvant être dirigée contre des auto-antigènes[4]. ils sont essentiellement à type de rash et de colite. D'autres atteintes sont plus rares : hypophysite, pancréatite, hépatite[5]. Des cas de myocardites fulminantes ont été décrits[6].
Une colite est ainsi vue dans un cas sur cinq, répondant habituellement bien aux corticoïdes[7] ou à l'infliximab[8] mais pouvant se compliquer d'une perforation intestinale[9]. L'aspect en coloscopie est variable[10] mais certains signes permettent de la distinguer d'une rectocolite hémorragique : moindre concentration en lymphocytes de type CD20, moindre plasmocytose, moindre distorsion des cryptes[11].
Efficacité[modifier | modifier le code]
Il améliore la survie des patients atteints de mélanomes métastatiques utilisé seul[12] ou en combinaison avec la dacarbazine[13]. Son efficacité semble être corrélé avec un taux plus élevé de lymphocytes, après traitement[14].
Dans le mélanome, l'efficacité est d'autant plus importante si le traitement est associé avec du nivolumab[15]. Associé avec ce dernier, il est plus efficace que le sunitinib dans le cancer du rein évolué[16].
Renseignements administratifs[modifier | modifier le code]
Autorisation temporaire d'utilisation (ATU)[modifier | modifier le code]
Une ATU nominative a été octroyée à partir du [17].
Une ATU de cohorte a été octroyée à partir du .
Autorisation de mise sur le marché (AMM)[modifier | modifier le code]
Une AMM centralisée a été octroyée le .
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Jerome Groopman, « The T-Cell Army », The New Yorker, (ISSN 0028-792X, lire en ligne, consulté le )
- http://www.bmsfrance.fr/nos-medicaments/Documents/YERVOY/AT_Yervoy_06-11-2013.pdf
- Michot JM, Bigenwald C, Champiat S et al. Immune‐related adverse events with immune checkpoint blockade: a comprehensive review, Eur J Cancer, 2016;54:139–48
- Weber JS, Kähler KC, Hauschild A, Management of immune‐related adverse events and kinetics of response with ipilimumab, J Clin Oncol, 2012;30:2691–7
- Johnson DB, Balko JM, Compton ML et al. Fulminant myocarditis with combination immune checkpoint blockade, N Engl J Med, 2016;375:1749–55
- Beck KE, Blansfield JA, Tran KQ et al. Enterocolitis in patients with cancer after antibody blockade of cytotoxic T‐lymphocyte‐associated antigen 4, J Clin Oncol, 2006;24:2283–9
- Minor DR, Chin K, Kashani‐Sabet M, Infliximab in the treatment of anti‐CTLA4 antibody (ipilimumab) induced immune‐related colitis, Cancer Biother Radiopharm, 2009;24:321–5
- Mitchell KA, Kluger H, Sznol M, Hartman DJ, Ipilimumab‐induced perforating colitis, J Clin Gastroenterol, 2013;47:781–5
- Verschuren EC, van den Eertwegh AJ, Wonders J et al. Clinical, endoscopic, and histologic characteristics of ipilimumab‐associated colitis, Clin Gastroenterol Hepatol, 2016;14:836–42
- Adler BL, Pezhouh MK, Kim A et al. Histopathological and immunophenotypic features of ipilimumab‐associated colitis compared to ulcerative colitis, J Int Med, 2018;283:568-577
- Hodi FS, O'Day SJ, McDermott DF et al. Improved survival with ipilimumab in patients with metastatic melanoma, N Engl J Med, 2010;363:711-723
- Robert C, Thomas L, Bondarenko I et al. Ipilimumab plus dacarbazine for previously untreated metastatic melanoma, N Engl J Med, 2011;364:2517-2526
- Ku GY, Yuan J, Page DB et al. Single-institution experience with ipilimumab in advanced melanoma patients in the compassionate use setting: lymphocyte count after 2 doses correlates with survival, Cancer, 2010;116:1767-1775
- Wolchok JD, Kluger H, Callahan MK et al. Nivolumab plus Ipilimumab in advanced melanoma, N Engl J Med, 2013;369:122-133
- Motzer RJ, Tannir NM, McDermott DF et al. Nivolumab plus ipilimumab versus sunitinib in advanced renal-cell carcinoma, N Engl J Med, 2018;378:1277-1290
- http://www.has-sante.fr/portail/upload/docs/application/pdf/2012-01/yervoy_14_12_2011_avis_ct_11462.pdf
