Cofacteur à molybdène
| Cofacteur à molybdène | |
 Structure du cofacteur à molybdène à base de molybdoptérine |
|
| Identification | |
|---|---|
| No CAS | |
| PubChem | 25202532 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C10H12MoN5O8PS2 [Isomères] |
| Masse molaire[1] | 521,29 ± 0,04 g/mol C 23,04 %, H 2,32 %, Mo 18,41 %, N 13,43 %, O 24,55 %, P 5,94 %, S 12,3 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Un cofacteur à molybdène, parfois abrégé en MoCo, est un cofacteur nécessaire à l'activité de certaines enzymes telles que la xanthine oxydase, la DMSO réductase, la sulfite oxydase, la nitrate réductase, l'éthylbenzène hydroxylase, la glycéraldéhyde-3-phosphate déshydrogénase à ferrédoxine et l'arséniate réductase à glutarédoxine[2],[3]. Chimiquement, de tels cofacteurs résultent de la formation d'un complexe entre un oxyde de molybdène et une molécule de molybdoptérine, ou un dérivé — parfois assez éloigné — de molybdoptérine.
Les nitrogénases, phylogénétiquement plus anciennes, sont les seules enzymes connues utilisant le molybdène mais sans molybdoptérine — elles utilisent à la place des centres fer-soufre, de structure très différente dans laquelle le molybdène est lié à d'autres atomes métalliques ; elles permettent à certaines bactéries et cyanobactéries de fixer l'azote atmosphérique.
Ce type de cofacteurs peut revêtir diverses formes actives chez les procaryotes, tel que le bis(molybdoptérine guanine dinucléotide)molybdène ci-dessous :
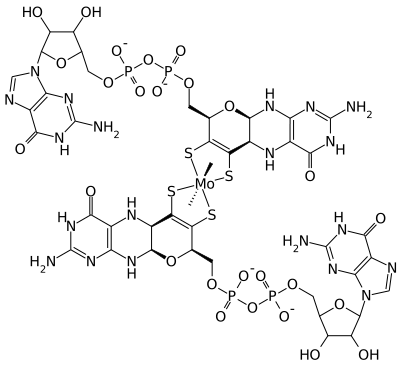
Structure du bis(molybdoptérine guanine dinucléotide)molybdène bactérien[4].
Le cofacteur à molybdène utilisé par la sulfite oxydase a encore une structure différente :

Structure du MoCo de la sulfite oxydase, avec un résidu cystéine lié à l'atome de molybdène[4].
En médecine
[modifier | modifier le code]Le déficit en cofacteur à molybdène est une maladie rare se caractérisant par la survenue de crises convulsives peu après la naissance.
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) G. Schwarz, « Molybdenum cofactor biosynthesis and deficiency », Cell. Mol. Life Sci., vol. 62, no 23, , p. 2792-2810 (PMID 16261263, DOI 10.1007/s00018-005-5269-y)
- (en) B. Smolinsky, S. A. Eichler, S. Buchmeier, J. C. Meier, G. Schwarz, « Splice-specific functions of gephyrin in molybdenum cofactor biosynthesis », J. Biol. Chem., vol. 283, no 25, , p. 17370–9 (PMID 18411266, DOI 10.1074/jbc.M800985200)
- (en) G. Schwarz, R. R. Mendel, M. W. Ribbe, « Molybdenum cofactors, enzymes and pathways », Nature, août 2009, 460 (7257) 839-847. DOI 10.1038/nature08302.


