Flavine adénine dinucléotide
| Flavine adénine dinucléotide | |
| |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.005.149 |
| No CE | 205-663-1 |
| DrugBank | DB03147 |
| PubChem | 703 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C27H33N9O15P2 [Isomères] |
| Masse molaire[1] | 785,549 7 ± 0,030 2 g/mol C 41,28 %, H 4,23 %, N 16,05 %, O 30,55 %, P 7,89 %, |
| Écotoxicologie | |
| DL50 | > 7 g·kg-1 (souris, oral)[2] 589 mg·kg-1(souris, i.v.)[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La flavine adénine dinucléotide (FAD) est une coenzyme d'oxydo-réduction dérivant de la riboflavine (vitamine B2). Il est associé aux enzymes de la classe des oxydo-réductases auxquelles il est lié par une liaison covalente : c'est un groupement prosthétique.
Ce coenzyme est notamment utilisé par les flavoprotéines du complexe II de la chaîne respiratoire mitochondriale : glycérol 3-P déshydrogénase, acylCoA déshydrogénase, succinate déshydrogénase. Au niveau de cette chaine respiratoire mitochondriale, le FAD permet la formation de 2ATP grâce au pompage de 6 protons dans l'espace inter-membranaire.
Le couple rédox est le suivant :
Le FAD intervient également dans la β-oxydation des acides gras lors de l'oxydation de l'acylCoA en TransΔ2-3 énoylCoA via l'acylCoA déshydrogénase. Cette réaction est essentielle à la progression de la β-oxydation mais peut être shunté dans certains cas : acide gras insaturé avec une double liaison sur un carbone impaire de type (Δ5, Δ9 ...).
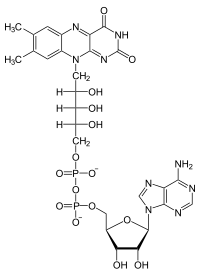
Structure-
Flavine - Ribitol - Phosphate - Phosphate - Ribose - Adénine
NB : Noyau Flavine (dérive de l'isoalloxazine)
Ribitol (ose linéaire en C5)
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Drugs in Japan Vol. -, Pg. 1124, 1995.

