Réarrangement sigmatropique 2,3
Un réarrangement sigmatropique 2,3 est un type de réarrangement sigmatropique, que l'on peut différencier en deux sous-types[1] :
- les réarrangements de sulfoxydes allyliques, d'oxydes d'amine et de sélénoxydes sont neutres ;
- les réarrangements de carbanions d'éthers d'allyle sont anioniques.
Le schéma général de ce genre de réarrangement est le suivant :

L'atome Y peut être un atome de soufre, de sélénium, d'oxygène ou d'azote. Si Y est un azote, la réaction est appelée réarrangement de Sommelet-Hauser ; si Y est un oxygène, elle est appelée réarrangement de Wittig 2,3 (qui ne doit pas être confondue avec la célèbre réaction de Wittig, qui implique un ylure de phosphonium). Si Y est un soufre, le produit peut être traité avec un thiophile pour produire un alcool allylique, la réaction globale étant connue sous le nom de réarrangement de Mislow-Evans.

Un réarrangement [2,3] peut résulter en la formation d'une liaison carbone-carbone. Il peut aussi être utilisé comme réaction d'expansion de cycle[2] :

Stéréosélectivité[modifier | modifier le code]
Les réarrangements sigmatropiques 2,3 peuvent offrir une haute stéréosélectivité. Lors de la formation de la nouvelle liaison double, il y a une forte préférence a former l'alcène E ou isomère trans. La stéréochimie de la nouvelle liaison C-C est quant à elle difficile à prédire. Elle peut être déduite du cycle à cinq de l'état de transition. Généralement, l'alcène E favorisera la formation du produit anti, alors que l'alcène Z favorisera celle du produit syn.
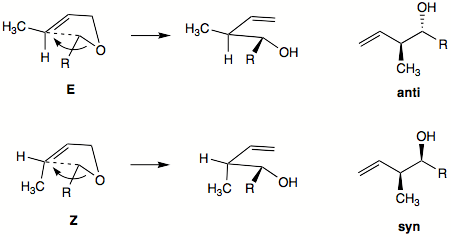
La diastéréosélectivité peut être forte pour l'alcène Z en présence d'un groupe alcynyle, alcényle ou aryle stabilisateur d'anion. La diastéréosélectivité en général moindre avec les alcènes Z. Les groupes hydrocarbures préfèreront en général une orientation exo dans l'état de transition de type « enveloppe ». Les groupes stabilisateurs d'anion préféreront eux une orientation endo pour l'état de transition.
Notes et références[modifier | modifier le code]
- March, Jerry, Advanced Organic Chemistry : Reactions, Mechanisms, and Structure, New York, Wiley, , 3e éd. (ISBN 0-471-85472-7).
- Ring expansion by 2,3-sigmatropic shifts of unstabilized sulfonium ylides. Synthesis of eight- to ten-membered thiacycloalk-4-enes V. Cere, C. Paolucci, S. Pollicino, E. Sandri, and A. Fava The Journal of Organic Chemistry 1978 43 (25), 4826-4831 DOI 10.1021/jo00419a024
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « 2,3-sigmatropic rearrangement » (voir la liste des auteurs).
