RAD51
| Recombinase RAD51 | ||
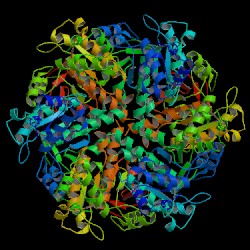 Structure d'un filament RAD51 de Saccharomyces cerevisiae (PDB 1SZP) | ||
| Caractéristiques générales | ||
|---|---|---|
| Nom approuvé | Recombinase RAD51 | |
| Symbole | RAD51 | |
| Synonymes | HRAD51, MRMV2, HsT16930, BRCC5, RECA, HsRad51, FANCR, RAD51A | |
| Homo sapiens | ||
| Locus | 15q15 | |
| Masse moléculaire | 36 966 Da[1] | |
| Nombre de résidus | 339 acides aminés[1] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
La recombinase RAD51 fait partie de la famille des protéines RAD51. Chez les eucaryotes, elle est codée par le gène RAD51 qui, chez l'humain, se trouve sur le chromosome 15. Elle participe à la réparation de l'ADN, et plus particulièrement des lésions doubles brins. La famille RAD51 est homologue des protéines RecA chez les bactéries, RadA chez les archées et Rad51 chez les levures[2]. Cette protéines est hautement conservée chez la plupart des eucaryotes, depuis les levures jusqu'aux humains[3].
Il existe de deux produits de transcription de ce gène distincts, résultant d'un mécanisme d'épissage alternatif, tandis que des variantes supplémentaires résultent par ailleurs d'une polyadénylation alternative.
Sept gènes apparentés au gène recA ont été recensés chez les mammifères : Rad51, Rad51L1/B, Rad51L2/C, Rad51L3/D, XRCC2, XRCC3 et DMC1/Lim15[4]. Hormis la DMC1, spécifique à la méiose, toutes ces protéines sont indispensables au développement des mammifères.
Chez l'humain, la protéine RAD51 compte 339 résidus d'acides aminés et joue un rôle essentiel dans la recombinaison homologue lors de la réparation de l'ADN à la suite de lésions doubles brins. Au cours de ce processus, des brins d'ADN sont échangés moyennant l'hydrolyse de molécules d'ATP, et la protéine RAD51 intervient dans la recherche d'homologie entre ces brins, et leur appariement par complémentarité.
Contrairement aux autres protéines qui interagissent avec l'ADN, celles de la famille Rec1/Rad51 forment un filament hélicoïdal de nucléoprotéine sur l'ADN[5].
La protéine RAD51 peut interagir avec la RPA, la BRCA2, la PALB2[6] et la RAD52 (en).
En médecine[modifier | modifier le code]
Une mutation du gène est impliquée dans le syndrome des mouvements en miroir familiaux congénitaux[7].
Notes et références[modifier | modifier le code]
- Les valeurs de la masse et du nombre de résidus indiquées ici sont celles du précurseur protéique issu de la traduction du gène, avant modifications post-traductionnelles, et peuvent différer significativement des valeurs correspondantes pour la protéine fonctionnelle.
- (en) Akira Shinohara, Hideyuki Ogawa et Tomoko Ogawa, « Rad51 protein involved in repair and recombination in S. cerevisiae is a RecA-like protein », Cell, vol. 69, no 3, , p. 457-470 (PMID 1581961, DOI 10.1016/0092-8674(92)90447-K, lire en ligne)
- (en) Akira Shinohara, Hideyuki Ogawa, Yoichi Matsuda, Noriko Ushio, Kazuho Ikeo et Tomoko Ogawa, « Cloning of human, mouse and fission yeast recombination genes homologous to RAD51 and recA », Nature Genetics, vol. 4, no 3, , p. 239-243 (PMID 8358431, DOI 10.1038/ng0793-239, lire en ligne)
- (en) M. Kawabata, T. Kawabata et M. Nishibori, « Role of recA/RAD51 family proteins in mammals », Acta Medica Okayama, vol. 59, no 1, , p. 1-5 (PMID 15902993)
- (en) Vitold E. Galkin, Yan Wu, Xiao-Ping Zhang, Xinguo Qian, Yujiong He, Xiong Yu, Wolf-Dietrich Heyer, Yu Luo et Edward H. Egelman, « The Rad51/RadA N-Terminal Domain Activates Nucleoprotein Filament ATPase Activity », Structure, vol. 14, no 6, , p. 983-992 (PMID 16765891, DOI 10.1016/j.str.2006.04.001, lire en ligne)
- (en) Rémi Buisson, Anne-Marie Dion-Côté, Yan Coulombe, Hélène Launay, Hong Cai, Alicja Z. Stasiak, Andrzej Stasiak, Bing Xia et Jean-Yves Masson, « Cooperation of breast cancer proteins PALB2 and piccolo BRCA2 in stimulating homologous recombination », Nature Structural & Molecula Biology, vol. 17, no 10, , p. 1247-1254 (PMID 20871615, DOI 10.1038/nsmb.1915, lire en ligne)
- Ahmed I, Mittal K, Sheikh TI et al. Identification of a homozygous splice site mutation in the dynein axonemal light chain 4 gene on 22q13.1 in a large consanguineous family from Pakistan with congenital mirror movement disorder, Hum Genet, 2014;133:1419–1429
