Hydrure de tris(triphénylphosphine)rhodium carbonyle
| Hydrure de tris(triphényl- phosphine)rhodium carbonyle | |||
| |||
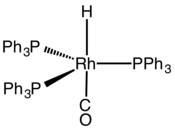
| Structure de l'hydrure de tris(triphénylphosphine)rhodium carbonyle | |||
| Identification | |||
|---|---|---|---|
| No CAS | |||
| No ECHA | 100.037.467 | ||
| No CE | 241-230-3 | ||
| SMILES | |||
| InChI | |||
| Apparence | poudre orange[1] | ||
| Propriétés chimiques | |||
| Formule | C55H46OP3Rh |
||
| Masse molaire[2] | 918,779 9 ± 0,047 5 g/mol C 71,9 %, H 5,05 %, O 1,74 %, P 10,11 %, Rh 11,2 %, |
||
| Propriétés physiques | |||
| T° fusion | 150 °C[1] | ||
| Précautions | |||
| SGH[1] | |||
| H312+H332, P280, P302+P352 et P304+P340 |
|||
| NFPA 704[1] | |||
| Transport[1] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
L’hydrure de tris(triphénylphosphine)rhodium carbonyle est un composé chimique de formule RhH(CO)[P(C6H5)3]3. Il s'agit d'un solide jaune soluble dans le benzène utilisé comme précatalyseur dans l'industrie pour les réactions d'hydroformylation[3]. C'est l'un des rares complexes d'hydrure de rhodium pentacoordonné qui soient stables. Il adopte une géométrie bipyramidale trigonale dans laquelle les ligands carbonyle CO et hydrure H sont en configuration trans, ce qui donne une symétrie pseudo-C3v. Les liaisons Rh–P, Rh–C et Rh–H ont respectivement pour longueurs 232 pm, 183 pm et 160 pm[4],[5].
Synthèse[modifier | modifier le code]
RhH(CO)[P(C6H5)3]3 a été obtenu pour la première fois par réduction de chlorure de bis(triphénylphosphine)rhodium carbonyle trans-[RhCl(CO)(P(C6H5)3)2] par du borohydrure de sodium NaBH4 ou de la triéthylamine N(CH2CH3)3 et de l'hydrogène H2 dans l'éthanol en présence d'un excès de triphénylphosphine P(C6H5)3 :
- RhCl(CO)[P(C6H5)3]2 + NaBH4 + P(C6H5)3 ⟶ RhH(CO)[P(C6H5)3]3 + NaCl + BH3.
Il peut également être produit à partir d'un aldéhyde, de chlorure de rhodium(III) RhCl3 et de triphénylphosphine dans un milieu alcool basique[6].
Application[modifier | modifier le code]
Ce précatalyseur a été découvert en cherchant à utiliser le catalyseur de Wilkinson comme catalyseur d'hydroformylation. On a observé que le complexe tendait à se carbonyler rapidement et que l'activité catalytique de la substance résultante était accrue par divers additifs mais inhibée par les halogénures. Cette inhibition n'était pas observée en présence d'une base, ce qui laissa à penser que l'hydrure était la forme catalytique du complexe[7].
Notes et références[modifier | modifier le code]
- « Fiche du composé Carbonylhydridotris(triphenylphosphine)rhodium(I), Rh 10.0% min », sur Alfa Aesar (consulté le ).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) J. F. Hartwig, Organotransition metal chemistry - from bonding to catalysis, University Science Books, 2009, p. 753, 757-578. (ISBN 978-1-891-38953-5)
- (en) I. S. Babra, L. S. Morley, S. C. Nyburg et A. W. Parkins , « The crystal and molecular structure of a new polymorph of carbonylhydridotris(triphenylphosphine)rhodium(I) having a Rh-H stretching absorption at 2 013 cm−1 », Journal of Crystallographic and Spectroscopic Research, vol. 23, , p. 997-1000 (DOI 10.1007/BF01185550, lire en ligne).
- (en) S. J. La Placa et J. A. Ibers, « Crystal and molecular structure of tritriphenylphosphine rhodium carbonyl hydride », Acta Crystallographica, vol. 18, , p. 511-519 (DOI 10.1107/S0365110X65001093, lire en ligne).
- (en) N. Ahmad, J. J. Levison, S. D. Robinson, M. F. Uttley, E. R. Wonchoba et G. W. Parshall, « Hydrido Phosphine Complexes of Rhodium(I) », Inorganic Syntheses: Reagents for Transition Metal Complex and Organometallic Syntheses, vol. 28, , p. 81-83 (DOI 10.1002/9780470132593.ch19, lire en ligne).
- (en) D. Evans, J. A. Osborn et G. Wilkinson, « Hydroformylation of alkenes by use of rhodium complex catalysts », Journal of the Chemical Society A: Inorganic, Physical, Theoretical, , p. 3133-3142 (DOI 10.1039/j19680003133, lire en ligne).



