Effet mésomère
L'effet mésomère en chimie est un effet électronique de chimie organique lié à la délocalisation des électrons. Il caractérise la propriété d'un substituant ou d'un groupe fonctionnel de céder ou d'accepter un doublet d'électron, permettant la délocalisation de celui-ci, et d'abaisser l'énergie du composé total avec pour effet de le stabiliser. Cet effet est utilisé de façon qualitative pour décrire le rôle de ce substituant dans la structure résonante, et symbolisé par la lettre M.
Effet +M[modifier | modifier le code]

Un substituant porteur d'un doublet non liant peut le céder pour former des formes mésomères. Un tel substituant qui peut céder un doublet et augmenter la densité d'électrons dans les formes mésomères possède un effet mésomère donneur et est noté +M. Un groupe +M favorise les réactions de substitution nucléophile en stabilisant le cation formé par le départ d'un nucléofuge. Lors d'une substitution électrophile aromatique, un substituant +M est un groupe orienteur ortho/para.
Substituant à effet +M[modifier | modifier le code]
Effet −M[modifier | modifier le code]
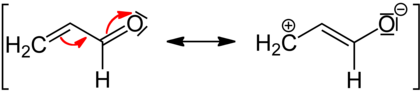
Un substituant capable d'attirer et de porter un doublet non liant et ainsi diminuer la densité d'électrons dans les formes mésomères possède un effet mésomère attracteur, noté −M. Cet effet a tendance à rendre les réactions de substitutions plus compliquées, en augmentant l'énergie d'activation. Un effet -M est donc désactivant d'un point de vue cinétique. Lors d'une substitution électrophile aromatique, un substituant -M est un groupe orienteur méta.
Substituant à effet -M[modifier | modifier le code]
Acidité[modifier | modifier le code]
Un substituant à effet -M augmente l'acidité car il augmente la stabilité de l'anion issu du départ d'un ion H+. C'est particulièrement le cas dans les composés aromatiques, les nitrophénols étant par exemple bien plus acides que le phénol :
- le phénol a un pKA de 9,99 ;
- les (mono)nitrophénols ont un pKA variant de 7,16 à 8,28 selon l'isomère ;
- les dinitrophénols ont un pKA compris entre 3,71 et 5 ;
- l'un des trinitrophénols, l'acide picrique a un pKA de 0,29.
Notes et références[modifier | modifier le code]
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Mesomerer Effekt » (voir la liste des auteurs).
