« Vératrole » : différence entre les versions
Aucun résumé des modifications |
+ |
||
| Ligne 152 : | Ligne 152 : | ||
| supplement = |
| supplement = |
||
}}<!-- ----------------------------- Fin de l'infoboîte ----------------------------- --> |
}}<!-- ----------------------------- Fin de l'infoboîte ----------------------------- --> |
||
Le '''vératrole''', ou '''1,2-diméthoxybenzène''', est un [[composé aromatique]] de [[formule chimique]] {{fchim|C|6|H|4|(OCH|3|)|2}}. Cet [[Éther-oxyde|éther]] [[Méthyle|diméthylique]] est l'un de trois isomères du [[diméthoxybenzène]], le composé ''ortho''. Il se présente sous la forme d'un liquide incolore à l'odeur agréable, faiblement soluble dans l'eau mais très soluble dans les [[Solvant organique|solvants organiques]]. |
Le '''vératrole''', ou '''1,2-diméthoxybenzène''', est un [[composé aromatique]] de [[formule chimique]] {{fchim|C|6|H|4|(OCH|3|)|2}}. Cet [[Éther-oxyde|éther]] [[Méthyle|diméthylique]] est l'un de trois isomères du [[diméthoxybenzène]], le composé ''ortho''. Il se présente sous la forme d'un liquide incolore à l'odeur agréable, faiblement soluble dans l'eau mais très soluble dans les [[Solvant organique|solvants organiques]]. |
||
== Occurrence == |
|||
Le vératrole est présent dans la nature. Il est notamment biosynthétisé par méthylation du [[gaïacol]] par la [[gaïacol O-méthyltransferase]]<ref name="ReferenceA">{{cite journal | doi = 10.1186/1471-2229-12-158| pmid = 22937972| pmc = 3492160| title = Identification of white campion (Silene latifolia) guaiacol O-methyltransferase involved in the biosynthesis of veratrole, a key volatile for pollinator attraction| journal = BMC Plant Biology| volume = 12| pages = 158| year = 2012| last1 = Gupta| first1 = Alok K| last2 = Akhtar| first2 = Tariq A| last3 = Widmer| first3 = Alex| last4 = Pichersky| first4 = Eran| last5 = Schiestl| first5 = Florian P}}</ref>. Le gène de la gaïacol O-méthyltransferase est par ailleurs le premier gène de parfum jamais découvert dans une plante<ref name="ReferenceA"/>. Le vératrole est un attracteur à insectes<ref name="ReferenceA"/>. |
|||
== Synthèse == |
|||
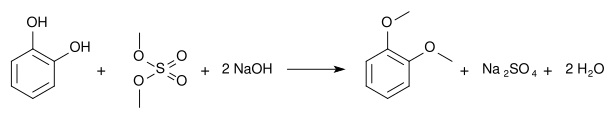
Le vératrole peut être obtenu en traitant du [[pyrocatéchol]] avec du [[sulfate de diméthyle]] {{fchim|(CH|3|)|2|SO|4}} : |
|||
:[[Fichier:Synthesis Veratrol.svg|Synthèse du vératrole.]] |
:[[Fichier:Synthesis Veratrol.svg|Synthèse du vératrole.]] |
||
| Ligne 158 : | Ligne 166 : | ||
Il peut également être obtenu par décomposition thermique de l'[[acide vératrique]] {{fchim|HOOCC|6|H|3|(OCH|3|)|2}}. |
Il peut également être obtenu par décomposition thermique de l'[[acide vératrique]] {{fchim|HOOCC|6|H|3|(OCH|3|)|2}}. |
||
== |
== Utilisations == |
||
C'est un [[Précurseur (chimie)|précurseur]] utilisé dans la [[synthèse organique]] d'autres composés aromatiques. Relativement riche en [[électron]]s, il peut facilement subir une [[substitution électrophile]]<ref>{{OrgSynth | title = 4-Iodoveratrole | author = Janssen, D. E. | author2 = Wilson, C. V. | collvol = 4 | collvolpages = 547 | year = 1963 | prep = CV4P0547}}</ref>. Il peut par exemple servir ä synthétiser la [[3,4-Diméthoxyacetophénone|3,4-diméthoxyacetophénone]] par [[acylation de Friedel-Crafts]]<ref name="ORGANIKUM_19_341">''[[Organikum]]'', 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, p. 341.</ref> ou est utilisé dans la synthèse de la [[domipizone]]<ref>{{Cite patent|EP|0129791}}, (1985); CA, 102, 220886 (synth, pharmacol).</ref>. |
|||
Le vératrole peut être facilement bromé par le [[N-Bromosuccinimide|NBS]] pour donner le 4-bromovératrole<ref name="BannardLatremouille1953">{{cite journal|last1=Bannard|first1=R. A. B.|last2=Latremouille|first2=G.|title=4-BROMOVERATROLE|journal=Canadian Journal of Chemistry|volume=31|issue=4|year=1953|pages=469–469|issn=0008-4042|doi=10.1139/v53-062}}</ref>. |
|||
=== Dérivés === |
|||
L'addition d'un autre substituant carboné au vératrole produit une classe de dérivés nommés d'après lui. Le tableau ci-dessous regroupe les plus importants d'entre eux. |
|||
:{| class="wikitable" style="text-align:center; font-size:90%" |
|||
|- |
|||
|bgcolor=#dddddd| ||bgcolor=#dddddd| –CH<sub>2</sub>OH ||bgcolor=#dddddd| –CHO ||bgcolor=#dddddd| –COOH |
|||
|- |
|||
| [[Image:Veratrol.svg|120px]] || [[Image:Veratrylalkohol.svg|120px]] || [[Image:Veratrumaldehyd.svg|125px]] || [[Image:Veratrumsäure.svg|120px|]] |
|||
|- |
|||
| Vératrol || [[Alcool de vératryle|Alcool vératrique]] || [[Vératraldéhyde]] || [[Acide vératrique]] |
|||
|} |
|||
Le vératraldéhyde peut notamment être produit par [[réaction de Vilsmeier-Haack]]<ref name="ORGANIKUM_19_345">''[[Organikum]]'', 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, p. 345.</ref> |
|||
== Notes et références == |
|||
{{Traduction/Référence|lang1=en|art1=1,2-Dimethoxybenzene|id1=891139711|lang2=de|art2=Veratrol|id1=177310799}} |
|||
{{Références}} |
{{Références}} |
||
Version du 11 avril 2019 à 21:34
| Vératrole | |||
 Structure du vératrole |
|||
| Identification | |||
|---|---|---|---|
| Nom UICPA | 1,2-diméthoxybenzène | ||
| Synonymes |
orthodiméthoxybenzène, o-diméthoxybenzène |
||
| No CAS | |||
| No ECHA | 100.001.860 | ||
| No CE | 202-045-3 | ||
| No RTECS | CZ6475000 | ||
| PubChem | 7043 | ||
| ChEBI | 59114 | ||
| SMILES | |||
| InChI | |||
| Propriétés chimiques | |||
| Formule | C8H10O2 [Isomères] |
||
| Masse molaire[1] | 138,163 8 ± 0,007 7 g/mol C 69,54 %, H 7,3 %, O 23,16 %, |
||
| Propriétés physiques | |||
| T° fusion | 15 °C[2] | ||
| T° ébullition | 206 à 207 °C[2] | ||
| Masse volumique | 1,084 g·cm-3[2] à 25 °C | ||
| Point d’éclair | 72 °C[2] | ||
| Précautions | |||
| SGH[2] | |||
| H302 |
|||
| Transport[2] | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Le vératrole, ou 1,2-diméthoxybenzène, est un composé aromatique de formule chimique C6H4(OCH3)2. Cet éther diméthylique est l'un de trois isomères du diméthoxybenzène, le composé ortho. Il se présente sous la forme d'un liquide incolore à l'odeur agréable, faiblement soluble dans l'eau mais très soluble dans les solvants organiques.
Occurrence
Le vératrole est présent dans la nature. Il est notamment biosynthétisé par méthylation du gaïacol par la gaïacol O-méthyltransferase[3]. Le gène de la gaïacol O-méthyltransferase est par ailleurs le premier gène de parfum jamais découvert dans une plante[3]. Le vératrole est un attracteur à insectes[3].
Synthèse
Le vératrole peut être obtenu en traitant du pyrocatéchol avec du sulfate de diméthyle (CH3)2SO4 :
Il peut également être obtenu par décomposition thermique de l'acide vératrique HOOCC6H3(OCH3)2.
Utilisations
C'est un précurseur utilisé dans la synthèse organique d'autres composés aromatiques. Relativement riche en électrons, il peut facilement subir une substitution électrophile[4]. Il peut par exemple servir ä synthétiser la 3,4-diméthoxyacetophénone par acylation de Friedel-Crafts[5] ou est utilisé dans la synthèse de la domipizone[6].
Le vératrole peut être facilement bromé par le NBS pour donner le 4-bromovératrole[7].
Dérivés
L'addition d'un autre substituant carboné au vératrole produit une classe de dérivés nommés d'après lui. Le tableau ci-dessous regroupe les plus importants d'entre eux.
–CH2OH –CHO –COOH 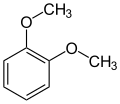


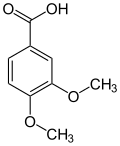
Vératrol Alcool vératrique Vératraldéhyde Acide vératrique
Le vératraldéhyde peut notamment être produit par réaction de Vilsmeier-Haack[8]
Notes et références
- (en)/(de) Cet article est partiellement ou en totalité issu des articles intitulés en anglais « 1,2-Dimethoxybenzene » (voir la liste des auteurs) et en allemand « Veratrol » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé 1,2-Dimethoxybenzene ≥ 99%, consultée le 9 octobre 2013.
- Alok K Gupta, Tariq A Akhtar, Alex Widmer, Eran Pichersky et Florian P Schiestl, « Identification of white campion (Silene latifolia) guaiacol O-methyltransferase involved in the biosynthesis of veratrole, a key volatile for pollinator attraction », BMC Plant Biology, vol. 12, , p. 158 (PMID 22937972, PMCID 3492160, DOI 10.1186/1471-2229-12-158)
- Janssen, D. E., 4-Iodoveratrole, Org. Synth., coll. « vol. 4 », , p. 547
- Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, p. 341.
- EP 0129791, (1985); CA, 102, 220886 (synth, pharmacol).
- R. A. B. Bannard et G. Latremouille, « 4-BROMOVERATROLE », Canadian Journal of Chemistry, vol. 31, no 4, , p. 469–469 (ISSN 0008-4042, DOI 10.1139/v53-062)
- Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, p. 345.