Ruthénocène
| Ruthénocène | |
  |
|
| Identification | |
|---|---|
| Nom UICPA | ruthénocène bis(η5-cyclopentadiényl)ruthénium |
| Synonymes |
Cp2Ru |
| No CAS | |
| No ECHA | 100.013.696 |
| No CE | 215-065-2 |
| PubChem | 11986121 |
| SMILES | |
| InChI | |
| Apparence | solide jaune[1] |
| Propriétés chimiques | |
| Formule | C10H10Ru |
| Masse molaire[2] | 231,26 ± 0,03 g/mol C 51,94 %, H 4,36 %, Ru 43,7 %, |
| Propriétés physiques | |
| T° fusion | 199 à 201 °C[1] |
| Précautions | |
| SGH[1] | |
| H315, H319, H335, P261 et P305+P351+P338 |
|
| NFPA 704[1] | |
| Composés apparentés | |
| Autres composés | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
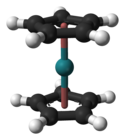
Le ruthénocène ou bis(η5-cyclopentadiényl)ruthénium est un composé organométallique du ruthénium de formule (C5H5)2Ru. Il appartient à la famille des composés sandwich et plus spécifiquement à la sous-famille des métallocènes. Il se présente sous la forme d'un solide jaune volatil.
Structure et liaisons
[modifier | modifier le code]Le ruthénocène consiste en un ion ruthénium pris en sandwich entre deux cycles de cyclopentadiényle. Ce centre métallique se lie de façon symétrique aux deux ligands cyclopentadiényle par des liaisons covalentes haptiques Ru-C de longueur 221–222 pm[3],[4].
Le ruthénocène est isoélectronique avec le ferrocène, et il possède une structure et des propriétés similaires. Les deux composés ont 18 électrons de valence ce qui explique leur grande stabilité. En phase gaz, les cycles de cyclopentadiényle du ruthénocène comme ceux du ferrocène adoptent une conformation éclipsée, mais la barrière de rotation est faible, si bien qu'en solution la rotation est libre et rapide[3]. En phase solide cependant, le ruthénocène conserve cette conformation éclipsée, contrairement au ferrocène qui prend une conformation décalée. Cette différence peut s'expliquer par le rayon ionique plus grand du ruthénium, ce qui accroît la distance entre les cycles de cyclopentadiényle et réduit les interactions stériques, ce qui permet à la conformation éclipsée d'être prévalente.
Propriétés chimiques
[modifier | modifier le code]Contrairement au ferrocène, le ruthénocène s'oxyde par échange de deux électrons, et non d'un seul[5]. Avec un anion non coordinant comme électrolyte, l'oxydation se fait par étape à 1 électron[6].
Synthèse
[modifier | modifier le code]Le ruthénocène fut synthétisé la première fois en 1952 par Geoffrey Wilkinson, qui avait déjà collaboré à l'étude de la structure du ferrocène l'année précédente[7]. Il fut préparé par la réaction entre le trisacétylacétonate de ruthénium avec du bromure de cyclopentadiénylmagnésium en excès[7] :
- Ru(acac)3 + 3 C5H5MgBr → Ru(C5H5)2 + 3 "acacMgBr" + "C5H5"
Le ruthénocène peut aussi être préparé par réaction entre le cyclopentadiénure de sodium avec le « dichlorure de ruthénium » (préparé in situ par réaction entre le ruthénium métallique et le trichlorure de ruthénium)[8] :
Utilisation
[modifier | modifier le code]Le ruthénocène a fait l'objet d'études comme photoinitiateur dans le cadre de réactions de polymérisation[9].
Notes et références
[modifier | modifier le code]- (en)/(de) Cet article est partiellement ou en totalité issu des articles intitulés en anglais « Ruthenocene » (voir la liste des auteurs) et en allemand « Ruthenocen » (voir la liste des auteurs).
- Fiche Sigma-Aldrich du composé Bis(cyclopentadienyl)ruthenium(II), consultée le 18 novembre 2014.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Didier Astruc, Organometallic Chemistry and Catalysis, Springer-Verlag Berlin Heidelberg 2007, , 608 p. (ISBN 978-3-540-46128-9, lire en ligne), p. 252
- Christoph Elschenbroich, Organometallchemie, B. G. Teubner Verlag, , 764 p. (ISBN 978-3-8351-0167-8), p. 452
- Smith, T. P; Taube, H.; Bino, A.; Cohen, S., « Reactivity of Haloruthenocene(IV) complexes », Inorg. Chem., vol. 23, no 13, , p. 1943 (DOI 10.1021/ic00181a030)
- Geiger, W. E. and Barrière, F., "Organometallic Electrochemistry Based on Electrolytes Containing [sic]Coordinating Fluoroarylborate Anions", Accounts of Chemical Research, 2010. DOI 10.1021/ar1000023.
- Wilkinson, G., « The Preparation and Some Properties of Ruthenocene and Ruthenicinium Salts », J. Am. Chem. Soc., vol. 74, no 23, , p. 6146 (DOI 10.1021/ja01143a538).
- Bublitz, D. E; McEwen, W. E.; Kleinberg, J., Ruthenocene, Org. Synth., coll. « vol. 5 », , p. 1001
- Cynthia T. Sanderson, Bentley J. Palmer, Alan Morgan, Michael Murphy, Richard A. Dluhy, Todd Mize, I. Jonathan Amster, and Charles Kutal "Classical Metallocenes as Photoinitiators for the Anionic Polymerization of an Alkyl 2-Cyanoacrylate" Macromolecules 2002, volume 35, p. 9648-9652.DOI 10.1021/ma0212238


