Réactif de Tebbe
| Réactif de Tebbe | ||
| ||
 | ||
| Identification | ||
|---|---|---|
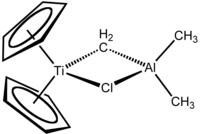
| Nom UICPA | μ-chloro[di(cyclopenta-2,4-dièn-1-yl)]diméthyl(μ-méthylène)titaniumaluminum | |
| No CAS | ||
| No ECHA | 100.157.162 | |
| PubChem | 53384502 | |
| Apparence | liquide rouge (en solution dans du toluène) | |
| Propriétés chimiques | ||
| Formule | C13H18AlClTi [Isomères] |
|
| Masse molaire[1] | 284,584 ± 0,015 g/mol C 54,87 %, H 6,38 %, Al 9,48 %, Cl 12,46 %, Ti 16,82 %, |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Le réactif de Tebbe (nommé en hommage au chimiste Frederick Nye Tebbe, dit Fred Tebbe) est un composé organométallique de formule (η5-C5H5)2Ti(µ-CH2)(µ-Cl)Al(CH3)2. Il est utilisé pour la méthylénation d'esters et de cétones et est préparé à partir de triméthylaluminium[2]. Ce complexe présente deux noyaux métalliques pontés par un radical méthyl ou chlore, l'un de titane et l'autre d'aluminium. Le noyau titane porte deux anions cyclopentadiène, et le noyau aluminium, deux méthyles. Le réactif de Tebbe est une substance de teinte rouge, commercialisée sous forme de solution de toluène, spontanément inflammable, qui doit donc être manipulée en enceinte purgée d'oxygène.
Préparation[modifier | modifier le code]
Le réactif de Tebbe est obtenu par réaction à température ambiante de dichlorure de titanocène (Cp2Cl2Ti) sur du triméthyl-aluminium[3]. On peut obtenir par la même occasion le carbène dit catalyseur de Schrock, servant notamment à la méthylénation, par action d'une base (par exemple de la pyridine).
Mécanisme de réaction[modifier | modifier le code]

Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Cf. F. N. Tebbe, G. W. Parshall et G. S. Reddy, « Olefin homologation with titanium methylene compounds », J. Am. Chem. Soc., vol. 100, no 11, , p. 3611–3613 (DOI 10.1021/ja00479a061).
- Cf. W.A. Herrmann, Advances in Organometallic Chemistry, vol. 20, , p. 195–197.
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Tebbe's reagent » (voir la liste des auteurs).
