Extrasystole ventriculaire
| Extrasystole ventriculaire | |
| Classification et ressources externes | |
| CIM-10 | I49.3 |
|---|---|
| MeSH | D018879 |
| modifier |
|
Une extrasystole ventriculaire (« ESV ») est une contraction prématurée (extrasystole) du ventricule cardiaque et issue de ce dernier. Elle s'oppose ainsi aux extrasystoles atriales.
En terme diagnostique ce qui importe est de savoir si l'extrasystolie ventriculaire présente ou non des signes de gravité pouvant conduire à une tachycardie ventriculaire, avec alors la nécessité d'introduire un traitement antiarythmique. Dans le cas contraire, le plus souvent, elle nécessite une simple surveillance.
Épidémiologie[modifier | modifier le code]
Elles sont très fréquentes, même en l'absence de toute maladie. Pendant le jour, elle est retrouvée dans de 40-100% des patients sains, jusqu'à 40 ans leur nombre dépasse rarement 200/24 h[1].
Clinique[modifier | modifier le code]
Elle peut être totalement asymptomatique et être découverte lors d'un examen systématique ou peut causer des palpitations. Rarement, si le nombre d'extrasystoles ventriculaires est très important, elle peut être responsable d'un tableau d'insuffisance cardiaque.
Tant à l'interrogatoire qu'à l'examen clinique, rien ne peut distinguer une extrasystole atriale d'une extrasystole ventriculaire.
Diagnostic[modifier | modifier le code]
L'électrocardiogramme permet d'en faire le diagnostic si elles sont suffisamment fréquentes pour apparaître dans un enregistrement d'une dizaine de secondes. Si elles sont plus rares, un holter cardiaque (enregistrement de 24 h ou plus) est utile. Il existe cependant une variabilité interjournalière importante du nombre d'extrasystoles ventriculaires [2] pouvant nécessiter des enregistrements plus prolongés ou répétés.
ECG[modifier | modifier le code]
On retrouve un complexe QRS non précédé par (ou sans relation chronologique fixe avec) une onde P. Le complexe QRS est typiquement large (supérieur à 0,12 s.) et déformé par rapport aux complexes QRS de base avec aspect soit de bloc de branche droit s'il s'agit d'une extrasystole ventriculaire naissant du ventricule gauche, soit de bloc de branche gauche s'il s'agit d'une ESV naissant du ventricule droit. La repolarisation est inversée avec une onde T négative.
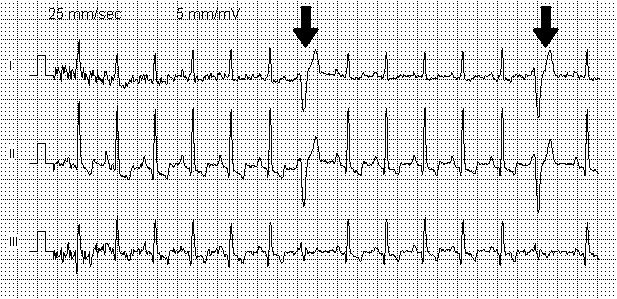
Autres examens[modifier | modifier le code]
Une échocardiographie doit être pratiquée pour rechercher une cause à l'extrasystolie[3]. Un test d'effort permet de voir si cette dernière est augmentée ou au contraire diminue ou disparaît à l'effort. Suivant l'orientation diagnostique, les investigations peuvent être complétées par une IRM cardiaque, une coronarographie.
Éléments pronostiques[modifier | modifier le code]
Le principal risque des ESV est d'induire une arythmie ventriculaire plus sévère qu'il s'agisse d'une tachycardie ventriculaire ou d'une fibrillation ventriculaire avec risque de mort subite. L'extrasystole ventriculaire sera l'élément déclencheur d'une arythmie soutenue.
Il existe plusieurs caractéristiques permettant d'estimer ce risque de complications :
- La morphologie (forme) des ESV : lorsque toutes les extrasystoles ont le même aspect, elles sont dites monomorphes. Lorsqu'elles ont des formes différentes, elles sont dites polymorphes (existence de plusieurs foyers ectopiques) : elles sont alors potentiellement plus graves. De même, un allongement plus important du QRS augmente le risque de survenue d'une cardiomyopathie[4].
- L'intervalle de couplage : le couplage d'une extrasystole par rapport au complexe QRS précédent est dit court lorsque l'ESV survient au sommet de l'onde T précédente (extrasystole précoce ou phénomène R/T). Le risque est alors plus important de survenue d'une tachycardie ventriculaire.
- Le nombre d'ESV par 24 heures ne peut être déterminé que par un holter et n'est pas un critère péjoratif. Une extrasystolie quantitativement très importante peut provoquer, rarement, une insuffisance cardiaque[5]. Toutefois, le nombre d'extrasystoles semble être corrélé avec une augmentation du risque de maladie cardiovasculaire[6].
- Leur rythme :
- on parle de doublet (deux ESV de suite), de triplet (trois ESV de suite) ; au-delà, on parle de salve d'ESV ou de tachycardie ventriculaire non soutenue. Ces phénomènes sont plus péjoratifs que des extrasystoles isolés.
- elles peuvent être bigéminées (une ESV après chaque complexe normal), ou trigéminées (une ESV tous les deux complexes normaux).
- La circonstance de survenue : une apparition préférentielle à l'effort peut être révélatrice d'une maladie coronarienne et est un critère de gravité. Une épreuve d'effort peut être réalisée pour mieux les évaluer.
- Le caractère interpolé : habituellement, une extrasystole est suivie par une brève pause, appelée « repos compensateur » et décalant ainsi légèrement le rythme cardiaque. Dans certains cas, ce repos compensateur n'existe pas et le complexe suivant arrive comme si l'extrasystole n'a pas eu lieu. On parle alors d'« extrasystole interpolée », avec un risque augmenté de révéler ou de se compliquer d'une cardiomyopathie[7].
Électrophysiologistes, médecins et sociétés savantes proposent des scores, par exemple depuis 1971 une classification pronostique par le cardiologue américain Bernard Lown[8].
La gravité de l'extrasystolie dépend aussi de l'existence d'une cardiopathie sous-jacente et surtout par l'altération de la fonction systolique quantifiée par la fraction d'éjection. Une échocardiographie fait donc partie du bilan de toute extrasystolie ventriculaire.
Peuvent donc être considérées comme bénignes les ESV sur cœur sain, monomorphes, de grande amplitude, sans forme répétitive, diminuant ou disparaissant à l'effort.
Doivent être considérées comme potentiellement graves, et justifiant alors un traitement antiarythmique, ainsi que celui de la cause, les ESV très prématurées (ou précoces), répétitives (survenant en doublets, triplets voire salves de tachycardie ventriculaire), polymorphes, avec des QRS très élargis et de faible amplitude, s'aggravant à l'effort, surtout si elles surviennent sur un cœur pathologique.
Traitement[modifier | modifier le code]
La prise en charge des extrasystoles ventriculaires a fait l'objet de la publication de recommandations. Celles de l'« European Society of Cardiology » datent de 2015[9].
Il a pour objectifs d'éviter la mort subite, et accessoirement, d'améliorer la qualité de vie en diminuant la gêne fonctionnelle. Ainsi les ESV bénignes et asymptomatiques ne nécessitent aucun traitement.
Si elles sont considérées comme bénignes mais sont gênantes pour le patient, on peut proposer des règles hygiéno-diététiques (diminution ou suppression des excitants), plus ou moins associées à un traitement sédatif de type anxiolytique. En cas de gêne fonctionnelle importante, on peut proposer l'utilisation de certains antiarythmiques comme les bêta-bloquants mais leur efficacité reste discutée dans cette indication[10]. Dans de rares cas, une ablation par radiofréquence du site d'émergence de l'extrasystole peut être proposée[11].
Le traitement d'une extrasystolie avec critères de gravités doit permettre de minimiser le risque de survenue de complications (tachycardie ou fibrillation ventriculaire). Il repose sur le traitement de la cause lorsque celle-ci est identifiée : cardiopathie sous-jacente. On peut également traiter un facteur déclenchant ou favorisant (hypokaliémie, arrêt d'un traitement dont on suspecte l'effet arythmogène...). Un traitement médicamenteux de type antiarythmique peut être proposé : bêta-bloquants, amiodarone, inhibiteurs calciques.
Notes et références[modifier | modifier le code]
- Hingorani P, Karnad DR, Rohekar P, Kerkar V, Lokhandwala YY, Kothari S, Arrhythmias seen in baseline 24-hour Holter ECG recordings in healthy normal volunteers during phase 1 clinical trials, J Clin Pharmacol, 2016;56:885–893
- Loring Z, Hanna P, Pellegrini CN, Longer ambulatory ECG monitoring increases identification of clinically significant ectopy, Pacing Clin Electrophysiol, 2016;39:592–597
- Marcus GM, Evaluation and management of premature ventricular complexes, Circulation, 2020;141:1404–1418
- Yokokawa M, Kim HM, Good E et al. Impact of QRS duration of frequent premature ventricular complexes on the development of cardiomyopathy, Heart Rhythm, 2012;9:1460–1464
- Baman TS, Lange DC, Ilg KJ et al. Relationship between burden of premature ventricular complexes and left ventricular function, Heart Rhythm, 2010;7:865-869
- Dukes JW, Dewland TA, Vittinghoff E et al. Ventricular ectopy as a predictor of heart failure and death, J Am Coll Cardiol, 2015;66:101–109
- Olgun H, Yokokawa M, Baman T et al. The role of interpolation in PVC-induced cardiomyopathy, Heart Rhythm, 2011;8:1046–1049
- (en) Lown B, Wolf M, « Approaches to sudden death from coronary heart disease », Circulation, vol. 44, no 1, , p. 130-42. (PMID 4104697, DOI 10.1161/01.CIR.44.1.130, lire en ligne [PDF])
- Priori SG, Blomstrom-Lundqvist C, Mazzanti A et al. 2015 ESC guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: the Task Force for the Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death of the European Society of Cardiology (ESC), Eur Heart J, 2015;36:2793–2867
- Krittayaphong R, Bhuripanyo K, Punlee K, Kangkagate C, Chaithiraphan S, Effect of atenolol on symptomatic ventricular arrhythmia without structural heart disease: a randomized placebo-controlled study, Am Heart J, 2002;144:e10
- Dukkipati SR, Choudry S, Koruth JS et al. Catheter ablation of ventricular tachycardia in structurally normal hearts: Indications, strategies, and outcomes—Part I, JACC, 2017;70:2909–2923
