Adénosine diphosphate ribose
| Adénosine diphosphate ribose | ||

| ||
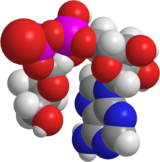 | ||
| Structure de l'adénosine diphosphate ribose. | ||
| Identification | ||
|---|---|---|
| Nom UICPA | ([(2R,3S,4R,5R)-5-(6-aminopurin-9-yl)-3,4-dihydroxyoxolan-2-yl]méthoxy-hydroxyphosphoryl)[(2R,3R,4R)-2,3,4-trihydroxy-5-oxopentyl] hydrogénophosphate | |
| Synonymes |
ADP-ribose, ADPR |
|
| No CAS | ||
| PubChem | 192 | |
| ChEBI | 16960 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C15H23N5O14P2 [Isomères] |
|
| Masse molaire[1] | 559,315 7 ± 0,018 8 g/mol C 32,21 %, H 4,14 %, N 12,52 %, O 40,05 %, P 11,08 %, |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
L’adénosine diphosphate ribose (ADP-ribose, ADPR), est un composé biochimique synthétisé sous forme de chaînes par la poly(ADP-ribose) polymérase. Elle peut être décrite comme une molécule d'adénosine diphosphate estérifiée par un ribose terminal.
Elle active, en s'y liant, le canal ionique TRPM2[2], au rôle encore mal compris mais qui interviendrait dans la sécrétion de l'insuline[3], dans la modulation d'une partie de la réponse au facteur de nécrose tumorale dans les leucocytes[4], ainsi que dans la toxicité, dans le cerveau, de la bêta-amyloïde, une protéine associée à la maladie d'Alzheimer[5].
L'ADP-ribose est polymérisé par des enzymes formant la série des poly(ADP-ribose) polymérases (PARP) et dont le rôle est de signaler la présence d'ADN monocaténaire au système enzymatique chargé de restaurer l'ADN bicaténaire. Une fois la réparation de l'ADN achevée, le poly(ADP-ribose) est dégradé par une poly(ADP-ribose) glycohydrolase (PARG)[6].
Métabolisme
ADP-D-ribose pyrophosphorylase

L'ADP-D-ribose pyrophosphorylase est une transférase (EC 2.7.7.96[7]) permettant la formation d'ADP-D-ribose en catalysant le transfert d'un groupe phosphate d'une molécule d'ATP sur un ribose-5-phosphate et d'un ribose sur l'ATP. La réaction dépend de la présence de diphosphate. En son absence, l'enzyme catalyse une autre réaction expliquée dans le paragraphe suivant.
ADP ribose phosphorylase

L'ADP ribose phosphorylase est une transférase (EC 2.7.7.35[8]) catalysant une réaction se produisant en absence de diphosphate produisant de l'ADP. Elle a été charactérisée chez Euglena gracilis.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
-
(en) Elena Fonfria, Ian C. B. Marshall, Christopher D. Benham, Izzy Boyfield, Jason D. Brown, Kerstin Hill, Jane P. Hughes, Stephen D. Skaper et Shaun McNulty, « TRPM2 channel opening in response to oxidative stress is dependent on activation of poly(ADP-ribose) polymerase », British Journal of Phamacology, vol. 143, no 1, , p. 186-192 (lire en ligne)
DOI 10.1038/sj.bjp.0705914 -
(en) Kazuya Togashi, Yuji Hara, Tomoko Tominaga, Tomohiro Higashi, Yasunobu Konishi, Yasuo Mori et Makoto Tominaga, « TRPM2 activation by cyclic ADP-ribose at body temperature is involved in insulin secretion », The EMBO Journal, vol. 25, no 9, , p. 1804-1815 (lire en ligne)
DOI 10.1038/sj.emboj.7601083 -
(en) Shinichiro Yamamoto, Shunichi Shimizu, Shigeki Kiyonaka, Nobuaki Takahashi, Teruaki Wajima, Yuji Hara, Takaharu Negoro, Toshihito Hiroi, Yuji Kiuchi, Takaharu Okada, Shuji Kaneko, Ingo Lange, Andrea Fleig, Reinhold Penner, Miyuki Nishi, Hiroshi Takeshima et Yasuo Mori, « TRPM2-mediated Ca2+ influx induces chemokine production in monocytes that aggravates inflammatory neutrophil infiltration », Nature Medicine, vol. 14, , p. 738-747 (lire en ligne)
DOI 10.1038/nm1758 -
(en) B. A. Miller, « The Role of TRP Channels in Oxidative Stress-induced Cell Death », Journal of Membrane Biology, vol. 209, no 1, , p. 31-41 (lire en ligne)
DOI 10.1007/s00232-005-0839-3 - (en) Maxim Isabelle, Xavier Moreel, Jean-Philippe Gagné, Michèle Rouleau, Chantal Ethier, Pierre Gagné, Michael J Hendzel et Guy G Poirier, « Investigation of PARP-1, PARP-2, and PARG interactomes by affinity-purification mass spectrometry », Proteome Science, vol. 8, , p. 22 (PMID 20388209, PMCID 2861645, DOI 10.1186/1477-5956-8-22)
- « ENZYME entry 2.7.7.96 », sur enzyme.expasy.org (consulté le )
- « ENZYME entry 2.7.7.35 », sur enzyme.expasy.org (consulté le )
