Sulindac
| Sulindac | |

| |
| Identification | |
|---|---|
| Nom UICPA | acide {(1Z)-5-fluoro-2-methyl-1-[4-(methylsulfinyl)benzylidène]-1H-indène-3-yl}acetic |
| No CAS | |
| No ECHA | 100.048.909 |
| DrugBank | DB00861 |
| PubChem | 1548887 |
| SMILES | |
| InChI | |
| Apparence | solide[1] |
| Propriétés chimiques | |
| Formule | C20H17FO3S |
| Masse molaire[2] | 356,411 ± 0,023 g/mol C 67,4 %, H 4,81 %, F 5,33 %, O 13,47 %, S 9 %, |
| Propriétés physiques | |
| T° fusion | 183-184 °C[1] |
| Solubilité | eau : 3000 mg/L [réf. souhaitée] |
| Cristallographie | |
| Système cristallin | triclinique[réf. souhaitée] |
| Précautions | |
| SGH[1] | |
| H302, H315, H361, P201, P202, P261, P264, P270, P271, P281, P312, P321, P330, P362, P301+P312, P302+P352, P304+P340, P305+P351+P338, P308+P313, P332+P313, P337+P313, P405, P403+P233 et P501 |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le sulindac est un anti-inflammatoire non stéroïdien (AINS) indénique du groupe des indoles. Il possède les propriétés suivantes : antalgique, antipyrétique, anti-inflammatoire, inhibition des fonctions plaquettaires. Le sulindac est utilisé dans la prise en charge de l'arthrose, de rhumatismes abarticulaires et inflammatoires chroniques.
Synthèse[modifier | modifier le code]
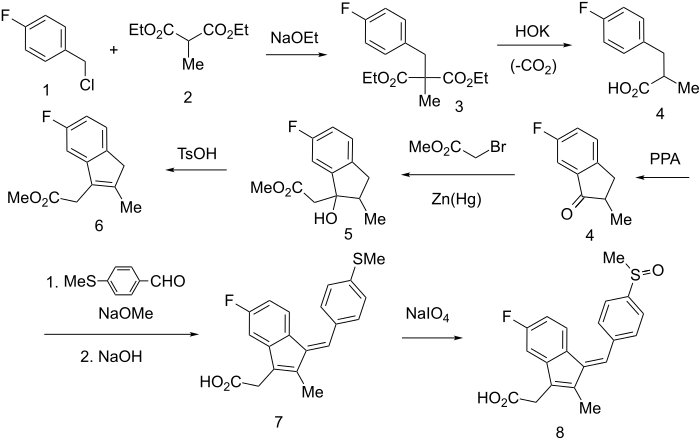
La synthèse commence par la réaction du chlorure de p-fluorobenzyle (1) avec le méthylmalonate de diéthyle (2) déprotoné par l'éthanolate de sodium et donne un diester intermédiaire (3), dont la saponification et la décarboxylation subséquente conduisent à la 5-fluoro-2-méthyl-3-indanone (4). Alternativement, 4 peut être formé par réaction de Perkin entre le p-fluorobenzaldéhyde et l'anhydride propionique en présence d'acétate de sodium, puis hydrogénation catalytique de la double liaison à l'aide d'un catalyseur au palladium sur charbon.
Une réaction de Réformatski avec un amalgame de zinc et un ester bromoacétique conduit au carbinol (5), qui est ensuite déshydraté avec de l'acide tosylique en l'indène 6. Alternativement, cette étape peut être effectuée dans une condensation de Knoevenagel avec de l'acide cyanoacétique, qui est ensuite décarboxylée.
Le groupe méthylène actif est condensé avec du p-méthylthiobenzaldéhyde, en utilisant du méthoxyde de sodium comme catalyseur, puis saponifié pour donner 7 qui à son tour s'oxyde avec du métapériodate de sodium en sulfoxyde 8 qui est l'agent anti-inflammatoire sulindac.
Notes et références[modifier | modifier le code]
- PubChem CID 1548887.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- R. F. Shuman, S. H. Pines, W. E. Shearin, R. F. Czaja, N. L. Abramson et R. Tull, « A sterically efficient synthesis of (Z)-5-fluoro-2-methyl-1-(p-methylthiobenzylidene)-3-indenylacetic acid and its S-oxide, sulindac », The Journal of Organic Chemistry, vol. 42, no 11, , p. 1914 (DOI 10.1021/jo00431a019)
- R.B. Greenwald, E.B. Witzel, DE 2039426 (1971).
- J.B. Conn, D.F. Hinkley,(en) Brevet U.S. 3647858 (1972).
- R.B. Greenwald, H. Jones, (en) Brevet U.S. 3654349 (1972).


