Organoïde
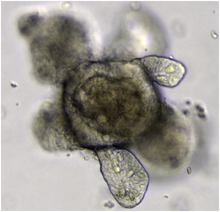
Un organoïde est une version miniature et simplifiée d'un organe, fabriquée in vitro en trois dimensions et qui présente une micro-anatomie réaliste[1]. Il est issu d'une ou de quelques cellules d'un tissu, de cellules souches embryonnaires[2] ou de cellules souches pluripotentes induites (iPSC)[3], qui peuvent s'auto-organiser en une structure tridimensionnelle grâce à leurs capacités d'auto-renouvellement et de différenciation. Les organoïdes sont utilisés par les scientifiques pour étudier les maladies et les traitements en laboratoire. Un organoïde présente les propriétés suivantes:
- il possède plusieurs types cellulaires spécifiques d’un organe
- il est capable de récapituler certaines fonctions spécifiques de l'organe (par exemple la contraction, l'activité neuronale, la sécrétion endocrinienne, la filtration, l'excrétion)
- il se forme par regroupement et auto-organisation dans l’espace, à la manière d'un organe.
Histoire[modifier | modifier le code]
Les tentatives de création d'organes in vitro ont commencé en 1907 par des expériences de dissociation-réagrégation, où Henry Van Peters Wilson a démontré que les cellules spongieuses dissociées mécaniquement peuvent se réagréger et s'auto-organiser pour générer un organisme entier[4]. Au cours des décennies suivantes, plusieurs laboratoires ont pu générer différents types d'organes in vitro grâce à la dissociation et à la réagrégation de tissus d'organes obtenus à partir d'amphibiens[5] ou d'embryons de poussins[6]. Les phénomènes de cellules mécaniquement dissociées s'agrégeant et se réorganisant pour reformer le tissu à partir duquel elles ont été obtenues ont ensuite conduit au développement de l'hypothèse de l'adhésion différentielle par Malcolm Steinberg en 1964.
Avec l'avènement du domaine de la biologie des cellules souches, le potentiel des cellules souches à former des organes in vitro a été réalisé très tôt avec l'observation que lorsque les cellules souches forment des tératomes ou des corps embryoïdes, les cellules différenciées peuvent s'organiser en différentes structures ressemblant à celles trouvées dans plusieurs types de tissus. L'avènement du domaine des organoïdes a commencé par le passage de la culture et de la différenciation des cellules souches dans des supports 2D à des supports 3D pour permettre le développement des structures tridimensionnelles complexes des organes.
En 2006, Yaakov Nahmias et David Odde ont montré l'auto-assemblage d'organoïdes hépatiques vasculaires maintenus pendant plus de 50 jours in vitro[7].
En 2008, Yoshiki Sasai et son équipe de l'institut RIKEN ont démontré que les cellules souches peuvent être transformées en boules de cellules neurales qui s'auto-organisent en couches distinctes[8].
En 2009, le laboratoire de Hans Clevers (en) de l'Institut Hubrecht et du Centre médical universitaire d'Utrecht, aux Pays-Bas, a montré que des cellules souches intestinales exprimant LGR5 s'auto-organisent en structures crypt-villositaires in vitro sans nécessiter de niche mésenchymateuse[9].
En 2010, Mathieu Unbekandt et Jamie A. Davies ont démontré la production d'organoïdes rénaux à partir de cellules souches rénogènes dérivées de fœtus murin. Des rapports ultérieurs ont montré une fonction physiologique significative de ces organoïdes in vitro et in vivo[10].
En 2013, Madeline Lancaster de l'Institut de biotechnologie moléculaire de l'Académie autrichienne des sciences a établi un protocole de culture d'organoïdes cérébraux dérivés de cellules souches qui imitent l'organisation cellulaire du cerveau humain en développement[11].
En 2014, Artem Shkumatov à l'Université de l'Illinois à Urbana-Champaign a démontré que des organoïdes cardiovasculaires peuvent être formés à partir de cellules souches embryonnaires en modulant la rigidité du substrat auquel ils adhèrent[12].
Processus de fabrication[modifier | modifier le code]
La formation d'organoïdes nécessite généralement la culture des cellules souches ou des cellules progénitrices dans un milieu en trois dimensions. Le milieu 3D peut être fabriqué à l'aide d'un hydrogel de matrice extracellulaire tel que Matrigel ou Cultrex BME, qui est une matrice extracellulaire riche en laminine sécrétée par la lignée tumorale Engelbreth-Holm-Swarm[13]. Les corps organoïdes peuvent ensuite être fabriqués en incorporant des cellules souches dans le support 3D. Lorsque des cellules souches pluripotentes sont utilisées pour la création de l'organoïde, les cellules sont généralement, mais pas tout le temps, autorisées à former des corps embryoïdes. Ces corps embryoïdes sont ensuite traités pharmacologiquement avec des facteurs de croissance et de différenciation pour conduire à l'identité organoïde souhaitée. Des organoïdes ont également été créés à l'aide de cellules souches adultes extraites de l'organe cible et cultivées dans des milieux 3D[14].
Différents types d'organoïdes[modifier | modifier le code]
Une multitude de structures d'organes ont été modélisées à l'aide d'organoïdes, par exemple des organoïdes cérébraux[15], thymiques[16], thyroidiens[17], intestinaux[18], hépatiques[19], testiculaires[20], pancréatiques[21], rétiniens[22], rénaux[23] ou d'embryon précoce[24] (gastruloïdes). Cette section a pour objectif de présenter des exemples utilisés dans la recherche actuelle.
Organoïde cérébral[modifier | modifier le code]
Un organoïde cérébral décrit des organes miniatures cultivés artificiellement, in vitro, ressemblant au cerveau. Les organoïdes cérébraux sont créés en cultivant des cellules souches pluripotentes humaines dans une structure tridimensionnelle se développent sur une période de plusieurs mois[15]. La procédure a des applications potentielles dans l'étude du développement, de la physiologie et de la fonction cérébrales. Les organoïdes cérébraux peuvent éprouver des « sensations simples » en réponse à une stimulation externe et les neuroscientifiques Andrea Lavazza, Elan Ohayon et Hideya Sakaguchi font partie de ceux qui craignent que de tels organes puissent développer une sensibilité[25]. Ils proposent que l'évolution ultérieure de la technique soit soumise à une procédure de surveillance éthique rigoureuse.
Organoïde pulmonaire[modifier | modifier le code]

Les organoïdes pulmonaires sont des micro-tissus cultivés en trois dimensions qui reproduisent les caractéristiques morphologiques et fonctionnelles des voies respiratoires[26]. Ils peuvent contenir les différents types de cellules épithéliales du poumon humain reposant sur une matrice extra-cellulaire. Les organoïdes pulmonaires présentent de nombreuses caractéristiques des voies respiratoires humaines, telles que la sécrétion de mucus, le battement des cils et la régénération. Cette fidélité à la réalité biologique en fait un outil très efficace pour étudier le développement embryonnaire du tissu pulmonaire, les mécanismes de réparation dans les lésions pulmonaires ainsi que les mécanismes physiopathologiques des maladies pulmonaires. Les organoïdes pulmonaires peuvent également être utilisés pour évaluer la toxicité ou l'efficacité des médicaments lors de tests in vitro.
Organoïde rétinien[modifier | modifier le code]
Les organoïdes rétiniens sont des structures en trois dimensions, auto-organisées qui contiennent tous les types cellulaires de la rétine[27]. Il y a trois étapes dans la génération d'organoïdes rétiniens. Les organoïdes de 35 à 40 jours sont formés d’un neuro-épithélium contenant des progéniteurs rétiniens en prolifération. Durant les stades intermédiaires (entre 60 et 100 jours), on observe une séparation nette entre une couche nucléaire externe avec des photorécepteurs et une couche interne contenant des neurones de la rétine interne. Enfin, dans les organoïdes rétiniens tardifs (après 150-175 jours), les photorécepteurs atteignent un stade avancé de développement. La cinétique de développement est assez fidèle au développement fœtal humain (entre la 23e et la 30e semaine). Il persiste cependant certaines limites, notamment lorsqu’il s’agit de maintenir ces organoïdes à long terme. On observe une désorganisation progressive de la région interne des organoïdes aux stades tardifs, ainsi qu’une perte des cellules ganglionnaires, ce qui est prévisible dans ce type de cultures car ces neurones sont dépourvus de leurs cibles cérébrales naturelles.
Applications[modifier | modifier le code]
Etude du développement[modifier | modifier le code]
Les organoïdes offrent aux chercheurs un modèle exceptionnel pour étudier la biologie du développement[28]. Depuis l'identification des cellules souches pluripotentes, de grands progrès ont été accomplis dans la direction du destin des cellules souches pluripotentes in vitro à l'aide de cultures 2D. Ces progrès dans la direction du destin de la cellule souche pluripotente, associés aux progrès des techniques de culture 3D, ont permis la création d'organoïdes qui récapitulent les propriétés de diverses sous-régions spécifiques d'une multitude d'organes. L'utilisation de ces organoïdes a ainsi grandement contribué à élargir notre compréhension des processus d'organogenèse et du domaine de la biologie du développement. Dans le développement du système nerveux central, par exemple, les organoïdes ont contribué à notre compréhension des forces physiques qui sous-tendent la formation de la cupule rétinienne. Des travaux plus récents ont considérablement prolongé les périodes de croissance des organoïdes corticaux et à près d'un an dans des conditions de différenciation spécifiques, les organoïdes persistent et présentent certaines caractéristiques des stades de développement du fœtus humain[29].
Modélisation de maladies[modifier | modifier le code]
Les organoïdes offrent la possibilité de créer des modèles cellulaires de maladies humaines, qui peuvent être étudiés en laboratoire pour mieux comprendre les causes de la maladie et identifier les traitements possibles. Dans un exemple, le système d'édition du génome appelé CRISPR a été appliqué à des cellules souches pluripotentes humaines pour introduire des mutations ciblées dans des gènes pertinents pour deux maladies rénales différentes, la polykystose rénale et la glomérulosclérose segmentaire focale[30]. Ces cellules souches pluripotentes modifiées par CRISPR ont ensuite été cultivées dans des organoïdes rénaux humains, qui présentaient des phénotypes spécifiques à la maladie. Les organoïdes rénaux des cellules souches présentant des mutations de la polykystose rénale ont formé de grandes structures de kystes translucides à partir des tubules rénaux. Lorsqu'ils sont cultivés en l'absence d'indices adhérents (en suspension), ces kystes ont atteint des tailles de 1 cm de diamètre sur plusieurs mois[31]. Les organoïdes rénaux présentant des mutations dans un gène lié à la glomérulosclérose segmentaire focale ont développé des défauts de jonction entre les podocytes, les cellules filtrantes affectées dans cette maladie[32]. Il est important de noter que ces phénotypes de la maladie étaient absents des organoïdes témoins de fond génétique identique, mais dépourvus des mutations CRISPR. La comparaison de ces phénotypes organoïdes avec des tissus malades de souris et d'humains a suggéré des similitudes avec des défauts de développement précoce.
Développées pour la première fois par Takahashi et Shinya Yamanaka en 2007, les cellules souches pluripotentes induites (iPSC) peuvent également être reprogrammées à partir de fibroblastes cutanés de patients[33]. Ces cellules souches portent le patrimoine génétique exact du patient, y compris toute mutation génétique susceptible de contribuer au développement d'une maladie humaine. La différenciation de ces cellules en organoïdes rénaux a été réalisée chez des patients atteints du syndrome de Lowe en raison de mutations ORCL1. Ce rapport a comparé les organoïdes rénaux différenciés de l'iPSC du patient à l'iPSC témoin non apparenté et a démontré une incapacité des cellules rénales du patient à mobiliser le facteur de transcription SIX2 du complexe de Golgi[34]. Étant donné que SIX2 est un marqueur bien caractérisé des cellules progénitrices du néphron dans le mésenchyme de la coiffe, les auteurs ont conclu que la maladie rénale fréquemment observée dans le syndrome de Lowe (échec global de la réabsorption du tubule proximal ou syndrome de Fanconi rénal) pourrait être liée à une altération de la structuration du néphron résultant du néphron cellules progénitrices dépourvues de cette importante expression du gène SIX2.
D'autres études ont utilisé l'édition de gènes CRISPR pour corriger la mutation du patient dans les cellules iPSC du patient afin de créer un contrôle isogénique, qui peut être effectué simultanément avec la reprogrammation des iPSC[35]. La comparaison d'un organoïde dérivé d'iPSC d'un patient avec un contrôle isogénique est l'étalon-or actuel dans le domaine car elle permet d'isoler la mutation d'intérêt comme seule variable dans le modèle expérimental[36]. Dans un de ces rapports, des organoïdes rénaux dérivés d'iPSC d'un patient atteint du syndrome de Mainzer-Saldino en raison de mutations hétérozygotes composées dans IFT140 ont été comparés à un organoïde témoin isogénique dans lequel une variante IFT140 donnant lieu à un transcrit d'ARNm non viable a été corrigé par CRISPR . Les organoïdes rénaux des patients ont démontré une morphologie ciliaire anormale compatible avec les modèles animaux existants qui a été ramenée à la morphologie de type sauvage dans les organoïdes corrigés par le gène. Le profilage transcriptionnel comparatif des cellules épithéliales purifiées à partir d'organoïdes patients et témoins a mis en évidence des voies impliquées dans la polarité cellulaire, les jonctions cellule-cellule et l'assemblage moteur de la dynéine, dont certaines avaient été impliquées pour d'autres génotypes au sein de la famille phénotypique des ciliopathies rénales. Un autre rapport utilisant un contrôle isogénique a démontré une localisation anormale de la néphrine dans les glomérules des organoïdes rénaux générés à partir d'un patient atteint d'un syndrome néphrotique congénital.
Médecine personnalisée[modifier | modifier le code]
Les organoïdes intestinaux issus de biopsies rectales à l'aide de protocoles de culture établis par le groupe de Hans Clevers (en) ont été utilisés pour modéliser la mucoviscidose[37] et ont conduit à la première application d'organoïdes pour un traitement personnalisé[38]. La mucoviscidose est une maladie héréditaire causée par des mutations du gène qui code pour un canal ionique épithélial nécessaire aux fluides de surface épithéliaux sains. Des études menées par le laboratoire de Jeffrey Beekman (Wilhelmina Children's Hospital, University Medical Center Utrecht, Pays-Bas) ont décrit en 2013 que la stimulation des organoïdes colorectaux avec des agonistes de l'AMPc tels que la forskoline ou la toxine du choléra induisait un gonflement rapide des organoïdes d'une manière entièrement dépendante du CFTR[37]. Alors que les organoïdes de sujets non atteints de mucoviscidose gonflent en réponse à la forskoline en raison du transport de fluide dans les lumières des organoïdes, cela est sévèrement réduit ou absent chez les organoïdes dérivés de personnes atteintes de mucoviscidose. Le gonflement pourrait être restauré par des thérapeutiques qui réparent la protéine CFTR (modulateurs CFTR), ce qui indique que les réponses individuelles à la thérapie de modulation CFTR pourraient être quantifiées dans un environnement de laboratoire préclinique. Schwank et al. a également démontré que le phénotype organoïde de la mucoviscidose intestinale pouvait être réparé par l'édition du gène CRISPR-Cas9 en 2013[39].
Des études de suivi par Dekkers et al. en 2016 a révélé que les différences quantitatives dans le gonflement induit par la forskoline entre les organoïdes intestinaux dérivés de personnes atteintes de mucoviscidose sont associées à des marqueurs diagnostiques et pronostiques connus tels que des mutations du gène CFTR ou des biomarqueurs in vivo de la fonction CFTR . De plus, les auteurs ont démontré que les réponses des modulateurs CFTR dans les organoïdes intestinaux avec des mutations CFTR spécifiques étaient corrélées avec les données publiées des essais cliniques de ces traitements. Cela a conduit à des études précliniques où des organoïdes de patients présentant des mutations CFTR extrêmement rares pour lesquels aucun traitement n'a été enregistré se sont avérés répondre fortement à un modulateur CFTR disponible en clinique. Le bénéfice clinique suggéré du traitement pour ces sujets sur la base du test organoïde préclinique a ensuite été confirmé lors de l'introduction clinique du traitement par les membres du centre clinique de FK sous la supervision de Kors van der Ent (Département de pneumologie pédiatrique, Hôpital pour enfants Wilhelmina, Centre médical universitaire Utrecht, Pays-Bas). Ces études montrent pour la première fois que les organoïdes peuvent être utilisés pour l'adaptation individuelle d'une thérapie ou d'une médecine personnalisée.
Greffe d'organe[modifier | modifier le code]
La recherche sur les organoïdes pourrait à terme permettre de reconstituer des organes complets par exemple pour permettre des greffes et remplacer des organes défectueux (Cœur, rein, foie, utérus etc.)[40].
Notes et références[modifier | modifier le code]
- Jean-Luc Galzi, Thierry Jouault et Joëlle Amédée, « Les organoïdes : des mini-organes au service de la biomédecine », médecine/sciences, vol. 35, no 5, , p. 467–469 (ISSN 0767-0974 et 1958-5381, DOI 10.1051/medsci/2019091, lire en ligne, consulté le )
- Pauliina Damdimopoulou, Sergey Rodin, Sonya Stenfelt et Liselotte Antonsson, « Human embryonic stem cells », Best Practice & Research Clinical Obstetrics & Gynaecology, vol. 31, , p. 2–12 (ISSN 1521-6934, DOI 10.1016/j.bpobgyn.2015.08.010, lire en ligne, consulté le )
- Kazutoshi Takahashi et Shinya Yamanaka, « Induction of Pluripotent Stem Cells from Mouse Embryonic and Adult Fibroblast Cultures by Defined Factors », Cell, vol. 126, no 4, , p. 663–676 (ISSN 0092-8674, DOI 10.1016/j.cell.2006.07.024, lire en ligne, consulté le )
- H. V. Wilson, « A New Method by Which Sponges May Be Artificially Reared », Science, vol. 25, no 649, , p. 912–915 (ISSN 0036-8075 et 1095-9203, DOI 10.1126/science.25.649.912, lire en ligne, consulté le )
- Johannes Holtfreter, « A study of the mechanics of gastrulation », Journal of Experimental Zoology, vol. 95, no 2, , p. 171–212 (ISSN 0022-104X et 1097-010X, DOI 10.1002/jez.1400950203, lire en ligne, consulté le )
- Paul Weiss et A. C. Taylor, « RECONSTITUTION OF COMPLETE ORGANS FROM SINGLE-CELL SUSPENSIONS OF CHICK EMBRYOS IN ADVANCED STAGES OF DIFFERENTIATION », Proceedings of the National Academy of Sciences, vol. 46, no 9, , p. 1177–1185 (ISSN 0027-8424 et 1091-6490, DOI 10.1073/pnas.46.9.1177, lire en ligne, consulté le )
- Yaakov Nahmias, Robert E. Schwartz, Wei-Shou Hu et Catherine M. Verfaillie, « Endothelium-Mediated Hepatocyte Recruitment in the Establishment of Liver-like TissueIn Vitro », Tissue Engineering, vol. 12, no 6, , p. 1627–1638 (ISSN 1076-3279 et 1557-8690, DOI 10.1089/ten.2006.12.1627, lire en ligne, consulté le )
- « Mini human brains grown in lab for first time », New Scientist, vol. 219, no 2932, , p. 17 (ISSN 0262-4079, DOI 10.1016/s0262-4079(13)62131-4, lire en ligne, consulté le )
- (en) Toshiro Sato, Robert G. Vries, Hugo J. Snippert et Marc van de Wetering, « Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche », Nature, vol. 459, no 7244, , p. 262–265 (ISSN 1476-4687, DOI 10.1038/nature07935, lire en ligne, consulté le )
- Mathieu Unbekandt et Jamie A. Davies, « Dissociation of embryonic kidneys followed by reaggregation allows the formation of renal tissues », Kidney International, vol. 77, no 5, , p. 407–416 (ISSN 0085-2538, DOI 10.1038/ki.2009.482, lire en ligne, consulté le )
- Artem Shkumatov, Kwanghyun Baek et Hyunjoon Kong, « Matrix Rigidity-Modulated Cardiovascular Organoid Formation from Embryoid Bodies », PLoS ONE, vol. 9, no 4, , e94764 (ISSN 1932-6203, DOI 10.1371/journal.pone.0094764, lire en ligne, consulté le )
- Stuart M. Chambers, Jason Tchieu et Lorenz Studer, « Build-a-Brain », Cell Stem Cell, vol. 13, no 4, , p. 377–378 (ISSN 1934-5909, DOI 10.1016/j.stem.2013.09.010, lire en ligne, consulté le )
- M L Li, J Aggeler, D A Farson et C Hatier, « Influence of a reconstituted basement membrane and its components on casein gene expression and secretion in mouse mammary epithelial cells. », Proceedings of the National Academy of Sciences, vol. 84, no 1, , p. 136–140 (ISSN 0027-8424 et 1091-6490, DOI 10.1073/pnas.84.1.136, lire en ligne, consulté le )
- Agnieszka Pastuła, Moritz Middelhoff, Anna Brandtner et Moritz Tobiasch, « Three-Dimensional Gastrointestinal Organoid Culture in Combination with Nerves or Fibroblasts: A Method to Characterize the Gastrointestinal Stem Cell Niche », Stem Cells International, vol. 2016, , p. 1–16 (ISSN 1687-966X et 1687-9678, DOI 10.1155/2016/3710836, lire en ligne, consulté le )
- Madeline A. Lancaster, Magdalena Renner, Carol-Anne Martin et Daniel Wenzel, « Cerebral organoids model human brain development and microcephaly », Nature, vol. 501, no 7467, , p. 373–379 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/nature12517, lire en ligne, consulté le )
- Nicholas Bredenkamp, Svetlana Ulyanchenko, Kathy Emma O’Neill et Nancy Ruth Manley, « An organized and functional thymus generated from FOXN1-reprogrammed fibroblasts », Nature Cell Biology, vol. 16, no 9, , p. 902–908 (ISSN 1465-7392 et 1476-4679, DOI 10.1038/ncb3023, lire en ligne, consulté le )
- Andreas Martin, Giuseppe Barbesino et Terry F. Davies, « T-Cell Receptors and Autoimmune Thyroid Disease—Signposts for T-Cell-Antigen Driven Diseases », International Reviews of Immunology, vol. 18, nos 1-2, , p. 111–140 (ISSN 0883-0185, DOI 10.3109/08830189909043021, lire en ligne, consulté le )
- Toshiro Sato, Robert G. Vries, Hugo J. Snippert et Marc van de Wetering, « Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche », Nature, vol. 459, no 7244, , p. 262–265 (ISSN 1476-4687, PMID 19329995, DOI 10.1038/nature07935, lire en ligne, consulté le )
- Meritxell Huch, Helmuth Gehart, Ruben van Boxtel et Karien Hamer, « Long-term culture of genome-stable bipotent stem cells from adult human liver », Cell, vol. 160, nos 1-2, , p. 299–312 (ISSN 1097-4172, PMID 25533785, PMCID 4313365, DOI 10.1016/j.cell.2014.11.050, lire en ligne, consulté le )
- Guillaume Richer, Yoni Baert et Ellen Goossens, « In-vitro spermatogenesis through testis modelling: Toward the generation of testicular organoids », Andrology, vol. 8, no 4, , p. 879–891 (ISSN 2047-2927, PMID 31823507, PMCID 7496450, DOI 10.1111/andr.12741, lire en ligne, consulté le )
- Meritxell Huch, Paola Bonfanti, Sylvia F. Boj et Toshiro Sato, « Unlimited in vitro expansion of adult bi-potent pancreas progenitors through the Lgr5/R-spondin axis », The EMBO journal, vol. 32, no 20, , p. 2708–2721 (ISSN 1460-2075, PMID 24045232, PMCID 3801438, DOI 10.1038/emboj.2013.204, lire en ligne, consulté le )
- Michelle O'Hara-Wright et Anai Gonzalez-Cordero, « Retinal organoids: a window into human retinal development », Development (Cambridge, England), vol. 147, no 24, , dev189746 (ISSN 1477-9129, PMID 33361444, PMCID 7774906, DOI 10.1242/dev.189746, lire en ligne, consulté le )
- Minoru Takasato, Pei X. Er, Han S. Chiu et Barbara Maier, « Kidney organoids from human iPS cells contain multiple lineages and model human nephrogenesis », Nature, vol. 526, no 7574, , p. 564–568 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/nature15695, lire en ligne, consulté le )
- Susanne C. van den Brink, Peter Baillie-Johnson, Tina Balayo et Anna-Katerina Hadjantonakis, « Symmetry breaking, germ layer specification and axial organisation in aggregates of mouse embryonic stem cells », Development, vol. 141, no 22, , p. 4231–4242 (ISSN 1477-9129 et 0950-1991, DOI 10.1242/dev.113001, lire en ligne, consulté le )
- Andrea Lavazza et Marcello Massimini, « Cerebral organoids: ethical issues and consciousness assessment », Journal of Medical Ethics, vol. 44, no 9, , p. 606–610 (ISSN 1473-4257, PMID 29491041, DOI 10.1136/medethics-2017-104555, lire en ligne, consulté le )
- Chloé Bourguignon, Charlotte Vernisse, Joffrey Mianné et Mathieu Fieldès, « Les organoïdes pulmonaires », médecine/sciences, vol. 36, no 4, , p. 382–388 (ISSN 0767-0974 et 1958-5381, DOI 10.1051/medsci/2020056, lire en ligne, consulté le )
- Olivier Goureau, Sacha Reichman et Gaël Orieux, « Les organoïdes de rétine », médecine/sciences, vol. 36, nos 6-7, , p. 626–632 (ISSN 0767-0974 et 1958-5381, DOI 10.1051/medsci/2020098, lire en ligne, consulté le )
- Marius Ader et Elly M Tanaka, « Modeling human development in 3D culture », Current Opinion in Cell Biology, vol. 31, , p. 23–28 (ISSN 0955-0674, DOI 10.1016/j.ceb.2014.06.013, lire en ligne, consulté le )
- Aaron Gordon, Se-Jin Yoon, Stephen S. Tran et Christopher D. Makinson, « Long-term maturation of human cortical organoids matches key early postnatal transitions », Nature Neuroscience, vol. 24, no 3, , p. 331–342 (ISSN 1097-6256 et 1546-1726, DOI 10.1038/s41593-021-00802-y, lire en ligne, consulté le )
- Benjamin S. Freedman, Craig R. Brooks, Albert Q. Lam et Hongxia Fu, « Modelling kidney disease with CRISPR-mutant kidney organoids derived from human pluripotent epiblast spheroids », Nature Communications, vol. 6, , p. 8715 (ISSN 2041-1723, PMID 26493500, PMCID 4620584, DOI 10.1038/ncomms9715, lire en ligne, consulté le )
- Nelly M. Cruz, Xuewen Song, Stefan M. Czerniecki et Ramila E. Gulieva, « Organoid cystogenesis reveals a critical role of microenvironment in human polycystic kidney disease », Nature Materials, vol. 16, no 11, , p. 1112–1119 (ISSN 1476-1122, PMID 28967916, PMCID 5936694, DOI 10.1038/nmat4994, lire en ligne, consulté le )
- Yong Kyun Kim, Ido Refaeli, Craig R. Brooks et Peifeng Jing, « Gene-Edited Human Kidney Organoids Reveal Mechanisms of Disease in Podocyte Development », Stem Cells (Dayton, Ohio), vol. 35, no 12, , p. 2366–2378 (ISSN 1549-4918, PMID 28905451, PMCID 5742857, DOI 10.1002/stem.2707, lire en ligne, consulté le )
- Kazutoshi Takahashi, Koji Tanabe, Mari Ohnuki et Megumi Narita, « Induction of Pluripotent Stem Cells from Adult Human Fibroblasts by Defined Factors », Cell, vol. 131, no 5, , p. 861–872 (ISSN 0092-8674, DOI 10.1016/j.cell.2007.11.019, lire en ligne, consulté le )
- Wen-Chieh Hsieh, Swetha Ramadesikan, Donna Fekete et Ruben Claudio Aguilar, « Kidney-differentiated cells derived from Lowe Syndrome patient's iPSCs show ciliogenesis defects and Six2 retention at the Golgi complex », PloS One, vol. 13, no 2, , e0192635 (ISSN 1932-6203, PMID 29444177, PMCID 5812626, DOI 10.1371/journal.pone.0192635, lire en ligne, consulté le )
- Sara E. Howden, James A. Thomson et Melissa H. Little, « Simultaneous reprogramming and gene editing of human fibroblasts », Nature Protocols, vol. 13, no 5, , p. 875–898 (ISSN 1750-2799, PMID 29622803, PMCID 5997775, DOI 10.1038/nprot.2018.007, lire en ligne, consulté le )
- Sandra J. Engle, Laura Blaha et Robin J. Kleiman, « Best Practices for Translational Disease Modeling Using Human iPSC-Derived Neurons », Neuron, vol. 100, no 4, , p. 783–797 (ISSN 0896-6273, DOI 10.1016/j.neuron.2018.10.033, lire en ligne, consulté le )
- Johanna F Dekkers, Caroline L Wiegerinck, Hugo R de Jonge et Inez Bronsveld, « A functional CFTR assay using primary cystic fibrosis intestinal organoids », Nature Medicine, vol. 19, no 7, , p. 939–945 (ISSN 1078-8956 et 1546-170X, DOI 10.1038/nm.3201, lire en ligne, consulté le )
- Johanna F. Dekkers, Gitte Berkers, Evelien Kruisselbrink et Annelotte Vonk, « Characterizing responses to CFTR-modulating drugs using rectal organoids derived from subjects with cystic fibrosis », Science Translational Medicine, vol. 8, no 344, (ISSN 1946-6234 et 1946-6242, DOI 10.1126/scitranslmed.aad8278, lire en ligne, consulté le )
- Gerald Schwank, Bon-Kyoung Koo, Valentina Sasselli et Johanna F. Dekkers, « Functional Repair of CFTR by CRISPR/Cas9 in Intestinal Stem Cell Organoids of Cystic Fibrosis Patients », Cell Stem Cell, vol. 13, no 6, , p. 653–658 (ISSN 1934-5909, DOI 10.1016/j.stem.2013.11.002, lire en ligne, consulté le )
- « Greffes : de nouvelles alternatives face au manque de greffons », sur Ça m'intéresse, (consulté le )
Voir aussi[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- (en) David A. Turner, Peter Baillie-Johnson et Alfonso Martinez Arias, « Organoids and the genetically encoded self-assembly of embryonic stem cells », Bioessays, vol. 38, no 2, , p. 181-191 (PMID 26666846, PMCID 4737349, DOI 10.1002/bies.201500111)
Liens externes[modifier | modifier le code]
- « Organoïdes : silence, ça puce ! », La Science, CQFD, France Culture, 25 avril 2024.
- « Organoïdes : small is beautiful » La Méthode scientifique, France Culture, 8 novembre 2019.
- [vidéo] Comment faire pousser des organes ? sur YouTube, chaine Scilabus.
