Isopropyl dodécyl fluorophosphonate
| Isopropyl dodécyl fluorophosphonate | |
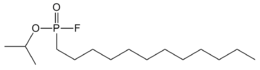 Structure de l'IDFP |
|
| Identification | |
|---|---|
| Nom UICPA | 1-[fluoro(propan-2-yloxy)phosphoryl]dodecane |
| No CAS | |
| PubChem | 24762154 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C15H32FO2P [Isomères] |
| Masse molaire[1] | 294,385 5 ± 0,014 8 g/mol C 61,2 %, H 10,96 %, F 6,45 %, O 10,87 %, P 10,52 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'isopropyl dodécyl fluorophosphonate (IDFP) est un composé organophosphoré apparenté au gaz innervant sarin. Comme celui-ci, l'IDFP est un inhibiteur irréversible de plusieurs enzymes différentes qui interviennent normalement pour dégrader des neurotransmetteurs. Sa longue chaîne alkyle fait de l'IDFP un inhibiteur de l'acétylcholinestérase (AChE) sensiblement moins puissant que le sarin, avec une concentration inhibitrice médiane IC50 de 6,3 mM, mais cette molécule reste un inhibiteur puissant de la monoacylglycérol lipase (MAGL), responsable de la dégradation de l'endocannabinoïde 2-arachidonylglycérol (2-AG), et de l'hydrolase des amides d'acides gras (FAAH), qui dégrade l'anandamide. L'IC50 de l'IDFP vaut 0,8 nM pour MAGL et 3,0 nM pour FAAH. L'inhibition de ces deux enzymes sans affecter l'AChE provoque l'augmentation du taux d'anandamide et de 2-AG dans le cerveau sans affecter celui d'acétylcholine, d'où l'apparition d'un comportement cannabinoïde sans symptômes cholinergiques chez les animaux étudiés[2],[3],[4],[5].
Bien qu'il ait une structure chimique semblable à celle de gaz innervants interdits, la longue chaîne alkyle de l'IDFP l'exclut de la définition des composés toxiques au titre de la Convention sur l'interdiction des armes chimiques[6], et comme il ne présente pas la même capacité à inhiber l'acétylcholinestérase que les composés organophosphorés apparentés, il ne fait pas l'objet de contrôles aussi stricts que ces derniers.
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Daniel K. Nomura, Jacqueline L. Blankman, Gabriel M. Simon, Kazutoshi Fujioka, Roger S. Issa, Anna M. Ward, Benjamin F. Cravatt et John E. Casida, « Activation of the endocannabinoid system by organophosphorus nerve agents », Nature Chemical Biology, vol. 4, no 6, , p. 373-378 (PMID 18438404, PMCID 2597283, DOI 10.1038/nchembio.86)
- (en) John E. Casida, Daniel K. Nomura, Sarah C. Vose et Kazutoshi Fujioka, « Organophosphate-sensitive lipases modulate brain lysophospholipids, ether lipids and endocannabinoids », Chemico-Biological Interactions, vol. 175, nos 1-3, , p. 355-364 (PMID 18495101, PMCID 2582404, DOI 10.1016/j.cbi.2008.04.008, lire en ligne)
- (en) Maxwell A. Ruby, Daniel K. Nomura, Carolyn S. S. Hudak, Lara M. Mangravite, Sally Chiu, John E. Casida et Ronald M. Krauss, « Overactive endocannabinoid signaling impairs apolipoprotein E-mediated clearance of triglyceride-rich lipoproteins », Proceedings of the National Academy of Sciences of the United States of America, vol. 105, no 38, , p. 14561-14566 (PMID 18794527, PMCID 2567196, DOI 10.1073/pnas.0807232105, lire en ligne)
- (en) Maxwell A. Ruby, Daniel K. Nomura, Carolyn S. S. Hudak, Anne Barber, John E. Casida et Ronald M. Krauss, « Acute Overactive Endocannabinoid Signaling Induces Glucose Intolerance, Hepatic Steatosis, and Novel Cannabinoid Receptor 1 Responsive Genes », PLoS ONE, vol. 6, no 11, , e26415 (PMID 22073164, PMCID 3208546, DOI 10.1371/journal.pone.0026415, lire en ligne)
- (en) Schedule 1.A. "Toxic chemicals" sur le site de l'Organisation pour l'interdiction des armes chimiques.
