Bocéprévir
Apparence
| Bocéprévir | |
| |
| Identification | |
|---|---|
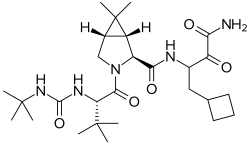
| Nom UICPA | (1R,2S,5S)-N-[(2Ξ)-4-amino-1-cyclobutyl-3,4-dioxobutan-2-yl)]- 3-{(2S)-2-[(tert-butylcarbamoyl)amino]-3,3-diméthylbutanoyl}- 6,6-diméthyl-3-azabicyclo[3.1.0]hexan-2-carboxamide |
| No CAS | |
| No ECHA | 100.226.246 |
| Code ATC | |
| PubChem | 10324367 |
| Propriétés chimiques | |
| Formule | C27H45N5O5 [Isomères] |
| Masse molaire[1] | 519,676 7 ± 0,027 3 g/mol C 62,4 %, H 8,73 %, N 13,48 %, O 15,39 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le bocéprévir est un inhibiteur de la protéase NS3/4A du virus de l'hépatite C de génotype 1 commercialisé en France sous le nom de Victrelis par les laboratoires MSD France depuis le [2].
Il est indiqué en association avec le peginterféron alfa et la ribavirine, chez le patient adulte atteint de maladie hépatique compensée, non préalablement traité ou en échec à un précédent traitement[3].
L’administration de bocéprevir est associée à la survenue d’une anémie chez un peu moins de la moitié des patients[4].
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Date de l'autorisation de mise sur le marché (AMM) européenne centralisée
- [PDF] Fiche HAS
- (en) Jensen DM, « A New era of hepatitis C therapy begins » N Engl J Med. 2011;364:1272-4.
- Cet article est partiellement ou en totalité issu de l'article intitulé « hépatite C » (voir la liste des auteurs).
