Vinylsilane
| Vinylsilane | |
| |
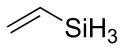
| Structure du vinylsilane | |
| Identification | |
|---|---|
| Nom UICPA | éthénylsilane |
| No CAS | |
| No ECHA | 100.027.926 |
| No CE | 230-719-7 |
| PubChem | 6327643 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C2H3Si |
| Masse molaire[1] | 55,130 7 ± 0,002 1 g/mol C 43,57 %, H 5,48 %, Si 50,94 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le vinylsilane est un composé chimique de formule CH2=CHSiH3. Ce dérivé organique du silane se présente sous la forme d'un gaz incolore dont l'intérêt est essentiellement théorique[2]. Ce sont surtout ses dérivés substitués sur l'atome de silicium qui sont utilisés. Les vinylsilanes sont notamment des intermédiaires utiles en synthèse organique[3]. En chimie des polymères et en science des matériaux, le vinyltriméthoxysilane CH2=CHSi(OCH3)3 et le vinyltriéthoxysilane CH2=CHSi(OCH2CH3)3 sont utilisés comme monomères et agents de couplage.
Les vinylsilanes sont souvent préparés par hydrosilylation d'alcynes. Ils peuvent être obtenus en faisant réagir des alcényl-lithium tels que le vinyllithium et des réactifs de Grignard avec des chlorosilanes. La silylation-déshydrogénation est une autre méthode de production des vinylsilanes[4].
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) M. A. Ring, H. E. O'Neal, S. F. Rickborn et B. A. Sawrey, « Kinetics of the high-temperature thermal decomposition of silanes and alkylsilanes », Organometallics, vol. 2, no 12, , p. 1891-1894 (DOI 10.1021/om50006a038, lire en ligne)
- (en) Ian Fleming, Jacques Dunoguès et Roger Smithers, « The Electrophilic Substitution of Allylsilanes and Vinylsilanes », Organic Reactions, (DOI 10.1002/0471264180.or037.02, lire en ligne)
- (en) Biao Lu et J. R. Falck, « Iridium-Catalyzed (Z)-Trialkylsilylation of Terminal Olefins », The Journal of Organic Chemistry, vol. 75, no 5, , p. 1701-1705 (PMID 20136153, PMCID 2830331, DOI 10.1021/jo902678p, lire en ligne)
