SN2
La substitution nucléophile bimoléculaire, ou communément appelée SN2 est un mécanisme réactionnel en chimie organique. C'est en fait un mécanisme limite, au sens où des réactions chimiques « naturelles » utilisant ce type de mécanisme ne se font jamais entièrement selon ce mécanisme, mais à un certain pourcentage. Le mécanisme limite « opposé » est la substitution nucléophile monomoléculaire ou SN1.
Cinétique de la réaction
[modifier | modifier le code]La réaction de substitution nucléophile bimoléculaire est appelée ainsi car il s'agit d'une réaction en 1 étape (on parle alors de réaction concertée), où 2 réactifs réagissent; elle a donc une cinétique de second ordre. L'expression de sa vitesse de réaction est donc la suivante :
Cette expression de la vitesse reste juste tant que le composé nucléophile reste dans des concentrations raisonnables. Si ce dernier est le solvant, dans le cas d'une solvolyse, on observe un comportement de pseudo premier ordre cinétique, due à la dégénérescence de l'ordre, c’est-à-dire une vitesse exprimée de la façon suivante :
Mécanisme réactionnel
[modifier | modifier le code]
Figure : les trois liaisons autour du carbone central sont coplanaires dans l'ET≠.
La substitution nucléophile bimoléculaire, ou SN2 est une réaction se faisant en une seule étape, sans intermédiaire réactionnel. L'atome X est plus électronégatif que le carbone auquel il est lié. Il capte les électrons de la liaison et dans un même temps, un groupe nucléophile — noté Nu — se lie au carbone, de l'autre côté du carbone central. On peut alors observer une inversion de la stéréochimie relative du carbone central, mais une conservation de la configuration absolue. C'est cette particularité qui fait de la réaction SN2 une réaction stéréospécifique. L'inversion citée précédemment est nommée « inversion de Walden ». Le postulat de Hammond permet de définir un état de transition — ET≠.
Stéréochimie
[modifier | modifier le code]La réaction de substitution nucléophile bimoléculaire, a contrario de la SN1, est à la fois stéréosélective, stéréospécifique et même énantiospécifique.
Attention : La configuration absolue n'est pas toujours changée par la SN2.
Influence de certains facteurs
[modifier | modifier le code]Influence du nucléofuge
[modifier | modifier le code]Deux facteurs doivent être pris en considération, la nucléophilie et la polarisabilité du nucléofuge (à noter que ces deux facteurs sont typiquement en corrélation : un bon nucléophile présente en général une polarisabilité élevée, puisque la déformation du nuage électronique est un des processus-clé de l'établissement de la nouvelle liaison chimique). L'électronégativité du nucléofuge est importante dans la mesure où elle détermine partiellement le caractère polaire du lien chimique R-X, lequel rend le substrat vulnérable aux attaques nucléophiles. Ainsi, on retrouvera les meilleurs nucléofuges à droite du tableau périodique (halogènes).
Cela dit, plus le nucléofuge sera polarisable, plus la réaction sera rapide[1]. Lorsqu'un nucléophile anionique s'approche de la "molécule cible", il y induira un dipôle plus aisément si le nucléofuge est polarisable. Typiquement, la polarisabilité d'un atome est corrélée avec le rayon de son nuage électronique. La taille d'un atome augmente au fur et à mesure que l'on descend dans une colonne du tableau périodique.
Parmi les halogènes, on peut classer la nucléofugacité comme ceci :
Ainsi, l'iode est un meilleur nucléofuge que le chlore grâce à sa plus grande polarisabilité. De même l'ordre de nucléophilie est en général identique[2].
Par conséquent l'ordre de nucléophilie est inversement proportionnelle à l'electronégativité.
Influence du nucléophile
[modifier | modifier le code]De manière simple et évidente, plus le nucléophile — — sera polarisable, et plus la SN2 sera rapide et favorisée, cinétiquement parlant.
Influence du solvant
[modifier | modifier le code]De façon similaire à l'influence du nucléophile, un solvant polaire stabiliserait le composé nucléophile, c'est pourquoi la SN2 sera favorisée dans un solvant peu polaire et aprotique — solvant ne créant pas de liaisons hydrogène. Par contre, un solvant polaire sera souvent nécessaire afin de dissoudre le nucléophile[3], tel que le THF (tétrahydrofurane), l'ACN (acétonitrile), le DMF (diméthylformamide) ou le DMSO (diméthylsulfoxyde), qui sont les exemples les plus fréquemment utilisés en laboratoire, mais d'autres solvants peuvent être utilisés.
"L'eau est un solvant extrêmement polaire, et donc inappropriée pour une SN2..."
Influence du groupement alkyle
[modifier | modifier le code]On observe des réactivités et des vitesses différentes suivant la classe du réactif. En effet, la possibilité de l'inversion de Walden, développée précédemment, est tributaire de la gêne stérique provoquée par les chaines liées au carbone central. On introduit donc les classes suivantes de composés :

La SN2 sera favorisée pour un réactif primaire. Et fortement défavorisée pour un composé tertiaire : en effet les chaines R1, R2 et R3 proposent une gêne importante du côté d'attaque du nucléophile, l'état de transition est haut en énergie et peut être impossible à atteindre, les produits ne peuvent alors pas se former. On ne peut pas statuer a priori sur le sort du composé secondaire, la réaction pouvant ou non se produire selon les conditions expérimentales.
Exemple de SN2
[modifier | modifier le code]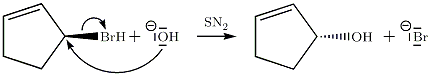
Cet exemple montre que le produit d'une molécule chirale par une SN2 est une molécule chirale.
Références
[modifier | modifier le code]- Eric Anslyn and Dennis Dougherty (2006) Modern Physical Organic Chemistry, 1098 pp.
- Clayden, Greeves, Warren and Wothers (2000) Organic Chemistry, 1536 pp., voir page 439.
- http://users.wfu.edu/wrightmw/chm122/handouts/Solvent%20and%20SN1SN2%20summary.pdf
4. Marine PEUCHMAUR Cours de Chimie Organique chapitre 6 page 7. http://unf3s.cerimes.fr/media/paces/Grenoble_1112/peuchmaur_marine/peuchmaur_marine_p06/peuchmaur_marine_p06.pdf

![{\displaystyle v=k\left[\mathrm {RX} \right]\left[Nu\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/56ccf41e39528568010649cfddaab4a91eaa594e)
![{\displaystyle v^{\prime }=k^{\prime }\left[\mathrm {RX} \right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/34a94e2dd5b5dc41b45753607aaf8401e5c48610)

