MCPA
| MCPA | |||
| |||
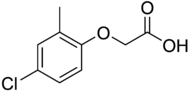
| Structure de la molécule de MCPA | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | acide (4-chloro-2-méthylphénoxy)acétique | ||
| Synonymes |
acide 4-chloro-o-tolyloxyacétique |
||
| No CAS | |||
| No ECHA | 100.002.146 | ||
| No CE | 202-360-6 | ||
| No RTECS | AG1575000 | ||
| PubChem | |||
| ChEBI | 50099 | ||
| SMILES | |||
| InChI | |||
| Apparence | poudre cristalline jaunâtre d'odeur phénolique[1] | ||
| Propriétés chimiques | |||
| Formule | C9H9ClO3 [Isomères] |
||
| Masse molaire[3] | 200,619 ± 0,011 g/mol C 53,88 %, H 4,52 %, Cl 17,67 %, O 23,93 %, |
||
| pKa | 3,13 à 25 °C[2] | ||
| Propriétés physiques | |||
| T° fusion | 120 °C[1],[2] 114 à 118 °C[4] |
||
| T° ébullition | 286,74 °C[2] | ||
| Solubilité | eau : 300 mg·l-1 à 25 °C[1] 630 mg·l-1 à 25 °C[2] |
||
| Masse volumique | 1,56 g·cm-3[1] | ||
| Pression de vapeur saturante | 5,9 × 10−6 mmHg à 25 °C[2] | ||
| Précautions | |||
| SGH[1],[4] | |||
| H302, H315, H318, H410, P273, P280, P305+P351+P338 et P501 |
|||
| Transport[1],[4] | |||
|
|||
| Écotoxicologie | |||
| DL50 | 439 mg/kg (souris, oral)[2] 700 mg/kg (rat, oral)[2] 700 mg/kg (cochon d'Inde, oral)[2] 28 mg/kg (souris, s.c.)[2] 28 mg/kg (souris, i.v.)[2] |
||
| LogP | 3,25 (octanol/eau)[2] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Le MCPA, ou acide 2-méthyl-4-chlorophénoxyacétique, est un composé organique utilisé comme substance active d'herbicide. C'est un herbicide sélectif, puissant et très largement utilisé de la famille des herbicides phénoxys. Le composé pur se présente sous la forme d'une poudre de couleur brune.
Histoire
[modifier | modifier le code]Les premières recherches ont commencé en 1936 au centre de recherche ICI de Jealott's Hill sur les effets des auxines (hormones végétales) sur la croissance des plantes. Il s'agissait de trouver un moyen de tuer les mauvaises herbes sans nuire à des cultures telles que le maïs[5].
La synthèse du MCPA fut d'abord rapportée par Synerholme et Zimmerman en 1945 puis par Templeman et Foster en 1946[6]. Templeman et Foster recherchaient des composés chimiques ayant une activité sélective similaire ou supérieure à celle de l'acide 1-naphtalène-acétique pour inhiber la croissance des mauvaises herbes sans affecter négativement celle des céréales. Ils ont synthétisé le MCPA à partir du phénol correspondant en le faisant réagir avec l'acide chloroacétique et une base diluée dans une réaction de substitution simple[7] :
- 2-méthyl-4-chlorophénol + ClCH2CO2H + base → MCPA + base·HCl
Utilisation commerciale
[modifier | modifier le code]Le MCPA est utilisé comme herbicide, généralement sous forme de sels ou d'esters. Ainsi utilisé, il permet de maîtriser les mauvaises herbes dicotylédones , y compris les chardons et les oseilles, dans les cultures de céréales et les pâturages. Il est sélectif contre les plantes à feuilles larges, y compris la plupart des arbres à feuilles caduques. Les trèfles sont tolérants à des doses d'application modérées.
Il est actuellement classé comme un pesticide à usage restreint aux États-Unis. Sa toxicité et sa biodégradation sont des sujets de recherche en cours. Une formulation est ainsi décrite par son fabricant comme « conçue pour des marchés spécifiques qui nécessitent le produit phénoxy le plus sûr possible, principalement pour une utilisation dans la région du Pacifique Nord-Ouest »[8] Bien qu'il ne soit pas extrêmement toxique[9], on a récemment déterminé que le MCPA peut former des complexes avec des ions métalliques et ainsi augmenter leur biodisponibilité[10], et des recherches sont en cours pour utiliser cette possibilité[11].
Utilisation en chimie
[modifier | modifier le code]Parce qu'il est bon marché, le MCPA est utilisé dans diverses applications chimiques. Son groupe acide carboxylique permet la formation de complexes conjugués avec des métaux (voir ci-dessus). La fonction acide fait du MCPA un intermédiaire de synthèse polyvalent pour obtenir des dérivés plus complexes[12].
Marques commerciales
[modifier | modifier le code]Les produits commerciaux suivants contiennent du MCPA[9] :
- Agritox, Agroxone, Chiptox, Chwastox, Cornox, Methoxone, Rhonox, Spurge Power, Tigrex, Verdone Extra (Royaume-Uni), Weed-Rhap, Weed'n'Feed, Weed-B-Gone, Zero Bindii & Clover Weeder (Australie), Jolt (Australie), Maatilan MCPA, K-MCPA, Hedonal, Basagran (Finlande), etc.
Notes et références
[modifier | modifier le code]- Entrée « Pentafluoroethane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais) (JavaScript nécessaire)
- (en) « MCPA », sur ChemIDplus.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé MCPA, consultée le 08/04/2011.
- (en) « Imperial Chemical Industries Limited: Display Advertising », The Times, .
- (en) S. Budaver, éd., Merck Index (11e éd.), Merck & Co, Inc., .
- (en) W.G. Templeman, W.A. Sexton, « The Differential Effect of Synthetic Plant Growth Substances upon Plant Species. I. Seed Germination and Early Growth Responses to α-Naphthylacetic Acid and Compounds of General Formula arylOCHCOO », Proceedings of the Royal Society of London, vol. 133, no 872, , p. 300–313 (DOI 10.1098/rspb.1946.0014).
- (en) « Chiptox », Nufarm.
- (en) « Extoxnet listing of MCPA » (consulté le ).
- (en) J. Kobylecka, B. Ptaszynski, R. Rogaczewski, A. Turek, « Phenoxyalkanoic acid complexes. Part I. Complexes of lead(II), cadmium(II) and copper(II) with 4-chloro-2-methylphenoxyacetic acid (MCPA) », Thermochimica Acta, vol. 407, nos 1-2, , p. 25–31 (DOI 10.1016/S0040-6031(03)00287-9).
- (en) R. Kruszynski, T.J. Bartczak, B. Ptaszynski et A. Turek, « A Novel Lead- bis (4-Chloro-2-Methylphenoxy)- Acetate Polymeric Complex », Journal of Coordination Chemistry, vol. 55, no 9, , p. 1079–1089 (DOI 10.1080/0095897021000010035).
- (en) A. R. Prasad, T. Ramalingam, A. B. Rao, P. V. Diwan et P. B. Sattur, « Synthesis and biological evaluation of 3-aryloxyalkyl-6-aryl-7H-s-triazolo3,4-b 1,3,4thiadiazines », European Journal of Medicinal Chemistry, vol. 25, no 2, , p. 199–201 (DOI 10.1016/0223-5234(89)90116-5).




