ICAM-1
ICAM-1 (de l'anglais : InterCellular Adhesion Molecule) ou CD54 est une protéine codée par le gène ICAM1 chez l'humain situé sur le chromosome 19 humain. Elle est présente à la surface des cellules endothéliales et des lymphocytes. Elle peut servir de récepteur aux virus du genre rhinovirus.
Structure
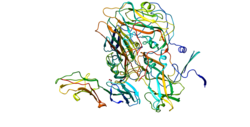
[modifier | modifier le code]ICAM-1 appartient à la superfamille des immunoglobulines, qui comprend les anticorps, les récepteurs des cellules B (BCR) et les récepteurs des cellules T (TCR). ICAM-1 est une glycoprotéine transmembranaire possédant un seul domaine transmembranaire. Sa structure est caractérisée par une forte glycosylation et un domaine extracellulaire composé de nombreuses boucles créées par les ponts disulfure de la protéine. La structure secondaire dominante de la protéine est le feuillet bêta, ce qui conduit les chercheurs à émettre l'hypothèse de la présence de domaines de dimérisation au sein de l'ICAM-1.
Fonction
[modifier | modifier le code]La protéine codée par ce gène est un type de molécule d'adhésion intercellulaire continu présente en faible concentration dans les membranes des leucocytes et les cellules endothéliales . Lors de la stimulation des cytokines, les concentrations augmentent considérablement. Lorsqu'il est activé, les leucocytes se lient aux cellules endothéliales via ICAM-1 / LFA-1, puis transmigrent dans les tissus.
Cible thérapeutique
[modifier | modifier le code]Le lifitegrast est un antagoniste du LFA-1 empêchant son interaction avec l'ICAM-1 et en cours de test dans la sécheresse oculaire.
Interactions
[modifier | modifier le code]Il a été montré qu'ICAM-1 interagit avec :
Notes et références
[modifier | modifier le code]- GRCh38: Ensembl release 89: ENSG00000090339 - Ensembl, May 2017
- GRCm38: Ensembl release 89: ENSMUSG00000037405 - Ensembl, May 2017
- « Publications PubMed pour l'Homme », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- « Publications PubMed pour la Souris », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- Lu C, Takagi J, Springer TA, « Association of the membrane proximal regions of the alpha and beta subunit cytoplasmic domains constrains an integrin in the inactive state », The Journal of Biological Chemistry, vol. 276, no 18, , p. 14642–48 (PMID 11279101, DOI 10.1074/jbc.M100600200)
- Shimaoka M, Xiao T, Liu JH, Yang Y, Dong Y, Jun CD, McCormack A, Zhang R, Joachimiak A, Takagi J, Wang JH, Springer TA, « Structures of the alpha L I domain and its complex with ICAM-1 reveal a shape-shifting pathway for integrin regulation », Cell, vol. 112, no 1, , p. 99–111 (PMID 12526797, DOI 10.1016/S0092-8674(02)01257-6)
- Yusuf-Makagiansar H, Makagiansar IT, Hu Y, Siahaan TJ, « Synergistic inhibitory activity of alpha- and beta-LFA-1 peptides on LFA-1/ICAM-1 interaction », Peptides, vol. 22, no 12, , p. 1955–62 (PMID 11786177, DOI 10.1016/S0196-9781(01)00546-0)
- Heiska L, Alfthan K, Grönholm M, Vilja P, Vaheri A, Carpén O, « Association of ezrin with intercellular adhesion molecule-1 and -2 (ICAM-1 and ICAM-2). Regulation by phosphatidylinositol 4, 5-bisphosphate », The Journal of Biological Chemistry, vol. 273, no 34, , p. 21893–900 (PMID 9705328, DOI 10.1074/jbc.273.34.21893)
- Kotovuori A, Pessa-Morikawa T, Kotovuori P, Nortamo P, Gahmberg CG, « ICAM-2 and a peptide from its binding domain are efficient activators of leukocyte adhesion and integrin affinity », Journal of Immunology, vol. 162, no 11, , p. 6613–20 (PMID 10352278)
- Huang C, Springer TA, « A binding interface on the I domain of lymphocyte function-associated antigen-1 (LFA-1) required for specific interaction with intercellular adhesion molecule 1 (ICAM-1) », The Journal of Biological Chemistry, vol. 270, no 32, , p. 19008–16 (PMID 7642561, DOI 10.1074/jbc.270.32.19008)