Acide asparagusique
| Acide asparagusique | |
  |
|
| Identification | |
|---|---|
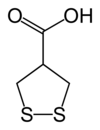
| Nom UICPA | acide 1,2-dithiolane-4-carboxylique |
| No CAS | |
| PubChem | 16682 |
| SMILES | |
| InChI | |
| Apparence | solide incolore |
| Propriétés chimiques | |
| Formule | C4H6O2S2 [Isomères] |
| Masse molaire[1] | 150,219 ± 0,014 g/mol C 31,98 %, H 4,03 %, O 21,3 %, S 42,69 %, |
| Propriétés physiques | |
| T° fusion | 75,7 à 76,5 °C[2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L’acide asparagusique, S2(CH2)2CHCO2H est un acide carboxylique organo-sulfuré présent, lui et son ester de méthyle, dans l’asperge[3]. Il consiste en une fonction acide carboxylique branchée en 4 d'un cycle 1,2-dithiolane. C'est un métabolite du thiopropénoate de méthyle et du 3-(thiométhyl)thiopropanoate de méthyle qui serait responsable de l'augmentation de l'odeur de l'urine après la consommation d'asperge[4].
-
thiopropénoate de méthyle
-
3-(thiométhyl)thiopropanoate de méthyle
Les études montrent que cet acide est un dérivé de l’acide isobutyrique[5]. Ce solide incolore a une température de fusion de 75.7-76.5 °C[2]. Le dithiol associé est aussi connu (température de fusion 59.5-60.5 °C)[6], il est appelé acide dihydroasparagusique ou acide dimercaptoisobutyrique.
Extraction
[modifier | modifier le code]Jansen (1948) a obtenu à partir de 40 kg de concentré d'arôme d'asperge 32 g d'un composé identifié comme l'acide 3,3’-dimercaptoisobutyrique[7].
Synthèse
[modifier | modifier le code]L'acide asparagusique peut être synthétisé à partir de l'acide 3,3'-dichloroisobutyrique et du disulfure de sodium (formé in situ à partir du sulfure de sodium et de soufre) :
Dégradation
[modifier | modifier le code]Chauffé (par exemple lors de la cuisson des asperges), l'acide asparagusique se décompose en acide 1,2,3-trithiane-5-carboxylique et en 1,2-dithiole:
Notes et références
[modifier | modifier le code]- (en)/(de) Cet article est partiellement ou en totalité issu des articles intitulés en anglais « Asparagusic acid » (voir la liste des auteurs) et en allemand « Asparagusinsäure » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Foss, Olav; Tjomsland, Olav, « Crystal and molecular structure of 1,2-dithiolane-4-carboxylic acid », Acta Chemica Scandinavica, vol. 12, , p. 1810–18 (DOI 10.3891/acta.chem.scand.12-1810)
- (en) S.C. Mitchell, « Food Idiosyncrasies: Beetroot and Asparagus », Drug Metabolism and Disposition, vol. 29, no 4 Pt 2, , p. 539–534 (PMID 11259347, lire en ligne, consulté le )
- (de) Römpp CD 2006, Georg Thieme Verlag 2006
- (en) R. J. Parry, A. E. Mizusawa, I. C. Chiu, M. V. Naidu, and M. Ricciardone, « Biosynthesis of Sulfur Compounds. Investigations of the Biosynthesis of Asparagusic Acid », Journal of the American Chemical Society, vol. 107, no 8, , p. 2512–2521 (DOI 10.1021/ja00294a051)
- (en) R. Singh, G. M. Whitesides, « Comparisons of Rate Constants for Thiolate-Disulfide Interchange in Water and in Polar Aprotic Solvents Using Dynamic 'H NMR Line Shape Analysis », J. Am. Chem. Soc., vol. 112, no 3, , p. 1190–1197 (DOI 10.1021/ja00159a046)
- (en) Jansen, E. F., « The isolation and identification of 2,2’-dithiolisobutyric acid from asparagus », Journal of Biological Chemistry, vol. 176, no 2, , p. 657–664 (PMID 18889921)



