« Pyrolyse d'ester » : différence entre les versions
orthographe |
m v1.41 - Lien magique ISBN obsolète - Catégorie:Pages utilisant des liens magiques ISBN |
||
| Ligne 1 : | Ligne 1 : | ||
La '''pyrolyse d'ester''' est une [[réaction organique]] de type [[pyrolyse]] sous vide convertissant les [[ester]]s contenant une [[hydrogène β]] en [[acide carboxylique]] correspondant et en [[alcène]]; Elle ne fonctionne donc pas par exemple pour les esters de méthyle<ref name=Hauptmann>[[Siegfried Hauptmann]]: ''Reaktion und Mechanismus in der organischen Chemie'', B. G. Teubner, Stuttgart, 1991, S. 130, ISBN |
La '''pyrolyse d'ester''' est une [[réaction organique]] de type [[pyrolyse]] sous vide convertissant les [[ester]]s contenant une [[hydrogène β]] en [[acide carboxylique]] correspondant et en [[alcène]]; Elle ne fonctionne donc pas par exemple pour les esters de méthyle<ref name=Hauptmann>[[Siegfried Hauptmann]]: ''Reaktion und Mechanismus in der organischen Chemie'', B. G. Teubner, Stuttgart, 1991, S. 130, {{ISBN|3-519-03515-4}}.</ref>. |
||
:[[Image:Esterpyrolyse 1c.svg]] |
:[[Image:Esterpyrolyse 1c.svg]] |
||
Une réaction produisant le même type de produits, dans des conditions plus douces est la [[réaction de Tschugajew]]<ref name=Laue>T. Laue und A. Plagens: ''Namens- und Schlagwort-Reaktionen der Organischen Chemie'', 5. Auflage, Teubner Studienbücher Chemie, 2006, S. 119, ISBN |
Une réaction produisant le même type de produits, dans des conditions plus douces est la [[réaction de Tschugajew]]<ref name=Laue>T. Laue und A. Plagens: ''Namens- und Schlagwort-Reaktionen der Organischen Chemie'', 5. Auflage, Teubner Studienbücher Chemie, 2006, S. 119, {{ISBN|3-8351-0091-2}}.</ref>. |
||
== Mécanisme == |
== Mécanisme == |
||
Version du 2 janvier 2017 à 00:55
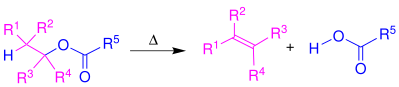
La pyrolyse d'ester est une réaction organique de type pyrolyse sous vide convertissant les esters contenant une hydrogène β en acide carboxylique correspondant et en alcène; Elle ne fonctionne donc pas par exemple pour les esters de méthyle[1].
Une réaction produisant le même type de produits, dans des conditions plus douces est la réaction de Tschugajew[2].
Mécanisme
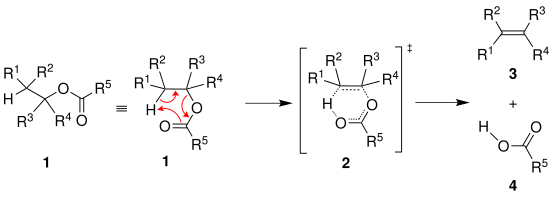
La pyrolyse de l'ester (1) suit mécanisme réactionnel d'élimination Ei, et un donc un exemple d'élimination syn. La réaction est en une étape, avec en état de transition un pseudo-cycle à six (2) ; le groupe alkyle donne son hydrogène en β au groupe carboxyle, dans une réaction concertée ou le doublet libre se rabat sur la liaison carbone-carbone, le doublet formant la liaison carbone-oxygène se rabattant sur pour forer un groupe carboxyle. Le résultat est donc un alcène (3) est un acide carboxylique (4)[2].
Exemples
On peut citer comme exemples la synthèse de l'acide acrylique par pyrolyse de l'acrylate d'éthyle à 590 °C[3], la synthèse du penta-1,4-diène à partir du diacétate de pentane-1,5-diol à 575 °C[4] ou encore la construction d'un assemblage de cyclobutène à 700 °C[5].
Notes et références
- Siegfried Hauptmann: Reaktion und Mechanismus in der organischen Chemie, B. G. Teubner, Stuttgart, 1991, S. 130, (ISBN 3-519-03515-4).
- T. Laue und A. Plagens: Namens- und Schlagwort-Reaktionen der Organischen Chemie, 5. Auflage, Teubner Studienbücher Chemie, 2006, S. 119, (ISBN 3-8351-0091-2).
- Organic Syntheses, Coll. Vol. 3, p.30 (1955); Vol. 29, p.2 (1949). Link
- Organic Syntheses, Coll. Vol. 4, p.746 (1963); Vol. 38, p.78 (1958). Link
- Organic Syntheses, Coll. Vol. 5, p.235 (1973); Vol. 43, p.17 (1963). Link
- (en)/(de) Cet article est partiellement ou en totalité issu des articles intitulés en anglais « Ester pyrolysis » (voir la liste des auteurs) et en allemand « Esterpyrolyse » (voir la liste des auteurs).