Scatol
| Scatol | |
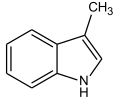  Structure du scatol. |
|
| Identification | |
|---|---|
| Nom UICPA | 3-méthyl-1H-indole |
| Synonymes |
4-méthyl-2,3-benzopyrrole |
| No CAS | |
| No ECHA | 100.001.338 |
| No CE | 201-471-7 |
| PubChem | 6736 |
| ChEBI | 9171 |
| SMILES | |
| InChI | |
| Apparence | cristaux blancs solides |
| Propriétés chimiques | |
| Formule | C9H9N [Isomères] |
| Masse molaire[2] | 131,174 5 ± 0,008 g/mol C 82,41 %, H 6,92 %, N 10,68 %, |
| pKa | -3.4 [1] |
| Propriétés physiques | |
| T° fusion | 97,5 °C [1] |
| T° ébullition | 266 °C [1] |
| Solubilité | 498 mg·l-1 (eau, 25 °C) [1] |
| Écotoxicologie | |
| DL50 | 3 450 mg·kg-1 (rat, oral) 175 mg·kg-1 (souris, i.p.) [1] |
| LogP | 2,6 [1] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le scatol - également orthographié scatole - ou 3-méthylindole est un composé organique légèrement toxique se présentant sous la forme d'un cristal blanc et appartenant à la famille des indoles. Il est naturellement présent dans les excréments (c'est un métabolite du tryptophane dans le tube digestif des mammifères) ainsi que dans le goudron de houille et a une forte odeur fécale. À faible concentration, il a une odeur florale que l'on retrouve dans plusieurs plantes et huiles essentielles, parmi lesquelles la fleur d'oranger, le jasmin, et le jujubier. Il est utilisé comme fragrance et fixateur dans de nombreux parfums ainsi que comme composé aromatique. Son nom est dérivé de la racine grecque skatos (génitif du mot σκώρ ou σκῶρ, σκατός), signifiant "excrément".
Propriétés physico-chimiques[modifier | modifier le code]
Le scatol peut être isolé sous forme de cristaux blancs ou d'une fine poudre solide, et il brunit en vieillissant. C'est un composé azoté qui possède un cycle pyrrole. Soluble dans l'alcool et le benzène, il donne une couleur violette dans le ferrocyanure de potassium et l'acide sulfurique. Le scatol possède le noyau aromatique caractéristique des hydrocarbures aromatiques. Sa structure est continue (tous les atomes sont hybridés sp²), plane, et respecte la règle 4n+2 car elle possède 10 électrons p. La molécule peut être synthétisée par la synthèse de Fischer de l'indole, mise au point par Emil Fischer[3].
Effet attractif sur les insectes[modifier | modifier le code]
Le 3-méthylindole est une substance attractive pour les moustiques femelles gravides, comme cela a été démontré aussi bien en laboratoire que sur le terrain[4]. Elle attire également les insectes coprophages pollinisateurs des fleurs cadavres d'Arums[5]. Comme ce composé est présent dans les fèces, on le retrouve dans les réseaux unitaires d'assainissement, les cours d'eau et les lacs recevant des déjections humaines et animales non-traitées. Cette attractivité représente un intérêt particulier pour l'étude des maladies dont les moustiques sont vecteurs, telles que la fièvre du Nil occidental par exemple[6].
Toxicologie[modifier | modifier le code]
Le scatol est une pneumotoxine qui affecte la synthèse des phospholipides nécessaires pour la production membranaire, comme cela a été vérifié sur des chèvres[7], des moutons, des rats, et certaines souches de souris[8]. Il cible sélectivement les pneumocytes de type I et les cellules de Clara, qui sont le principal site des enzymes du cytochrome P450 dans les poumons. Ces enzymes oxydent le scatol en intermédiaires réactifs, dont le 3-méthylèneindolénine, qui endommagent les cellules en formant des protéines combinées[9]. Chez les bovins, un changement brutal de pâturage peut provoquer une intoxication au 3-méthylindole ruminal, appelée emphysème des regains[10] (fog fever en anglais).
Dans un rapport émis en 1994 par cinq importants fabricants de cigarettes, le scatol faisait partie des 599 additifs listés[11] et soumis à l'approbation du département de la Santé et des Services sociaux des États-Unis (United States Department of Health and Human Services). Il y apparaît comme agent aromatique.
Le scatol est urticant et ainsi interdit en France.
Agroalimentaire[modifier | modifier le code]
Le scatol est l'une des deux substances incriminées dans l'odeur de verrat, une odeur désagréable qui se dégage parfois lors de la cuisson de la viande de porc.
Notes et références[modifier | modifier le code]
- (en) « Scatol », sur ChemIDplus, consulté le 20 décembre 2010
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- La synthèse est décrite dans le Guide de préparations organiques à l’usage des étudiants de Fischer, disponible sur Wikisource : Guide de préparations organiques à l’usage des étudiants.
- (en) Schiestl, F.P. & Roubik, D.W., « Odor Compound Detection in Male Euglossine Bees », Journal of Chemical Ecology, vol. 29, no 1, , p. 253–257 (PMID 12647866, DOI 10.1023/A:1021932131526, lire en ligne)
- (en) B.N. Smith & B.J.D. Meeuse, « Production of volatile amines and skatole at anthesis in some Arum lily species », Plant Physiology, vol. 41, no 2, , p. 343-347.
- (en) Beechler, J W., J G Miller, and M S Mulla, « Field evaluation of synthetic compounds mediating oviposition in Culex mosquitoes (Diptera: Culicidae) », J Chem Ecol,
- (en) Stan Kubow et Tammy M. Bray, The effect of lung concentrations of glutathione and vitamin E on the pulmonary toxicity of 3-methylindole, Canadian Journal of Physiologie and Pharmacologie, 66(7): 863–867 (1988)
- (en) M Miller, « 3-Methylindole Induces Transient Olfactory Mucosal Injury in Ponies », Veterinary Pathology, vol. 40, no 4, , p. 363–70 (PMID 12824507, DOI 10.1354/vp.40-4-363)
- Guillaume Belbis, Flore du rumen : origine, composition, évolution, conséquences physiopathologiques, École Nationale Vétérinaire d’Alfort (thèse de doctorat vétérinaire), Nancy, 2007, 140 p.
- Institut de l'élevage (collectif), Maladies des bovins, Paris, France Agricole, coll. « Manuel pratique », , 797 p. (ISBN 978-2-85557-149-2, lire en ligne), p. 228
- Liste d'additifs dans les cigarettes
