Cyclotrivératrylène
| Cyclotrivératrylène | |
 Structure du cyclotrivératrylène |
|
| Identification | |
|---|---|
| Synonymes |
2,3,7,8,12,13-hexaméthoxy-10,15-dihydro-5h-tribenzo[a,d,g]cyclononène |
| No CAS | |
| PubChem | 273730 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C27H30O6 |
| Masse molaire[1] | 450,523 5 ± 0,025 5 g/mol C 71,98 %, H 6,71 %, O 21,31 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
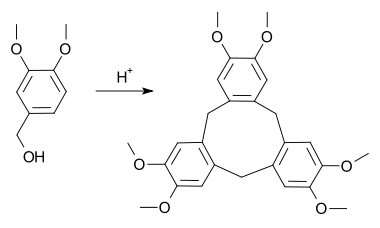
Le cyclotrivératrylène (CTV) est un composé organique macrocyclique apparenté aux calixarènes et utilisé comme hôte moléculaire en chimie hôte-invité[2]. Sa première synthèse a été réalisée en 1915 par Gertrude Robinson, première épouse du chimiste britannique Robert Robinson[3], qui l'avait cependant identifié au dimère et non au trimère. Sa structure correcte a été déterminée en 1963 par Lindsey[4], qui a nommé ce composé cyclotrivératrylène. Il peut être produit à partir d'alcool de vératryle par substitution électrophile aromatique de l'acide approprié, qui peut être l'acide perchlorique, l'acide formique ou l'acide sulfurique dans l'acide acétique.
Il existe une voie de synthèse alternative à partir du vératrole et du formaldéhyde.
Les groupes éther sont situés sur le bord supérieur. Le CTV a une conformation en forme de bol comme un éther couronne. Ses dérivés sont connus pour se lier aux fullerènes et l'on a pu démonter l'utilisation de CTV dans la séparation de mélange de fullerènes. Ces dérivés sont également connus pour former des cristaux liquides et sont utilisés comme unités structurelles pour la constitution de polymères et de réseaux de polymères (gels). Le CTV peut former, avec des complexes métalliques appropriés, des polymères ou des oligomères métallo-supramoléculaires.
La liaison de deux unités de CTV par trois espaceurs moléculaires donne des cryptophanes, qui sont des composés formant des cages moléculaires utilisés pour l'encapsulation (en).
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Michaele J. Hardie, « Recent advances in the chemistry of cyclotriveratrylene », Chemical Society Reviews, vol. 39, no 2, , p. 516-527 (lire en ligne) DOI 10.1039/B821019P
- (en) Gertrude Maud Robinson, « XXX.—A reaction of homopiperonyl and of homoveratryl alcohols », Journal of the Chemical Society, Transactions, vol. 107, , p. 267-276 (lire en ligne) DOI 10.1039/CT9150700267
- (en) A. S. Lindsey, « 316. The structure of cyclotriveratrylene (10,15-dihydro-2,3,7,8,12,13-hexamethoxy-5H-tribenzo[a,d,g]cyclononene) and related compounds », Journal of the Chemical Society (Resumed), no 0, , p. 1685-1692 (lire en ligne) DOI 10.1039/JR9650001685