Oxyde de vanadium(V)
| Pentoxyde de vanadium | |||

| |||
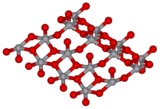 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | Oxyde de Vanadium (V) | ||
| Synonymes |
Pentoxyde de vanadium |
||
| No CAS | |||
| No ECHA | 100.013.855 | ||
| No CE | 215-239-8 | ||
| SMILES | |||
| InChI | |||
| Apparence | poudre cristalline jaune à rouge ou solide de formes variables[1]. | ||
| Propriétés chimiques | |||
| Formule | V2O5 | ||
| Masse molaire[2] | 181,88 ± 0,001 7 g/mol O 43,98 %, V 56,02 %, |
||
| Propriétés physiques | |||
| T° fusion | 690 °C[1] | ||
| T° ébullition | (décomposition) : 1 750 °C[1] | ||
| Solubilité | dans l'eau : 8 g·l-1[1] | ||
| Masse volumique | 3,4 g·cm-3[1] | ||
| Précautions | |||
| SGH[4] | |||
| H302, H332, H335, H341, H361d, H372 et H411 |
|||
| Transport | |||
|
|||
| Classification du CIRC | |||
| Groupe 2B : Peut-être cancérogène pour l'homme[3] | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
L'oxyde de vanadium(V) ou pentoxyde de vanadium (V2O5) est la forme la plus oxydée du vanadium. On s'en sert comme catalyseur souvent sur un support d'alumine.
Il est utilisé dans la synthèse de l'acide sulfurique où il catalyse l'oxydation du dioxyde de soufre en trioxyde.
Voir aussi
Références
- PENTAOXYDE DE DIVANADIUM, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 2B : Peut-être cancérogènes pour l'homme », sur http://monographs.iarc.fr, CIRC, (consulté le )
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)



