Diméthyldichlorosilane
| Diméthyldichlorosilane | |
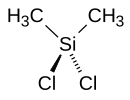  Structure du diméthyldichlorosilane |
|
| Identification | |
|---|---|
| Nom UICPA | dichloro(diméthyl)silane |
| Synonymes |
dichlorodiméthylsilane |
| No CAS | |
| No ECHA | 100.000.820 |
| No CE | 200-901-0 |
| PubChem | 6398 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore et volatil d'odeur piquante |
| Propriétés chimiques | |
| Formule | C2H6Cl2Si [Isomères] |
| Masse molaire[1] | 129,061 ± 0,006 g/mol C 18,61 %, H 4,69 %, Cl 54,94 %, Si 21,76 %, |
| Propriétés physiques | |
| T° fusion | −86 °C[2] |
| T° ébullition | 70 °C[2] |
| Solubilité | décomposition brutale au contact de l'eau |
| Masse volumique | 1,06 g·cm-3[2] |
| T° d'auto-inflammation | 425 °C[2] |
| Point d’éclair | −12 °C[2] |
| Pression de vapeur saturante | 15 kPa[2] à 20 °C |
| Précautions | |
| SGH[2] | |
| H225, H315, H319, H335, P210, P302+P352 et P305+P351+P338 |
|
| Transport[2] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le diméthyldichlorosilane est un composé chimique de formule SiCl2(CH3)2. Il s'agit d'un gaz incolore, volatil et très inflammable, d'odeur piquante. Il se décompose brutalement au contact de l'eau pour former des chaînes linéaires et cycliques où alternent les atomes de silicium et d'oxygène. Il est produit industriellement essentiellement comme précurseur de polysilanes et de silicones (polysiloxanes).
Production

La production de diméthyldichlorosilane est réalisée industriellement à l'aide de la synthèse de Müller-Rochow, ou synthèse directe, qui consiste à faire passer du chlorométhane CH3Cl à travers du silicium finement divisé et du chlorure de cuivre(I) CuCl dans un réacteur à lit fluidisé à environ 300 °C[3] :
Ce procédé produit environ 80 à 90 % de diméthyldichlorosilane SiCl2(CH3)2, mais aussi 5 à 15 % de méthyltrichlorosilane SiCl3CH3, 3 à 5 % de méthyldichlorosilane SiHCl2CH3 et 3 à 5 % de chlorure de triméthylsilyle SiCl(CH3)3. Ces composés sont ensuite séparés par distillation fractionnée, leur température d'ébullition étant respectivement de 70,0 °C, 65,7 °C, 40,7 °C et 57,3 °C[4].
Réactions
Au contact de l'eau, le diméthyldichlorométhane s'hydrolyse pour former des silicones linéaires et cycliques. La longueur des polymères formés de cette manière dépend de la concentration en groupes terminaux ajoutés au mélange. La vitesse de la réaction est déterminée par la vitesse de transfert des réactifs à travers l'interface entre les phases aqueuses et organiques, de sorte qu'elle est accélérée en conditions turbulentes. Le milieu réactionnel peut également être adapté afin d'optimiser le rendement des produits recherchés :
- n SiCl2(CH3)2 + n H2O → [–Si(CH3)2–O–]n + 2n HCl(aq).
- m SiCl2(CH3)2 + (m+1) H2O → HO[–Si(CH3)2–O–]mH + 2m HCl(aq).
Le diméthyldichlorosilane réagit avec le méthanol CH3OH pour donner du diméthoxydiméthylsilane :
Bien que l'hydrolyse du diméthoxydiméthylsilane soit plus lente, elle est préférée lorsque la formation d'acide chlorhydrique HCl(aq) n'est pas souhaitée :
- n Si(CH3)2(OCH3)2 + n H2O → [–Si(CH3)2–O–]n + 2n CH3OH.
Le diméthyldichlorosilane étant facilement hydrolysé par la moindre trace d'humidité, il ne peut être manipulé à l'air libre. Une méthode utilisée pour contourner ce problème consiste à le convertir en un composé moins réactif, en l'occurrence le bis(diméthylamino)silane Si(CH3)2(N(CH3)2)2, avec formation de chlorure de diméthylammonium NH2(CH3)2Cl :
- SiCl2(CH3)2 + 4 NH(CH3)2 → Si(CH3)2(N(CH3)2)2 + 2 NH2(CH3)2Cl.
Le bis(diméthylamino)silane présente également l'avantage de former un polymère alternant lorsqu'on le fait réagir avec un comonomère disilanol[5] :
- n Si(CH3)2(N(CH3)2)2 + n HO(CH2)2Si–R–Si(CH2)2OH → [Si(CH3)2OSi(CH2)2–R–Si(CH2)2O]n + 2n HN(CH3)2.
Le sodium métallique peut être utilisé pour polymériser le diméthyldichlorosilane en formant du polysilane avec des chaînes –Si–Si–. D'autres types de monomères substitués de dichlorosilane SiH2Cl2, comme le diphényldichlorosilane SiCl2Ph2, peuvent être ajoutés pour ajuster les propriétés du polymère obtenu :
- n SiCl2(CH3)2 + 2n Na → [–Si(CH3)2–]n + 2n NaCl,
- n SiCl2(CH3)2 + SiCl2Ph2 + 2(n+m) Na → [–Si(CH3)2–]n[–Si(Ph2)–]m + 2(n+m) NaCl.
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Dimethyldichlorosilane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 5 décembre 2012 (JavaScript nécessaire)
- (en) Eugene G. Rochow, William S. Tatlock, « Dimethyldichlorosilane (Dimethylsilicon Dichloride) », Inorganic Syntheses, vol. 3, , p. 56-58 (lire en ligne) DOI 10.1002/9780470132340.ch14
- (en) Amitabha Mitra, David A. Atwood, « Polysiloxanes & Polysilanes », Encyclopedia of Inorganic Chemistry, (lire en ligne) DOI 10.1002/0470862106.ia201
- (en) Ulrich Lauter, Simon W. Kantor, Klaus Schmidt-Rohr et William J. MacKnight, « Vinyl-Substituted Silphenylene Siloxane Copolymers: Novel High-Temperature Elastomers », Macromolecules, vol. 32, no 10, , p. 3426-3431 (lire en ligne) DOI 10.1021/ma981292f.




