Éther azacouronne
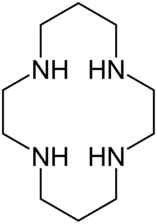
Un éther azacouronne, azaéther couronne ou éther couronne aza, est un composé chimique analogue à un éther couronne dont les atomes d'oxygène formant les liaisons éther sont remplacés par des atomes d'azote formant des fonctions amine, d'où le préfixe aza[1],[2]. Par exemple, aux éthers couronnes de formule générale (CH2CH2O)n correspondent des éthers azacouronnes de formule générale (CH2CH2NH)n, où n = 3, 4, 5 ou 6. Le 1,4,7-triazacyclononane (n = 3), le cyclène[3] (n = 4) et l'hexaaza-18-couronne-6 (en)[4] (n = 6) ont été particulièrement étudiés.
Synthèse
[modifier | modifier le code]La synthèse des éthers azacouronnes rencontre les difficultés associées à la production des macrocycles[5]. Le cycle à 18 atomes du (CH2CH2NH)6 (en) peut être produit en combinant deux triamines[4]. En réagissant avec le chlorure de tosyle, la diéthylènetriamine donne un dérivé portant deux groupes sulfonamides secondaires. Ces composés peuvent être utilisés comme synthons pour la macrocyclisation.
Variétés
[modifier | modifier le code]Il existe de nombreux types d'éthers azacouronnes :
- les éthers azacouronnes ont souvent des ponts éthylène (CH2)2 triméthylène (CH2)3. Le cyclame (en) (1,4,8,11-tétraazacyclotétradécane) contient les deux ;
- les éthers azacouronnes peuvent contenir des amines tertiaires. Par exemple, le 1,4,7-triméthyl-1,4,7-triazacyclononane ne contient que des amines tertiaires. Les cryptands, qui sont intermédiaires tridimensionnels entre éthers couronnes et éthers azacouronnes, contiennent deux amines tertiaires ;
- certains macrocycles contiennent à la fois des fonctions éther et des amines[6]. C'est par exemple le cas de l'éther diaza-18-couronne-6 [(CH2CH2O)2(CH2CH2NH)]2[7] ;
- les amines tertiaires permettent des configurations « en lasso » augmentant les capacités de complexation de ces composés[8].
Notes et références
[modifier | modifier le code]- (en) Andrea Bencini, Antonio Bianchi, Enrique Garcia-España, Mauro Micheloni et José Antonio Ramirez, « Proton coordination by polyamine compounds in aqueous solution », Coordination Chemistry Reviews, vol. 1, no 188, , p. 97-156 (DOI 10.1016/S0010-8545(98)00243-4, lire en ligne)
- (en) Roland Reichenbach-Klinke et Burkhard König, « Metal complexes of azacrown ethers in molecular recognition and catalysis », Journal of the Chemical Society, Dalton Transactions, no 2, , p. 121-130 (DOI 10.1039/b106367g, lire en ligne)
- (en) David P. Reed et Gary R. Weisman, « 1,4,7,10-Tatraazacyclododecane », Organic Syntheses, vol. 78, , p. 73 (DOI 10.15227/orgsyn.078.0073, lire en ligne)
- (en) T. J. Atkins1, J. E. Richman et W. F. Oettle, « Macrocyclic Polyamines: 1,4,7,10,13,16-Hexaäzacycloöctadecane », Organic Syntheses, vol. 58, , p. 86 (DOI 10.15227/orgsyn.058.0086, lire en ligne)
- (en) Krzysztof E. Krakowiak, Jerald S. Bradshaw et Daria J. Zamecka-Krakowiak, « Synthesis of aza-crown ethers », Chemical Reviews, vol. 89, no 4, , p. 929-972 (DOI 10.1021/cr00094a008, lire en ligne)
- (en) Hans K. Frensdorff, « Stability constants of cyclic polyether complexes with univalent cations », Journal of the American Chemical Society, vol. 93, no 3, , p. 600-606 (DOI 10.1021/ja00732a007, lire en ligne)
- (en) Vincent J. Gatto, Steven R. Miller et George W. Gokel, « 4,13-Diaza-18-Crown-6 », Organic Syntheses, vol. 68, , p. 227 (DOI 10.15227/orgsyn.068.0227, lire en ligne)
- (en) George W. Gokel, Leonard J. Barbour, Riccardo Ferdani et Jiaxin Hu, « Lariat Ether Receptor Systems Show Experimental Evidence for Alkali Metal Cation−π Interactions », Accounts of Chemical Research, vol. 35, no 10, , p. 878-886 (PMID 12379140, DOI 10.1021/ar000093p, lire en ligne)