2,2,6,6-Tétraméthylpipéridine
(Redirigé depuis 2,2,6,6-tétraméthylpipéridine)
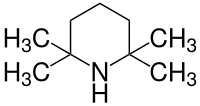
| 2,2,6,6-Tétraméthylpipéridine | |||
| |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | 2,2,6,6-tétraméthylpipéridine | ||
| Synonymes |
norpempidine, tétraméthylpipéridine |
||
| No CAS | |||
| No ECHA | 100.011.090 | ||
| No CE | 212-199-3 | ||
| No RTECS | TN4220000 | ||
| PubChem | 13035 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide incolore à jaune clair[1] | ||
| Propriétés chimiques | |||
| Formule | C9H19N [Isomères] |
||
| Masse molaire[2] | 141,253 9 ± 0,008 7 g/mol C 76,53 %, H 13,56 %, N 9,92 %, |
||
| Propriétés physiques | |||
| T° fusion | 28 °C[1] | ||
| T° ébullition | 152 °C[3] | ||
| Masse volumique | 0,837 g·cm-3 à 25 °C[3] | ||
| Point d’éclair | 24 °C[3] | ||
| Propriétés optiques | |||
| Indice de réfraction | = 1,445 à 20 °C[3] | ||
| Précautions | |||
| SGH[3] | |||
| H226, H301, H315, H319, H335, P261, P301+P310 et P305+P351+P338 |
|||
| Transport[3] | |||
|
|||
| Écotoxicologie | |||
| DL50 | 220 mg·kg-1 (souris, oral)[1] | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
La 2,2,6,6-tétraméthylpipéridine (TMP ou HTMP), est un composé organique dérivé de la pipéridine, une amine cyclique. Elle se présente sous la forme d'un liquide incolore à l'odeur de « poisson » caractéristique des amines. Elle est utilisée en chimie comme base encombrée, ayant l'avantage d'être soluble dans les solvants organiques, contrairement aux bases inorganiques telles que l'hydroxyde de potassium.
La TMP est un précurseur de bases plus fortes, tels que le tétraméthylpipéridinure de lithium (en) et du radical TEMPO.
Synthèse[modifier | modifier le code]
Une synthèse[4] possible de ce composé commence par l'addition conjuguée d'ammoniac sur la phorone. L'intermédiaire hydrazone est réduit via une réduction de Wolff-Kishner.

Notes et références[modifier | modifier le code]
- fiche 2,2,6,6-tetramethylpiperidine sur chemicalland21.com.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé 2,2,6,6-tetramethylpiperidine ≥99%, consultée le 26/04/2014. + [PDF] Fiche MSDS
- Detlef Kampmann, Georg Stuhlmüller, Roger Simon, Fabrice Cottet, Frédéric Leroux, Manfred Schlosser, A Large-Scale Low-Cost Access to the Lithium 2,2,6,6-Tetramethylpiperidide Precursor, Synthesis, 2005, vol. 2005(06), pp. 1028–1029. DOI 10.1055/s-2004-834856.




