« PRISMA (Norme de réalisation de revue systématique de la littérature) » : différence entre les versions
Créé en traduisant la page « Preferred Reporting Items for Systematic Reviews and Meta-Analyses » |
(Aucune différence)
|
Version du 25 février 2023 à 01:06

PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) est une norme qui regroupe un ensemble d'outils de pratique fondée sur les preuves visant à aider les auteurs d'articles scientifiques à balayer un grand nombre de sources lors de la réalisation de revues systématiques de la littérature ou de méta-analyses. À l'origine, cette méthode est utilisée dans le domaine médical pour évaluer les avantages et les inconvénients d'une démarche ou d'un traitement. Le but de PRISMA est de permettre aux auteurs de s'assurer de la transparence et de l'exhaustivité de leur revue systématique ou méta-analyse.[1] Elle permet de s'assurer que le travail de recherche documentaire ainsi produit est réplicable. Les chercheurs doivent expliciter les moyens mis en œuvre pour répondre à leur question de recherche, lister les mots-clés saisis dans les bases de données, et enfin définir les critères d'inclusion et d'exclusion des articles renvoyés. Lors de l'étape de criblage les articles pertinents au regard de la question de recherche sont conservés, ceux qui ne le sont pas sont laissés de coté. Les articles sont analysés en suivant une démarche prédéfinie. [2]
La norme PRISMA a remplacé la norme QUOROM antérieure.
Objectifs de PRISMA
Le but de la méthode PRISMA est d'aider les auteurs à améliorer la qualité de leurs publications de revues systématiques et méta-analyses.[3] Si PRISMA s'est principalement développée autour des études portant sur des essais randomisés, elle peut tout aussi bien être utile pour conduire d'autres types de revues de la littérature (par exemple, des études diagnostiques ou des études observationnelles ).
Histoire
En 1987, Cynthia Mulrow examine pour la première fois la qualité méthodologique d'un échantillon de 50 articles de revue de la littérature publiés dans quatre revues médicales de premier plan entre 1985 et 1986. Elle constate qu'aucun article analysé ne respecte l'ensemble des huit critères scientifiques alors présents dans les guides et recommandations pour la rédaction de revue de la littérature. De plus, le manque d'évaluation de la qualité des études prises en compte dans ces revues est un écueil majeur.[4] En 1987, Sacks et ses collègues[5] évaluent la qualité de 83 méta-analyses, en utilisant une grille de notation composés de 23 critères répartis dans six domaines principaux: la conception de l'étude, le choix de données assez homogènes pour être combinées, le contrôle des biais, l' analyse statistique, l'analyse de sensibilité et l'application des résultats. Les résultats de cette recherche montrent que la qualité des méta-analyses considérées est la plupart du temps médiocre. Dans leur conclusion, ils soulignent le besoin urgent d'améliorer les méthodes de recherche documentaire, d'évaluation de la qualité des essais et de synthèse des résultats.

En 1996, un groupe de 30 épidémiologistes, médecins, statisticiens, éditeurs et chercheurs de plusieurs pays se réunissent lors d'une conférence dans le but de rédiger des recommandations en vue d'améliorer la qualité des méta-analyses portant sur des essais randomisés contrôlés.[6] Cette conférence abouti à la liste de contrôle QUOROM et à un organigramme qui décrivent la manière adéquate de présenter le résumé, puis les sections introduction, méthodologie, résultats et discussion d'un article rendant compte d'une revue systématique ou d'une méta-analyse.[6] Huit des dix-huit éléments originaux constituent la base de la norme QUOROM. L'évaluation des articles est organisée autour de catégories; but de la recherche, sélection et évaluation de la qualité des articles primaires, agrégation des données, caractéristiques de l'étude et synthèse des données quantitatives. L'idée derrière l'inclusion de ce diagramme dans les pratiques des chercheurs est d'accroître la transparence des décisions prises pour inclure ou exclure certaines études du champs de la revue systématique et ainsi de renforcer l'objectivité des résultats qui en sont issus. En effet, l’exclusion arbitraire d'articles dans une revue systématique est susceptible d'engendrer des biais de sélection qui amoindriraient la qualité des résultats.[6]
En 2009, la norme QUOROM a été mise à jour pour tenir compte de plusieurs avancées conceptuelles et pratiques dans la science des revues systématiques et a été renommée PRISMA (Preferred Reporting Items of Systematic reviews and Meta-Analyses).[3]
Par la suite, celle-ci a connu deux mises à jour, PRISMA-2020[7][8], et PRISMA-S[9] qui incluent de nouvelles lignes directrices et recommandations.
Les éléments de PRISMA
La liste de contrôle PRISMA
La liste de contrôle comprend 27 éléments relatifs au contenu d'une revue systématique ou d'une méta-analyse. Ceux-ci sont répartis dans sept sections; titre, résumé, introduction, méthode, résultats, discussion et financement.[10]
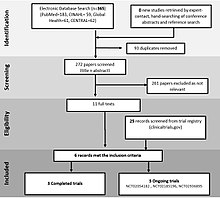
Le diagramme de flux PRISMA
Voici un exemple de diagramme de flux PRISMA :
Impact de PRISMA
L'utilisation de la liste de contrôle PRISMA est susceptible d'améliorer la qualité d'une revue systématique et permet davantage de transparence dans le processus utilisé pour sélectionner les articles qui lui servent de base. La norme PRISMA a été décrite et publiée dans plusieurs journaux à comité de lecture.[12][13][14][15][16]
De nombreuses revues médicales font référence à PRISMA dans leurs instructions aux auteurs, voire l'exigent pour toute publication de revue de littérature ou méta-analyse. Des enquêtes récentes auprès de revues médicales de premier plan ont évalué dans quelle mesure la méthode PRISMA a été intégrée dans leurs instructions aux auteurs. Pour un échantillon de 146 revues publiant des revues systématiques, la méthode PRISMA est mentionnée dans les instructions aux auteurs pour 27 % d'entre elles. Cette fréquence est plus élevée pour les revues de médecine générale et interne (50 %) que pour les revues de médecine spécialisée (25 %). [17] Ces résultats montrent que l'adoption des lignes directrices PRISMA par les revues reste insuffisante, bien qu'il y ait eu une certaine amélioration au fil du temps.
Environ 174 revues médicales à comité de lecture recommandent l'utilisation de la norme PRISMA pour la publication de revues systématiques et méta-analyses. [18] PRISMA a également été incluse comme l'un des outils d'évaluation des rapports de recherche au sein du réseau EQUATOR (Enhancing the Quality and Transparency of Health Care Research), une initiative internationale qui vise à améliorer la fiabilité et la qualité de la littérature scientifique dans le domaine médical en promouvant la transparence et la précision des articles.
Sources
- the PRISMA statement
- Regona, M.et al Opportunities and Adoption Challenges of AI in the Construction Industry: A PRISMA Review. J. Open Innov. Technol. Mark. Complex. 2022, 8, 45. https://doi.org/10.3390/joitmc8010045
- Liberati, Altman, Tetzlaff et Mulrow, « The PRISMA Statement for Reporting Systematic Reviews and Meta-Analyses of Studies That Evaluate Health Care Interventions: Explanation and Elaboration », PLOS Medicine, vol. 6, no 7, , e1000100 (PMID 19621070, PMCID 2707010, DOI 10.1371/journal.pmed.1000100) Erreur de référence : Balise
<ref>incorrecte : le nom « prisma » est défini plusieurs fois avec des contenus différents. - Mulrow, « The Medical Review Article: State of the Science », Annals of Internal Medicine, vol. 106, no 3, , p. 485–488 (PMID 3813259, DOI 10.7326/0003-4819-106-3-485)
- Sacks, Berrier, Reitman et Ancona-Berk, « Meta-Analyses of Randomized Controlled Trials », New England Journal of Medicine, vol. 316, no 8, , p. 450–455 (PMID 3807986, DOI 10.1056/NEJM198702193160806)
- Moher, Cook, Eastwood et Olkin, « Improving the quality of reports of meta-analyses of randomised controlled trials: the QUOROM statement », The Lancet, vol. 354, no 9193, , p. 1896–1900 (PMID 10584742, DOI 10.1016/S0140-6736(99)04149-5, S2CID 21826935)
- « The PRISMA 2020 statement: an updated guideline for reporting systematic reviews », BMJ (Clinical Research Ed.), vol. 372, , n71 (PMID 33782057, PMCID 8005924, DOI 10.1136/bmj.n71)
- « PRISMA 2020 explanation and elaboration: updated guidance and exemplars for reporting systematic reviews », BMJ (Clinical Research Ed.), vol. 372, , n160 (PMID 33781993, PMCID 8005925, DOI 10.1136/bmj.n160)
- Rethlefsen et et al. and PRISMA-S Group, « PRISMA-S: an extension to the PRISMA Statement for Reporting Literature Searches in Systematic Reviews. », Syst Rev., vol. 10, no 1, , p. 39 (DOI 10.1186/s13643-020-01542-z)
- Gedda, M, « Traduction française des lignes directrices PRISMA pour l'écriture et la lecture des revues systématiques et des méta-analyses », BMJ, 339, (lire en ligne [PDF])
- Bhaumik et Lassi, « Vitamin D as an adjunct for acute community-acquired pneumonia among infants and children: systematic review and meta-analysis », WikiJournal of Medicine, vol. 4, no 1, (DOI 10.15347/wjm/2017.005)
- Moher, Liberati, Tetzlaff et Altman, « Preferred Reporting Items for Systematic Reviews and Meta-Analyses: The PRISMA Statement », PLOS Medicine, vol. 6, no 7, , e1000097 (PMID 19621072, PMCID 2707599, DOI 10.1371/journal.pmed.1000097)
- Moher, Liberati, Tetzlaff et Altman, « Preferred Reporting Items for Systematic Reviews and Meta-Analyses: The PRISMA Statement », Annals of Internal Medicine, vol. 151, no 4, , p. 264–269 (PMID 21603045, PMCID 3090117, DOI 10.7326/0003-4819-151-4-200908180-00135)
- Moher, Liberati, Tetzlaff et Altman, « Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement », BMJ, vol. 339, , b2535 (PMID 19622551, PMCID 2714657, DOI 10.1136/bmj.b2535)
- Moher, Liberati, Tetzlaff et Altman, « Preferred Reporting Items for Systematic Reviews and Meta-Analyses: The PRISMA Statement », Journal of Clinical Epidemiology, vol. 62, no 10, , p. 1006–1012 (PMID 19631508, DOI 10.1016/j.jclinepi.2009.06.005, hdl 2434/211629)
- Moher, Liberati, Tetzlaff et Altman, « Preferred reporting items for systematic reviews and meta-analyses: The PRISMA statement », International Journal of Surgery, vol. 8, no 5, , p. 336–341 (PMID 20171303, DOI 10.1016/j.ijsu.2010.02.007)
- Tao, Li, Zhou et Moher, « From QUOROM to PRISMA: A Survey of High-Impact Medical Journals' Instructions to Authors and a Review of Systematic Reviews in Anesthesia Literature », PLOS ONE, vol. 6, no 11, , e27611 (PMID 22110690, PMCID 3217994, DOI 10.1371/journal.pone.0027611, Bibcode 2011PLoSO...627611T)
- PRISMA Endorsers. http://www.prisma-statement.org/Endorsement/PRISMAEndorsers
Liens externes
- Réseau ÉQUATEUR (Améliorer la qualité et la transparence de la recherche médicale)
