Kositer
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kositer | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Izgovarjava | IPA: [kɔˈsiːtəɾ] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Alotropi | srebrno-bel, β (beta); siv, α (alfa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Videz | srebrnobel (beta, β) ali siv (alfa, α) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standardna atomska teža Ar, std(Sn) | 118,710(7)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kositer v periodnem sistemu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vrstno število (Z) | 50 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina | skupina 14 (ogljikova skupina) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Perioda | perioda 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | blok p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Razporeditev elektronov | [Kr] 4d10 5s2 5p2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Razporeditev elektronov po lupini | 2, 8, 18, 18, 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikalne lastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Faza snovi pri STP | trdnina | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tališče | 231,93 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vrelišče | 2602 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gostota (blizu s.t.) | bel, β: 7,265 g/cm3 siv, α: 5,769 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| v tekočem stanju (pri TT) | 6,99 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Talilna toplota | bel, β: 7,03 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izparilna toplota | bel, β: 296,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplotna kapaciteta | bel, β: 27,112 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Parni tlak
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lastnosti atoma | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidacijska stanja | −4, −3, −2, −1, 0,[2] +1,[3] +2, +3,[4] +4 (amfoterni oksid) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativnost | Paulingova lestvica: 1,96 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizacijske energije |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomski polmer | empirično: 140 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentni polmer | 139±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsov polmer | 217 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Druge lastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pojavljanje v naravi | prvobitno | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristalna struktura | telesno centrirana tetragonalna bel (β) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristalna struktura | diamantna kubična siv (α) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hitrost zvoka tanka palica | 2730 m/s (pri r.t.) (zvito) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperaturni raztezek | 22,0 µm/(m⋅K) (pri 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplotna prevodnost | 66,8 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Električna upornost | 115 nΩ⋅m (pri 0 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetna ureditev | siv: diamagnetik[5] bel (β): paramagnetik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetna susceptibilnost | (bel) +3,1·10−6 cm3/mol (298 K)[6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Youngov modul | 50 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Strižni modul | 18 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stisljivostni modul | 58 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poissonovo razmerje | 0,36 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trdota po Brinellu | 50–440 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Številka CAS | 7440-31-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zgodovina | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Odkritje | okoli 32. stoletje pr. n. št. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Simbol | "Sn": iz lat. stannum | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Najpomembnejši izotopi kositra | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kositer ali cin je kemični element s simbolom Sn (iz latinsko Stannum stannum) in atomskim številom 50. Kositer je srebrna kovina, ki ima značilen rumenkast odtenek. Kositer je tako kot indij dovolj mehak, da ga je mogoče rezati brez večje sile. [7] Ko se palica kositra upogne, lahko slišimo tako imenovani "kositrov krik " kot v kristalih kositra nastajajo kristali dvojčki; to lastnost imajo tudi indij, kadmij, cink in zmrznjeno živo srebro. Čisti kositer po strjevanju ohranja zrcalni videz, podoben večini kovin. Vendar se v večini kositrovih zlitin kovina strdi z dolgočasno sivo barvo. Kositer je po-prehodna kovina v skupini 14 periodnega sistema elementov. Pridobiva se predvsem iz minerala kasiterita, ki vsebuje kositrov oksid, SnO2. Kositer kaže kemijsko podobnost z obema sosedoma v skupini 14, to je z germanijem in svincem, in ima dve glavni stopnji oksidacije, +2 in nekoliko stabilnejšo +4. Kositer je 49. najpogostejši element na Zemlji in je z 10 stabilnimi izotopi element z največjim številom stabilnih izotopov v periodnem sistemu, zahvaljujoč čarobnemu številu protonov. Ima dva glavna alotropa: pri sobni temperaturi je to stabilen β-kositer, srebrno bela, gnetljiva kovina, pri nizkih temperaturah pa preide v manj gost siv α-kositer, ki ima diamantno kubično strukturo. Kovinski kositer v zraku ne oksidira zlahka.
Prva zlitina kositra,ki se je že od leta 3000 prn.št. uporabljala v velikem obsegu, je bron, zlitina kositra in bakra. Po 600 pr.n.št.so začeli izdelovati čisti kovinski kositer iz 85–90% kositra, preostanek je običajno iz bakra, antimona in svinca, uporabljal se je za posodo vse od bronaste dobe do 20. stoletja. Dandanes se kositer uporablja v številnih zlitinah, predvsem v mehkih spajkah iz svinca in svinca, ki vsebujejo običajno 60% ali več kositra, in pri izdelavi prozornih, električno prevodnih filmov indijevega kositrovega oksida za optoelektroniko. Druga velika vloga kositra so proti rji odporne prevleke jekla. Zaradi nizke toksičnosti anorganskega kositra se pocinjeno jeklo pogosto uporablja za pakiranje živil v pločevinke. Nekatere organokositrne spojine pa so lahko skoraj tako strupene kot cianid .
Značilnosti[uredi | uredi kodo]
Fizikalne lastnosti[uredi | uredi kodo]

kositer je mehka, voljna, gnetljiva in visoko kristalna srebrno bela kovina. Ko se bar kositra ukrivi, je slišati prasketanje zaradi nastanka kristalov dvojčkov.[8] Kositer se topi pri nizkih temperaturah kakih 232 °C, najniže v skupini 14.[9][10]
β-kositer (kovinska oblika ali struktura belega kositra, BCT), ki je stabilen pri sobni temperaturi in nad njo, je gnetljiv. α-kositer (nekovinska oblika ali siv kositer), ki je stabilen pod 13,2 °C, je po drugi strani krhek. α-kositer ima diamantno kubično kristalno strukturo, podobno kot diamant, silicij ali germanij. α-kositer nima kovinskih lastnosti, ker njegovi atomi tvorijo kovalentno strukturo, v kateri se elektroni ne morejo prosto gibati. Je mrko siv praškasti material, ki se razen v nekaj specializiranih polprevodniških aplikacijah ne uporablja. [8] Ta dva alotropa, α-kositer in β-kositer, sta bolj pogosto znana kot sivi kositer in beli kositer. Obstajata še dva druga alotropa, γ in σ, in sicer pri temperaturah nad 161 °C in tlakih nad več GPa.[11] V hladnih razmerah se β-kositer spontano spreminja v α-kositer, pojav, ki je znan kot " kositrova kuga" ali "kositrova bolezen". Nekateri nepreverljivi viri pravijo tudi, da so se med Napoleonovo rusko kampanjo leta 1812 temperature tako ohladile, da so se pločevinasti gumbi na vojaških uniformah sčasoma razpadli, kar je prispevalo k porazu velike vojske [12] - vztrajna legenda, ki verjetno nima ozadja v resničnih dogodkih. [13] [14] [15]
Čeprav je temperatura transformacije α-β nominalno 13,2 °C, nečistoče (npr Al, Zn itd.) temperaturo prehoda znižajo precej pod 0 °C: Če se doda antimon ali bizmut, do prehoda verjetno sploh ne pride, kar poveča trajnost kositra.[16]
Tržne vrste kositra (99,8%) se upirajo preoblikovanju zaradi zaviralnega učinka majhnih količin bizmuta, antimona, svinca in srebra, ki so prisotne kot nečistoče. Legirni elementi, kot so baker, antimon, bizmut, kadmij in srebro, povečajo njegovo trdoto. Kositer precej rad tvori trde, krhke intermetalne faze, ki so pogosto nezaželene. V drugih kovinah na splošno ne tvori trdnih raztopin širokih razponov in le redki elementi imajo omembe vrednost topnost v trdnem stanju v kositru. Preprosti evtektični sistemi pa so prisotni v kombinaciji z bizmutom, galijem, svincem, talijem in cinkom. [16]
Kositer postane superprevodnik pod 3,72 K [17] in je eden prvih superprevodnikov, ki se jih je raziskalo; Meissnerjev učinek, ena značilnih lastnosti superprevodnikov, so prvič dokazali v superprevodniških kristalih kositra. [18]
Kemične lastnosti[uredi | uredi kodo]
Kositer se upira koroziji zaradi vode, lahko pa ga napadejo kisline in alkalije. Kositer se lahko zelo gladko polira in uporablja se kot zaščitni premaz za druge kovine. [8] Zaščitni oksidni (pasivacijski) sloj preprečuje nadaljnjo oksidacijo.[19] Kositer deluje kot katalizator, kadar je kisik v raztopini in pomaga pospešiti kemično reakcijo.
Izotopi[uredi | uredi kodo]
Kositer ima deset stabilnih izotopov z atomskimi masami od 112, 114 do 120, 122 in 124, največje število med elementi v periodnem sistemu. Med njimi je največ 120Sn (skoraj tretjina vsega kositra), 118Sn in 116Sn, najmanj pa 115Sn. Izotopi s parnimi masnimi števili nimajo jedrskega spina, tisti z neparnimi pa imajo spin +1/2. Kositer je s svojimi tremi skupnimi izotopi 116Sn, 118Sn in 120Sn eden najlažjih elementov za odkrivanje in analizo z NMR spektroskopijo, njegovi kemijski premiki pa se nanašajo na SnMe
4.. [note 1] [20]
To veliko število stabilnih izotopov naj bi bilo neposreden rezultat atomskega števila 50, " čarobnega števila " v jedrski fiziki. Kositer se pojavlja tudi v 31 nestabilnih izotopih, ki zajemajo vse preostale atomske mase od 99 do 139. Razpolovni čas vseh radioizotopov je poleg 126Sn z razpolovno dobo 230.000 let manj kot eno leto. Radioaktivni 100Sn, odkriti leta 1994, in 126Sn sta dva izmed redkih nuklidov z " dvojno čarobnim " jedrom: kljub temu, da sta nestabilna in imajo zelo enostransko razmerje med protonom in nevtronom, predstavljata končni točki, prek katerih stabilnost hitro upada. [21] Za izotope med 111 in 131 je bilo značilnih še 30 metastabilnih izomerov, najbolj stabilen pa je 121mSn z razpolovno dobo 43,9 let.
Relativne razlike v številčnosti stabilnih izotopov kositra lahko razložimo z različnimi načini tvorjenja pri zvezdni nukleosintezi. 116Sn do 120Sn vključno nastajajo s s-procesom (zajem počasnih nevtronov) v večini zvezd in zato so najpogostejši izotopi, medtem ko 122Sn in 124Sn nastajata samo v r-procesu (hitri zajem nevtronov) v supernovah in sta manj pogosta. (Izotopi 117Sn do 120Sn vključujejo prispevke tudi od r- procesa.) Končno, najredkejših s protoni bogatih izotopov, 112Sn, 114Sn in 115Sn, ni mogoče dobiti v pomembnih količinah v s - ali r- procesih in jih štejemo med p-jedra, katerih izvor še ni dobro razumljen. Nekatere hipoteze glede mehanizma za njihov nastanek predlagajo zajem protonov kot tudi foto razpad, čeprav bi 115Sn lahko tudi nastajal delno v s -procesu, bodisi neposredno bodisi kot potomec dolgoživega 115In [22]
Etimologija[uredi | uredi kodo]
Besedo cin si delijo germanski jeziki in jo lahko izsledimo do rekonstruiranega protogermanskega *tin-om ; sorodniki vključujejo nemški Zinn , Švedski tenn in nizozemski tin. V drugih indoevropskih vejah besede ne najdemo, razen kot izposojeno iz germanske veje (npr. Irski tinne iz angleščine).
Latinsko ime stannum prvotno pomenilo zlitino srebra in svinca, v 4. stoletju pa je pomenilo 'cin' [23] - starejše latinsko ime zanj je bilo plumbum candidum , ali "beli svinec". Stannum očitno prihaja iz prejšnjega stāgnum (kar pomeni isto snov), izvor romanskih in keltskih izrazov za kositer. [24] Izvor stannum / stāgnum ni znan; lahko da ima pred-indoevropske korenine. [25]
Meyers Konversations-Lexikon po drugi strani zagovarja tezo, da stannum izhaja iz (predhodnika) v kornijščina stean , in je dokaz, da je bil Cornwall v prvih stoletjih našega štetja glavni vir kositra.
Zgodovina[uredi | uredi kodo]

Pridobivanje in uporabo kositra je mogoče datirati v začetke bronaste dobe okoli leta 3000 pred našim štetjem, ko so opazili, da imajo bakreni predmeti iz rud več kovin z različnimi deleži različne fizikalne lastnosti. [26] Najzgodnejši bronasti predmeti so imeli vsebnost kositra ali arzena manj kot 2%, zato naj bi bili rezultat nenamernega legiranja zaradi prisotnostii kovin v bakreni rudi. [27] Dodatek druge kovine bakru poveča njegovo trdoto, zniža temperaturo taljenja in izboljša postopek ulivanja z izdelavo bolj tekoče taline, ki se ohladi na gostejšo, manj gobasto kovino. To je bila pomembna novost, ki je omogočila veliko bolj zapletene oblike pri odlivanju v zaprte kalupe bronaste dobe. Arsenski bronasti predmeti se prvič pojavijo na Bližnjem vzhodu, kjer je arzen pogosto povezan z bakrovo rudo; zelo hitro je tveganje za zdravje postalo jasno in iskanje virov se je osredotočilo na veliko manj nevarne kositrne rude. [28] To je ustvarilo povpraševanje po redkem kovinskem kositru in oblikovalo trgovsko mrežo, ki je daljne vire kositra povezovala s trgi bronaste dobe.
Kasiterit (SnO2), oblika kositrovega oksida, je bil v starih časih najverjetneje prvotni vir kositra. Druge oblike kositrove rude so manj bogati sulfidi, kot je stanit, ki zahtevajo bolj vključen postopek taljenja. Kasiterit se pogosto kopiči v naplavinah kot usedline, saj je trši, težji in kemično bolj odporen kot pripadajoči granit. [27] Kasiterit je običajno črne ali na splošno temne barve in te nanose je mogoče zlahka videti na rečnih bregovih. Aluvialne depozite je bilo mogoče mimogrede zbirati in izpirati po podobnih metodah kot pri iskanju zlata. [29]
Spojine in kemija[uredi | uredi kodo]
Anorganske spojine[uredi | uredi kodo]
V veliki večini svojih spojin ima kositer oksidacijsko stanje II ali IV.Halogenidne spojine so znane v obeh stopnjah oksidacije. Za Sn (IV) so znani vsi štirje halogenidi: SnF4, SnCl4, SnBrl4 in SnI4. Trije težji med njimi so hlapne molekularne spojine, tetrafluorid pa je polimer. Vsi štirje halogenidi obstajajo tudi kot soli Sn(II): SNF2 SnCl2, SnBr2 in SnI2. Vse štiri so trdi polimeri. Od teh osmih spojin imajo samo jodidi barvo.
Kositrov (II) klorid je komercialno najpomembnejši kositrov halid. Kot za druge podobne spojine, reagira klor s kovinskim kositrom, da nastane SnCl4, v reakciji klorovodikove kisline in kositra pa nastane SnCl2 in vodikov plin. Druga možnost je, da se SnCl4 in Sn združita s kositrovim (II) kloridom v naslednji reakciji : [30]
- SnCl4 + Sn → 2 SnCl2
Kositer lahko tvori veliko oksidov, sulfidov in drugih halkogenidnih spojin. Dioksid SnO2 (kasiterit) nastane pri segrevanju kositra v prisotnosti zraka. SnO2 je amfoterenkar pomeni, da se raztaplja tako v kislih kot bazičnih raztopinah. [31] Stanati s strukturo [Sn(OH)6] 2-, kot K2[Sn(OH)6], so tudi znani, čeprav prosta kositrova kislina H2[Sn(OH)6] ni znan.
Sulfidi kositra obstajajo v +2 in +4 stopnjah oksidacije: kot kositer (II) sulfid in kositer (IV) sulfid (mozaično zlato ).

Hidridi[uredi | uredi kodo]
Stanan (SnH4), s kositrom v +4 stopnji oksidacije je nestabilen. Vendar so organokositrni hidridi dobro znani, npr. Tributiltin hidrid (Sn (C4H9)3H). [8] Te spojine sproščajo prehodne tributil kositer radikale, ki so redki primeri spojin kositra (III). [33]
Organokositrne spojine[uredi | uredi kodo]
Organokositrne spojine, včasih imenovane tudi stanani, so kemične spojine z vezjo kositer-ogljik. [34] Med spojinami kositra so organski derivati komercialno najbolj uporabni. [35] Nekatere organokositrne spojine so zelo strupene in so se uporabljale kot biocidi. Prva organokositrna spojina, o kateri se je poročal, je bil dietiltin dijodid ((C2H5)2Snl2) leta 1849. [36]
Večina organokositrnih spojin so brezbarvne tekočine ali trdne snovi, ki so stabilne na zraku in v vodi. Privzemajo tetraedrično geometrijo. Spojine tetraalkil- in tetraariltina se lahko pripravijo z uporabo Grignardovih reagentov : [35]
- SnCl
4 + 4 RMgBr → R
4Sn + 4 MgBrCl
Mešane halogenid-alkili, ki so pogostejši in komercialno pomembnejši od derivatov tetraorgana, se pripravljajo z reakcijami prerazporeditve :
- SnCl
4 + R
4Sn → 2 SnCl2R2
Dvovalentne organokositrne spojine so neobičajne, čeprav pogostejše kot sorodne dvovalentne organogermanijeve in organosilicijeve spojine. Večjo stabilizacijo, ki jo uživa Sn (II), pripisujemo " učinku inertnega para ". Spojine organokositra (II) so tako stanileni (formula: R2Sn, kot je videti v singletnih karbenih) kot distanileni (R4Sn2), ki so približno enakovredni alkenom. Oba razreda kažeta nenavadne reakcije. [37]
Pogostnost in najdišča[uredi | uredi kodo]

Kositer nastane v dolgem <i id="mwAeQ">s</i> -procesu v zvezdah z nizko do srednjo maso (z masami od 0,6 do 10-krat večje od mase Sonca) in nazadnje z beta razpadom težkih izotopov indija. [38]Kositer je 49. najpogostejši element v zemeljski skorji, ki predstavlja 2 ppm v primerjavi s 75 ppm za cink, 50 ppm za baker in 14 ppm za svinec. [39]
Kositer se ne pojavlja kot naravni element, temveč ga je treba pridobivati iz različnih rud. Kasiterit (SnO2) je edini komercialno pomemben vir kositra, čeprav se majhne količine kositra pridelujejo tudi iz kompleksnih sulfidov, kot so stannit, cilindrit, frankeit, kanfildit in teallit. Minerali s kositrom so skoraj vedno povezani z granitno kamnino, običajno na ravni 1% vsebnosti kositrovega oksida. [40]
Zaradi večje specifične teže kositrovega dioksida je približno 80% pridobljenega kositra iz sekundarnih nahajališč, ki jih najdemo nizvodno od primarnih najdišč. Kositer se pogosto pridobiva iz zrnc, ki jih je v preteklosti sprala voda in odložila v doline ali morje. Najbolj ekonomični načini pridobivanja kositra je poglabljanje, hidravlično kopanje ali odprte jame. Večina svetovnega kositra je izdelan iz Placer depozitov, ki lahko vsebujejo tudi tako malo kot 0,015% kositra. [41]
| Država | Rezerve |
|---|---|
| 1.500.000 | |
| 250.000 | |
| 310.000 | |
| 800.000 | |
| 590.000 | |
| 400.000 | |
| 350.000 | |
| 180.000 | |
| 170.000 | |
| Drugo | 180.000 |
| Skupaj | 4.800.000 |
V letu 2011 so izkopali približno 253.000 ton kositra, večinoma na Kitajskem (110.000 t), Indoneziji (51.000 t), Peruju (34.600 t), Boliviji (20.700 t) in Braziliji (12.000 t). [42] Ocene za proizvodnjo kositra so se v preteklosti spreminjale glede na dinamiko ekonomske izvedljivosti in razvoja rudarskih tehnologij, vendar se ocenjuje, da bo Zemlji ob sedanjih stopnjah porabe in tehnologijah v 40 letih zmanjkalo kositra, ki ga je mogoče rudariti. [43] Lester Brown meni, da bi kositra lahko zmanjkalo v 20 letih na podlagi izjemno konzervativne ekstrapolacije 2-odstotne rasti na leto. [44]
Sekundarni ali odpadni kositer je tudi pomemben vir kovine. Predelava kositra s sekundarno proizvodnjo ali recikliranjem odpadnega kositra se hitro narašča. Medtem ko ZDA od leta 1993 ne kopajo in tudi več ne talijo kositra, so bile največja sekundarna proizvajalka, ki je leta 2006 reciklirala skoraj 14.000 ton. [42]O novih nahajališčih poročajo v Mongoliji [45] leta 2009 pa je skupina Seminole Group Colombia CI, SAS odkrila nova nahajališča v Kolumbiji. [46]
Cena in trgi[uredi | uredi kodo]
Deset največjih podjetij je leta 2007 proizvedlo večino kositra na svetu.Večina svetovnega kositra se trguje na Londonski borzi kovin (LME) iz osmih držav pod 17 blagovnimi znamkami. [47]Leta 1947 je bil ustanovljen Mednarodni svet za kositer, ki je nadzoroval cene kositra, dokler ni leta 1985 propadel. Leta 1984 je bilo ustanovljeno Združenje držav proizvajalk kositra, v katerega so bili včlanjeni Avstralija, Bolivija, Indonezija, Malezija, Nigerija, Tajska in Zair. [48] Londonska borza kovin (LME) je glavno mesto za trgovanje s kositrom. [42] Drugi pogodbeni trgi kositra so trg kositra v Kuala Lumpurju (KLTM) in borza kositra v Indoneziji (INATIN). [49]
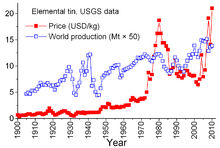
Kositer je edinstven med drugimi mineralnimi surovinami zaradi zapletenih sporazumov med državami proizvajalkami in državami potrošnicami iz leta 1921. Prejšnji sporazumi so bili nekoliko neformalni in občasni ter so leta 1956 privedli do "prvega mednarodnega sporazuma o kositru", prvega iz nenehno oštevilčenih serij, ki so se dejansko propadle leta 1985. S to vrsto sporazumov je Mednarodni svet za kositer (ITC) znatno vplival na cene kositra. ITC je podpiral ceno kositra v obdobjih nizkih cen z nakupom kositra za njegove varovalne zaloge in v obdobjih visokih cen trg s prodajo kositra iz zaloge umirjal. To je bil pristop prostega trga, katerega namen je bil zagotoviti zadosten pretok kositra v države potrošnice in dobiček za države proizvajalke. Vendar zaloge niso zadoščale in večino teh 29 let so cene kositra naraščale, včasih močno, zlasti med letoma 1973 in 1980, ko je močna inflacija pestila številna svetovna gospodarstva. [50]
V poznih sedemdesetih in zgodnjih osemdesetih letih je ameriška vlaga agresivno prodajala svoje zaloge kositra, deloma zato, da izkoristi zgodovinsko visoke cene kositra. Ostra recesija 1981–82 je bila precej huda za industrijo pločevine. Poraba kositra se je močno zmanjšala. ITC se je uspel izogniti resničnim strmim padcem s pospešenim odkupom svojih rezervnih zalog; ta dejavnost je zahtevala, da se je ITC veliko zadolževal pri bankah in kovinskih podjetjih za povečanje svojih virov. ITC se je še naprej zadolževal do konca leta 1985, ko je dosegel svoj kreditni limit. Takoj je sledila velika "kositrska kriza" - kositer je bil za približno tri leta izključen iz trgovanja na Londonski borzi kovin, ITC se je kmalu zatem razpustil in cena kositra, ki je zdaj v prostem tržnem okolju, je strmo padla na 4 dolarje na funt in na tej ravni ostala v devetdesetih letih. [50] Cena se je do leta 2010 znova višala, po porastu potrošnje pa je sledila svetovna gospodarska kriza 2008–2009, ki je spremljala obnovo zalog in nadaljnjo rast potrošnje svetovnih gospodarstev v razvoju. [42]
Uporaba[uredi | uredi kodo]
Spajka[uredi | uredi kodo]
Leta 2018 je bila za spajkanje uporabljena slaba polovica vsega proizvedenega kositra. Preostanek je bil razdeljen med prevleke s kositrom,kemikalije kositra, medenino in bronaste zlitine ter specialne namene. [51]i

Kositer se že dolgo uporablja v zlitinah s svincem kot spajkanje v količinah od 5 do 70% m / m. Kositer s svincem tvori evtektično zmes v utežnem deležu 61,9% kositra in 38,1% svinca (atomski delež: 73,9% kositra in 26,1% svinca), s temperaturo tališča 183 ° C (361,4 ° F). Takšne spajke se uporabljajo predvsem za spajanje cevi ali električnih vezij. Odkar sta 1. julija 2006 začela veljati direktiva Evropske unije o odpadni električni in elektronski opremi (direktiva o OEEO) in direktiva o omejevanju nevarnih snovi, se je vsebnost svinca v takih zlitinah zmanjšala. Zamenjava svinca ima številne težave, vključno z višjim tališčem in tvorbo brčic kositra,, ki povzročajo električne težave. V svinčevih spajkah se lahko pojavi kositrova kuga, kar povzroči izgubo spajkanega spoja. Pospešeno se iščejo nadomestne zlitine, čeprav težave s celovitostjo sklepov ostajajo. [52]
Kositrne prevleke[uredi | uredi kodo]
Kositer se zlahka veže na železo in se uporablja za proti-korozijske prevleke svinca, cinka in jekla. Pokositrene jeklene posode se pogosto uporabljajo za konzerviranje hrane, kar predstavlja velik del trga kovinskega kositra. Konzerva iz pločevine za konzerviranje hrane je bila prvič izdelana v Londonu leta 1812. [53] Bakrene posode za kuhanje, kot so ponev in ponve, so pogosto obložene s tanko prevleko iz kositra, ker je kombinacija kislih živil in bakra lahko strupena.
Previdnostni ukrepi[uredi | uredi kodo]
Primeri zastrupitve s kovino kositra, njenimi oksidi in solmi so skoraj neznani. Po drugi strani pa so nekatere organokositrne spojine skoraj tako strupene kot cianid. [35]
Izpostavljenost kositru na delovnem mestu je lahko z vdihavanjem, stikom s kožo in stikom z očmi. Uprava za varnost in zdravje pri delu (OSHA) je postavila zakonsko mejo (dovoljeno mejo izpostavljenosti) za izpostavljenost kositru na delovnem mestu kot 2 mg / m 3 v 8-urnem delovnem dnevu. Nacionalni inštitut za varnost in zdravje pri delu (NIOSH) je določil priporočeno mejo izpostavljenosti (REL) 2 mg / m 3 v 8-urnem delovnem dnevu. Na ravni 100 mg / m 3, kositer je takoj nevaren za življenje in zdravje. [54]
Opombe[uredi | uredi kodo]
- ↑ Only H, F, P, Tl and Xe have a higher receptivity for NMR analysis for samples containing isotopes at their natural abundance.
Sklici[uredi | uredi kodo]
- ↑ Meija, Juris; in sod. (2016). »Atomic weights of the elements 2013 (IUPAC Technical Report)«. Pure and Applied Chemistry. 88 (3): 265–91. doi:10.1515/pac-2015-0305.
- ↑ »New Type of Zero-Valent Tin Compound«. Chemistry Europe. 27. avgust 2016.
- ↑ »HSn«. NIST Chemistry WebBook. National Institute of Standards and Technology. Pridobljeno 23. januarja 2013.
- ↑ »SnH3«. NIST Chemistry WebBook. National Institure of Standards and Technology. Pridobljeno 23. januarja 2013.
- ↑ Lide, D. R., ur. (2005). »Magnetic susceptibility of the elements and inorganic compounds«. CRC Handbook of Chemistry and Physics (PDF) (86th izd.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ↑ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. str. E110. ISBN 0-8493-0464-4.
- ↑ Gray, Theodore (2007). »Tin images«. The Elements. Black Dog & Leventhal.
- ↑ 8,0 8,1 8,2 8,3 Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). »Tin«. Lehrbuch der Anorganischen Chemie (v nemščini) (91–100 izd.). Walter de Gruyter. str. 793–800. ISBN 978-3-11-007511-3.
- ↑ »Ink with tin nanoparticles could print future circuit boards«. Phys.org. 12. april 2011. Arhivirano iz prvotnega spletišča dne 16. septembra 2011.
- ↑ Jo, Yun Hwan; Jung, Inyu; Choi, Chung Seok; Kim, Inyoung; Lee, Hyuck Mo (2011). »Synthesis and characterization of low temperature Sn nanoparticles for the fabrication of highly conductive ink«. Nanotechnology. 22 (22): 225701. Bibcode:2011Nanot..22v5701J. doi:10.1088/0957-4484/22/22/225701. PMID 21454937.
- ↑ Molodets, A.M.; Nabatov, S.S. (2000). »Thermodynamic potentials, diagram of state, and phase transitions of tin on shock compression«. High Temperature. 38 (5): 715–721. doi:10.1007/BF02755923.
- ↑ Le Coureur, Penny; Burreson, Jay (2004). Napoleon's Buttons: 17 molecules that changed history. New York: Penguin Group, USA.
- ↑ Öhrström, Lars (2013). The Last Alchemist in Paris. Oxford: Oxford University Press. ISBN 978-0-19-966109-1.
- ↑ Cotton, Simon (29. april 2014). »Book review: The last alchemist in Pari«. Chemistry World. Royal Society of Chemistry. Arhivirano iz prvotnega spletišča dne 10. avgusta 2014. Pridobljeno 22. novembra 2019.
- ↑ Emsley, John (1. oktober 2011) [2001]. Nature's Building Blocks: an A-Z Guide to the Elements (New izd.). New York, United States: Oxford University Press. str. 552. ISBN 978-0-19-960563-7.
Only officers had metal buttons, and those were made of brass.
- ↑ 16,0 16,1 Schwartz, Mel (2002). »Tin and alloys, properties«. Encyclopedia of Materials, Parts and Finishes (2. izd.). CRC Press. ISBN 978-1-56676-661-6.
- ↑ Dehaas, W.; Deboer, J.; Vandenberg, G. (1935). »The electrical resistance of cadmium, thallium and tin at low temperatures«. Physica. 2 (1–12): 453. Bibcode:1935Phy.....2..453D. doi:10.1016/S0031-8914(35)90114-8.
- ↑ Meissner, W.; R. Ochsenfeld (1933). »Ein neuer effekt bei eintritt der Supraleitfähigkeit«. Naturwissenschaften. 21 (44): 787–788. Bibcode:1933NW.....21..787M. doi:10.1007/BF01504252.
- ↑ Craig, Bruce D.; Anderson, David S.; International, A. S. M. (Januar 1995). Handbook of corrosion data. str. 126. ISBN 978-0-87170-518-1. Arhivirano iz prvotnega spletišča dne 11. maja 2016.
- ↑ »Interactive NMR Frequency Map«. Arhivirano iz prvotnega spletišča dne 4. junija 2011. Pridobljeno 5. maja 2009.
- ↑ Walker, Phil (1994). »Doubly Magic Discovery of Tin-100«. Physics World. 7 (June): 28. doi:10.1088/2058-7058/7/6/24.
- ↑ Cameron, A. G. W. (1973). »Abundance of the Elements in the Solar System« (PDF). Space Science Reviews. 15 (1): 121–146. Bibcode:1973SSRv...15..121C. doi:10.1007/BF00172440. Arhivirano iz prvotnega spletišča (PDF) dne 21. oktobra 2011.
- ↑ Encyclopædia Britannica, 11th Edition, 1911, s.v. 'tin', citing H. Kopp
- ↑ »The Ancient Mining of Tin«. oxleigh.freeserve.co.uk. Arhivirano iz prvotnega spletišča dne 3. aprila 2009. Pridobljeno 7. julija 2009.
- ↑ American Heritage Dictionary
- ↑ Cierny, J.; Weisgerber, G. (2003). »The "Bronze Age tin mines in Central Asia«. V Giumlia-Mair, A. (ur.). The Problem of Early Tin. Oxford: Archaeopress. str. 23–31. ISBN 978-1-84171-564-3.
- ↑ 27,0 27,1 Penhallurick, R. D. (1986). Tin in Antiquity: its Mining and Trade Throughout the Ancient World with Particular Reference to Cornwall. London: The Institute of Metals. ISBN 978-0-904357-81-3.
- ↑ Charles, J. A. (1979). »The development of the usage of tin and tin-bronze: some problems«. V Franklin, A. D. (ur.). The Search for Ancient Tin. Washington D.C.: A seminar organized by Theodore A. Wertime and held at the Smithsonian Institution and the National Bureau of Standards, Washington D.C. March 14–15, 1977. str. 25–32.
- ↑ Dube, RK (september 2006). »Interrelation between gold and tin: A historical perspective«. Gold Bulletin. 39 (3): 103–113. doi:10.1007/BF03215537.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. izd.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ Taylor, F. Sherwood (1942). Inorganic & Theoretical Chemistry (6th izd.). Heineman.
- ↑ J. M. Leger; J. Haines; A. Atouf (1996). »The high pressure behaviour of the cotunnite and post-cotunnite phases of PbCl2 and SnCl2«. J. Phys. Chem. Solids. 57 (1): 7–16. Bibcode:1996JPCS...57....7L. doi:10.1016/0022-3697(95)00060-7.
- ↑ Gaur, D. P.; Srivastava, G.; Mehrotra, R. C. (1973). »Organic Derivatives of Tin. III. Reactions of Trialkyltin Ethoxide with Alkanolamines«. Zeitschrift für Anorganische und Allgemeine Chemie. 398: 72. doi:10.1002/zaac.19733980109.
- ↑ Elschenbroich, C. "Organometallics" (2006) Wiley-VCH: Weinheim. ISBN 978-3-527-29390-2
- ↑ 35,0 35,1 35,2 Graf, G. G. (2000) "Tin, Tin Alloys, and Tin Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2005 Wiley-VCH, Weinheim DOI: 10.1002/14356007.a27_049
- ↑ Thoonen, Sander H. L.; Deelman, Berth-Jan; van Koten, Gerard (2004). »Synthetic aspects of tetraorganotins and organotin(IV) halides« (PDF). Journal of Organometallic Chemistry. 689 (13): 2145–2157. doi:10.1016/j.jorganchem.2004.03.027. Arhivirano iz prvotnega spletišča (PDF) dne 7. avgusta 2011. Pridobljeno 31. julija 2009.
- ↑ Peng, Yang; Ellis, Bobby D.; Wang, Xinping; Fettinger, James C.; Power, P. P. (2009). »Reversible Reactions of Ethylene with Distannynes Under Ambient Conditions«. Science. 325 (5948): 1668–1670. Bibcode:2009Sci...325.1668P. doi:10.1126/science.1176443. PMID 19779193.
- ↑ Shu, Frank H. (1982). The physical universe: An introduction to astronomy. University Science Books. str. 119–121. ISBN 978-0-935702-05-7.
- ↑ Emsley 2001
- ↑ »Tin: From Ore to Ingot«. International Tin Research Institute. 1991. Arhivirano iz prvotnega spletišča dne 22. marca 2009. Pridobljeno 21. marca 2009.
- ↑ Sutphin, David M.; Sabin, Andrew E.; Reed, Bruce L. (1. junij 1992). Tin – International Strategic Minerals Inventory Summary Report. str. 9. ISBN 978-0-941375-62-7. Arhivirano iz prvotnega spletišča dne 28. aprila 2016.
- ↑ 42,0 42,1 42,2 42,3 42,4 Carlin, Jr., James F. »Tin: Statistics and Information«. United States Geological Survey. Arhivirano iz prvotnega spletišča (PDF) dne 6. decembra 2008. Pridobljeno 23. novembra 2008.
- ↑ Reilly, Michael (26. maj 2007). »How Long Will it Last?«. New Scientist. 194 (2605): 38–39. Bibcode:2007NewSc.194...38R. doi:10.1016/S0262-4079(07)61508-5. ISSN 0262-4079.
- ↑ Brown, Lester (2006). Plan B 2.0. New York: W.W. Norton. str. 109. ISBN 978-0-393-32831-8.
- ↑ Kovalenko, V. I.; Yarmolyuk, V. V. (1995). »Endogenous rare metal ore formations and rare metal metallogeny of Mongolia«. Economic Geology. 90 (3): 520. doi:10.2113/gsecongeo.90.3.520. Arhivirano iz spletišča dne 5. septembra 2008.
- ↑ »Seminole Group Colombia Discovers High Grade Tin Ore in the Amazon Jungle«. FreePR101 PressRelease. Arhivirano iz prvotnega spletišča dne 26. avgusta 2014.
- ↑ »LME Tin Brands«. ITRI.co.uk. International Tin Research Institute. Arhivirano iz prvotnega spletišča dne 7. decembra 2008. Pridobljeno 5. maja 2009.
- ↑ »Agreement establishing the Association of Tin Producing Countries [1984] ATS 10«. Australasian Legal Information Institute, Australian Treaties Library.
- ↑ »12 Januari Pemasaran Perdana INATIN«. 15. december 2011. Arhivirano iz prvotnega spletišča dne 26. aprila 2012.
- ↑ 50,0 50,1 Carlin, James F., Jr. (1998).
- ↑ https://www.mining.com/tin-demand-to-decline-ita/
- ↑ Black, Harvey (2005). »Getting the Lead Out of Electronics«. Environmental Health Perspectives. 113 (10): A682–5. doi:10.1289/ehp.113-a682. PMC 1281311. PMID 16203230.
- ↑ Childs, Peter (Julij 1995). »The tin-man's tale«. Education in Chemistry. Zv. 32, št. 4. Royal Society of Chemistry. str. 92. Pridobljeno 19. junija 2018.
- ↑ »CDC - NIOSH Pocket Guide to Chemical Hazards - Tin«. www.cdc.gov. Arhivirano iz prvotnega spletišča dne 25. novembra 2015. Pridobljeno 24. novembra 2015.
Zunanje povezave[uredi | uredi kodo]
- Kositer v periodnem sistemu video posnetkov (Univerza v Nottinghamu)
- Lesena tabela periodnega sistema Theodoreja Greya : Vzorci kositra in odlitki
- Osnovne kovine: kositer Arhivirano 2012-07-12 na Wayback Machine.
- CDC - NIOSH žepni vodnik po kemijskih nevarnostih
- Kositer (USD centov na kg)



