Respiration cellulaire

La respiration cellulaire est l'ensemble des processus du métabolisme cellulaire convertissant l'énergie chimique contenue dans le glucose en adénosine triphosphate (ATP). Ces processus impliquent une succession de réactions chimiques formant des voies métaboliques qui appartiennent au catabolisme, c'est-à-dire qu'elles consistent à cliver les grosses molécules biologiques en molécules plus petites, ce qui libère de l'énergie ainsi qu'un certain nombre de déchets. Ces réactions sont globalement exothermiques, c'est-à-dire qu'elles produisent de la chaleur, la plupart étant des réactions d'oxydoréduction. De ce point de vue, la respiration s'apparente chimiquement à une combustion des nutriments, jouant le rôle de donneurs d'électrons (réducteur), en présence d'un accepteur d'électrons (oxydant).
La respiration est l'une des voies essentielles permettant aux cellules de produire de l'énergie métabolique pour leur développement et leur activité. Parmi les nutriments utilisés par les cellules des animaux et des plantes, on compte les glucides (ose), les peptides (acides aminés) et les lipides (acides gras), tandis que l'oxydant le plus fréquent dans les systèmes biologiques est l'oxygène moléculaire O2. L'énergie biochimique récupérée sous forme d'ATP peut ensuite être utilisée par des processus qui consomment de l'énergie tels que les biosynthèses, la locomotion ou encore le transport actif de substances chimiques à travers les membranes biologiques.
Respiration aérobie[modifier | modifier le code]
La respiration aérobie requiert du dioxygène O2 pour produire de l'ATP. C'est la voie prépondérante de dégradation du pyruvate, issu de la glycolyse. Celle-ci se déroule dans le cytosol, mais le pyruvate doit pénétrer dans les mitochondries pour y être entièrement oxydé par le cycle de Krebs, lequel se déroule dans la matrice mitochondriale. Le cycle de Krebs convertit le pyruvate en dioxyde de carbone CO2 et en coenzymes réduites (NADH et FADH2), coenzymes dont les électrons à haut potentiel de transfert contiennent l'essentiel de l'énergie chimique des molécules dégradées. Ces coenzymes réduites sont alors oxydées par la chaîne respiratoire dans la membrane mitochondriale interne. L'énergie des électrons à haut potentiel de transfert permet de pomper des protons hors de la matrice mitochondriale vers l'espace intermembranaire. Il s'établit un gradient de concentration de protons à travers la membrane interne, lequel génère un gradient électrochimique suffisant pour actionner l'ATP synthase, une enzyme capable de phosphoryler l'ADP en ATP grâce à l'énergie emmagasinée dans ce gradient électrochimique. On appelle phosphorylation oxydative l'ensemble formé par la chaîne respiratoire et l'ATP synthase couplés par gradient électrochimique.
Les manuels de biologie indiquent généralement que chaque molécule de glucose entièrement oxydée par la respiration cellulaire est susceptible de produire 38 molécules d'ATP : 2 ATP issus de la glycolyse, 2 ATP issus du cycle de Krebs, et 34 ATP issus de la chaîne respiratoire. Ce rendement nominal n'est cependant jamais atteint en raison des pertes par dissipation du gradient électrochimique à travers la membrane interne des mitochondries ainsi qu'en raison du coût énergétique du transport actif du pyruvate depuis le cytosol jusqu'à la matrice mitochondriale, de sorte que les estimations actuelles s'établissent autour de 30 à 32 molécules d'ATP formées par molécules de glucose oxydée[1].
La respiration aérobie est jusqu'à 15 fois plus efficace que la respiration anaérobie, qui produit seulement 2 ATP par molécule de glucose oxydée. Cependant, certains organismes anaérobie, comme les archées méthanogène, sont capables d'accroître ce rendement en utilisant d'autres accepteurs d'électrons finaux que l'oxygène.
Glycolyse[modifier | modifier le code]
La glycolyse est une voie métabolique qui se déroule dans le cytosol des cellules de pratiquement tous les êtres vivants. Elle peut fonctionner de manière aérobie ou anaérobie, c'est-à-dire respectivement en présence ou en l'absence d'oxygène. Chez l'homme, elle conduit au pyruvate en conditions aérobies et au lactate en conditions anaérobies.
En conditions aérobies, ce processus convertit une molécule de glucose en deux molécules de pyruvate, avec production concomitante de deux molécules d'ATP. Plus précisément, il commence par consommer deux molécules d'ATP pour accroître la réactivité du glucose en vue de son clivage par l'aldolase puis en produit quatre par phosphorylation au niveau du substrat, avec production de deux molécules de NADH. La réaction globale de la glycolyse peut s'écrire :
La première étape de la glycolyse est la formation de glucose-6-phosphate, à partir de glucose sous l'action de l'hexokinase, ou de glycogène sous l'action successive de la glycogène phosphorylase et de la phosphoglucomutase en passant par le glucose-1-phosphate. Le glucose-6-phosphate est ensuite isomérisé en fructose-6-phosphate par la glucose-6-phosphate isomérase et une seconde molécule d'ATP est utilisée pour phosphoryler ce dernier en fructose-1,6-bisphosphate par la phosphofructokinase-1. C'est le fructose-1,6-bisphosphate qui est clivé en deux molécules à trois atomes de carbone, qui sont chacune converties en pyruvate.
Décarboxylation du pyruvate[modifier | modifier le code]
Le pyruvate est oxydé en acétyl-CoA et NADH avec libération de CO2 à travers une décarboxylation catalysée par le complexe pyruvate déshydrogénase. Il s'agit d'un complexe de trois enzymes différentes situé dans la matrice mitochondriale des eucaryotes et dans le cytosol des procaryotes.
Cycle de Krebs (cycle de l'acide citrique)[modifier | modifier le code]
En milieu anaérobie (absence d'oxygène O2), le pyruvate issu de la glycolyse subit une fermentation, tandis que, en milieu aérobie (présence d'O2), le pyruvate issu de la glycolyse est converti en acétyl-CoA, à partir duquel il est dégradé par le cycle de Krebs dans la matrice mitochondriale pour donner deux molécules de CO2 et permettant la formation de trois molécules de NADH, une molécule de FADH2 et une molécule de GTP, équivalent à une molécule d'ATP. Le NADH et le FADH2 peuvent être oxydés par la chaîne respiratoire pour produire davantage d'ATP.
Le cycle de Krebs est un processus en dix étapes impliquant huit enzymes et diverses coenzymes. L'acétyl-CoA (composé à deux atomes de carbone, c'est-à-dire en C2) est condensé avec l'oxaloacétate (composé en C4) pour former du citrate (composé en C6), lequel est réarrangé en isocitrate, plus réactif, qui donne de l'α-cétoglutarate (composé en C5). Ce dernier donne ensuite de la succinyl-CoA (groupe en C4) puis successivement du succinate, du fumarate, du malate et, finalement, à nouveau de l'oxaloacétate.
Phosphorylation oxydative[modifier | modifier le code]
Chez les eucaryotes, la phosphorylation oxydative se déroule dans la membrane mitochondriale interne, plus précisément au niveau des crêtes de cette membrane (cristae). Elle comprend la chaîne respiratoire, qui assure l'oxydation des coenzymes réduites par le cycle de Krebs, et l'ATP synthase, enzyme capable de phosphoryler l'ADP en ATP à partir de l'énergie libérée par la chaîne respiratoire au cours de l'oxydation des coenzymes. Cette énergie est emmagasinée sous forme de gradient électrochimique à travers la membrane interne de la mitochondrie sous l'effet de pompes à protons qui génèrent un gradient de concentration de protons au cours de la circulation des électrons le long de la chaîne respiratoire. L'étape finale de cette dernière est la réduction d'une molécule d'oxygène par quatre électrons pour former deux molécules d'eau en fixant quatre protons.
Rendement énergétique de la respiration aérobie[modifier | modifier le code]
Le tableau ci-dessous résume les étapes qui produisent de l'ATP et des coenzymes réduites lors de l'oxydation complète d'une molécule de glucose en CO2 et H2O.
| Étape | Coenzymes produites | ATP produits | Source d'ATP |
|---|---|---|---|
| Phase préparatoire de la glycolyse | −2 | La conversion du glucose en fructose-1,6-bisphosphate consomme deux molécules d'ATP du cytoplasme | |
| Phase finale de la glycolyse | 4 | Phosphorylation au niveau du substrat | |
| 2 NADH | 6 | Phosphorylation oxydative : chaque molécule de NADH donne 1,5 molécule d'ATP et non 2,5 ATP en raison du transport actif du NADH jusqu'à la matrice mitochondriale. | |
| Décarboxylation du pyruvate | 2 NADH | 6 | Phosphorylation oxydative |
| Cycle de Krebs | 2 | Phosphorylation au niveau du substrat | |
| 6 NADH | 18 | Phosphorylation oxydative | |
| 2 FADH2 | 4 | Phosphorylation oxydative | |
| Production totale | 38 ATP | Par oxydation complète d'une molécule de glucose en dioxyde de carbone et oxydation de toutes les coenzymes réduites jusqu'à formation d'eau. | |
Le rendement théorique de l'oxydation complète d'une molécule de glucose au cours de la respiration cellulaire est de 38 molécules d'ATP mais est rarement atteint en raison de différentes pertes d'énergie telles que le transport actif du pyruvate produit dans le cytosol par la glycolyse jusque dans la matrice mitochondriale pour être dégradé par le cycle de Krebs après décarboxylation en acétyl-CoA, ou encore :
- par le transport actif du phosphate dans la mitochondrie par la protéine SLC25A3 (en), qui fonctionne comme un antiport échangeant des ions phosphate H2PO4− contre des ions hydroxyde OH− ou comme un symport avec les protons H+ en utilisant la force proton-motrice générée par la chaîne respiratoire.
- par le transport actif de l'ADP et de l'Adénosine triphosphate à travers la membrane mitochondriale interne par la translocase ATP/ADP, un antiport qui utilise également la force proton-motrice par le fait que l'ATP possède une charge électrique de –4 tandis que l'ADP n'a qu'une charge électrique de –3 : l'ATP sort de la mitochondrie en dissipant le gradient électrochimique généré par la chaîne respiratoire.
Le résultat de ces différents processus de transport actif utilisant la force proton-motrice et le gradient électrochimique générés par la chaîne respiratoire est que plus de trois protons sont nécessaires pour produire une molécule d'ATP par phosphorylation oxydative. C'est la raison pour laquelle la production maximum d'ATP par molécule de glucose entièrement oxydée ne dépasse pas 30 molécules[1].
En pratique, ce rendement peut même être encore réduit en raison de fuites de protons à travers la membrane mitochondriale interne[2].
D'autres facteurs sont également susceptibles de dissiper le gradient de concentration de protons autour de la membrane interne de la mitochondrie, ce qui représente une dissipation d'énergie supplémentaire et induit donc une baisse du rendement énergétique global de l'oxydation de cette molécule de glucose. C'est par exemple le cas d'une protéine, la thermogénine, exprimée dans certains types de cellules et qui a pour effet de transporter des protons à travers la membrane mitochondriale interne, laquelle leur est normalement imperméable. En dissipant le gradient de concentration de protons, cette protéine découple les deux composantes de la phosphorylation oxydative : l'énergie libérée par la chaîne respiratoire sous forme d'un gradient électrochimique n'est plus utilisée pour produire de l'ATP en phosphorylant l'ADP mais est simplement convertie en chaleur. Ceci est particulièrement important pour la thermogenèse dans le tissu adipeux brun chez les mammifères en hibernation.
Fermentation[modifier | modifier le code]

En milieu anaérobie, c'est-à-dire en l'absence d'oxygène, le pyruvate issu de la glycolyse n'est pas transporté dans les mitochondries mais demeure dans le cytosol, où il est converti en déchets susceptibles d'être éliminés de la cellule. Ce processus permet d'oxyder les coenzymes réduites au cours de la glycolyse afin de permettre à celle-ci de se poursuivre.
Dans le muscle squelettique, la fermentation convertit le pyruvate en lactate (acide lactique) : c'est la fermentation lactique. Elle survient lorsque le catabolisme demandé par l'effort physique dépasse les capacités de la chaîne respiratoire, ce qui conduit le cytosol à fonctionner de façon anaérobie : en l'absence d'oxygène, le pyruvate joue le rôle d'accepteur d'électrons sous l'action de la lactate déshydrogénase :
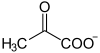
|
+ NADH + H+ NAD+ + | 
|
| Pyruvate | L-Lactate | |
| Lactate déshydrogénase – EC | ||
Le lactate peut également être utilisé par le foie pour produire du glycogène.
Chez la levure, il se produit une fermentation différente, appelée fermentation alcoolique, qui aboutit à la formation d'éthanol et de CO2 sous l'action successive de la pyruvate décarboxylase et de l'alcool déshydrogénase par l'intermédiaire de l'acétaldéhyde (voir ci-contre).
Le rendement énergétique de la fermentation est sensiblement inférieur à celui de la respiration aérobie : seules deux molécules d'ATP sont produites par molécule de glucose fermentée. Ceci vient du fait que les produits de la fermentation sont encore riches en énergie : l'éthanol, par exemple, est un combustible susceptible d'être utilisé comme biocarburant à la place de l'essence pour alimenter des moteurs à combustion interne — on parle de bioéthanol. L'avantage, cependant, est que l'ATP produit au cours de la glycolyse est disponible plus rapidement pour couvrir les besoins énergétiques de la cellule que celui issu de la phosphorylation oxydative.
Respiration anaérobie[modifier | modifier le code]
La respiration anaérobie est une forme de respiration cellulaire utilisant comme accepteur final d'électrons une autre substance que l'oxygène. Comme la respiration aérobie, elle utilise une chaîne respiratoire, mais celle-ci fonctionne sans oxygène. À la place de ce dernier interviennent d'autres accepteurs d'électrons, moins oxydants, tels que les ions sulfate SO42− ou nitrate NO3−, ou encore le soufre S ou le fumarate.
Cette forme de respiration cellulaire est utilisée essentiellement par des procaryotes vivant dans des milieux dépourvus d'oxygène. De nombreux organismes anaérobies sont tués par l'oxygène : on dit que ce sont des anaérobies obligatoires.
Notes et références[modifier | modifier le code]
- (en) P. R. Rich, « The molecular machinery of Keilin's respiratory chain », Biochemical Society Transactions, vol. 31, no 6, , p. 1095-1105 (PMID 14641005, DOI 10.1042/bst0311095, lire en ligne)
- (en) R. K. Porter et M. D. Brand, « Mitochondrial proton conductance and H+/O ratio are independent of electron transport rate in isolated hepatocytes », Biochemical Journal, vol. 310, no Pt 2, , p. 379-382 (PMID 7654171, PMCID 1135905, DOI 10.1042/bj3100379, lire en ligne)

