Radioactivité


La radioactivité est le phénomène physique par lequel des noyaux atomiques instables (dits radionucléides ou radioisotopes) se transforment spontanément en d'autres atomes (désintégration) en émettant simultanément des particules de matière (électrons, noyaux d'hélium, neutrons, etc.) et de l'énergie (photons et énergie cinétique). La radioactivité a été découverte en 1896 par Henri Becquerel dans le cas de l'uranium, et très vite confirmée par Marie Curie pour le radium.
L'émission de particules matérielles et immatérielles est appelée rayonnement, et l'énergie des particules est suffisante pour entraîner l'ionisation de la matière traversée, d'où le nom de rayonnements ionisants. On distingue classiquement les rayons α constitués de noyaux d'hélium (également appelés particules α), les rayons β constitués d'électrons (particules β) et les rayons γ constitués de photons, auxquels il faut ajouter les neutrons qui dérivent des fissions spontanées.
Les effets sur un organisme vivant d'une exposition aux rayonnements ionisants (irradiation) dépendent du niveau et de la durée de l'exposition (aiguë ou chronique), de la nature du rayonnement ainsi que de la localisation de la radioactivité (exposition externe, interne, en surface, etc.).
Les rayonnements provenant de substances radioactives sont largement utilisés dans l'industrie pour le contrôle de pièces manufacturées, les soudures, l'usure, et en médecine nucléaire à des fins de diagnostic à faible dose, et à des fins thérapeutiques à forte dose pour soigner les cancers. Lors des différents usages de la radioactivité, il convient naturellement de suivre les mesures de prévention, de protection et de contrôle adaptées au niveau de radioactivité.
Histoire
La radioactivité fut découverte en 1896 par Henri Becquerel (1852-1908), lors de ses travaux sur la phosphorescence : les matières phosphorescentes émettent de la lumière dans le noir après expositions à la lumière, et Becquerel supposait que la lueur qui se produit dans les tubes cathodiques exposés aux rayons X pouvait être liée au phénomène de phosphorescence. Son expérience consistait à sceller une plaque photographique dans du papier noir et mettre ce paquet en contact avec différents matériaux phosphorescents. Tous ses résultats d'expérience furent négatifs, à l'exception de ceux faisant intervenir des sels d'uranium, lesquels impressionnaient la plaque photographique à travers la couche de papier. Cependant, il apparut bientôt que l'impression de l'émulsion photographique n'avait rien à voir avec le phénomène de phosphorescence, car l'impression se faisait même lorsque l'uranium n'avait pas été exposé à la lumière au préalable. Par ailleurs, tous les composés d'uranium impressionnaient la plaque, y compris les sels d'uranium non phosphorescents et l'uranium métallique. De plus les physiciens Julius Elster (en) et Hans Gleiter (en) montrent dès 1898 que le phénomène n'est sensible ni à la température, ni à la pression ni à un bombardement d'électrons[1]. À première vue, ce nouveau rayonnement était semblable au rayonnement X, découvert l'année précédente (en 1895) par le physicien allemand Wilhelm Röntgen (1845-1923). Des études ultérieures menées par Becquerel lui-même, ainsi que par Marie Curie (1867-1934) et Pierre Curie (1859-1906), ou encore par Ernest Rutherford (1871-1937), montrèrent que la radioactivité est nettement plus complexe que le rayonnement X. En particulier, ils découvrirent qu'un champ électrique ou magnétique séparait les rayonnements « uraniques » en trois faisceaux distincts, qu'ils baptisèrent α, β et γ. La direction de la déviation des faisceaux montrait que les particules α étaient chargées positivement, les β négativement, et que les rayonnements γ étaient neutres. En outre, la magnitude de la déflexion indiquait nettement que les particules α étaient bien plus massives que les β.
- Reproduction de l'expérience de Becquerel.
-
Section polie de pechblende.
-
Papier photographique impressionné par le rayonnement de la pechblende.
En faisant passer les rayons α dans un tube à décharge et en étudiant les raies spectrales ainsi produites, on pouvait conclure que le rayonnement α est constitué d'hélions, autrement dit de noyaux d'hélium (4He). D'autres expériences permettaient d'établir que les rayons β sont composés d'électrons comme les particules dans un tube cathodique, et que les rayons γ sont, tout comme les rayons X, des photons très énergétiques. Par la suite, on découvrit que de nombreux autres éléments chimiques ont des isotopes radioactifs. Ainsi, en traitant des tonnes de pechblende, une roche uranifère, Marie Curie réussit à isoler quelques milligrammes de radium dont les propriétés chimiques sont tout à fait similaires à celles du baryum (ces deux éléments chimiques sont des métaux alcalino-terreux), mais qu'on arrive à distinguer à cause de la radioactivité du radium.

Les dangers des rayonnements ionisants pour la santé ne furent pas immédiatement reconnus. Ainsi, Nikola Tesla (1856-1943), en soumettant volontairement en 1896 ses propres doigts à une irradiation par des rayons X, constata que les effets aigus de cette irradiation étaient des brûlures qu'il attribua, dans une publication, à la présence d'ozone. D'autre part, les effets mutagènes des radiations, en particulier les risques de cancer, ne furent découverts qu'en 1927 par Hermann Joseph Muller (1890-1967). Avant que les effets biologiques des radiations ne soient connus, des médecins et des sociétés attribuaient aux matières radioactives des propriétés thérapeutiques : le radium, en particulier, était populaire comme tonifiant, et fut prescrit sous forme d'amulettes ou de pastilles. Marie Curie s'est élevée contre cette mode, arguant que les effets des radiations sur le corps n'étaient pas encore bien compris. Durant les années 1930, les nombreuses morts qui ont semblé pouvoir être reliées à l'utilisation de produits contenant du radium ont fait passer cette mode.
Diversité des radioisotopes
Les radioisotopes les plus fréquents dans les roches terrestres sont l'isotope 238 de l'uranium (238U), l'isotope 232 du thorium (232Th), et surtout l'isotope 40 du potassium (40K). Outre ces isotopes radioactifs naturels encore relativement abondants, il existe dans la nature des isotopes radioactifs nettement plus rares. Il s'agit notamment des éléments instables produits lors de la suite de désintégrations des isotopes mentionnés, par exemple de divers isotopes du radium et du radon.
Un des radioisotopes naturels les plus utilisés par l'homme est l'isotope 235 de l'uranium (235U) qui se trouve dans la nature en faible proportion (moins de 1 %) associé à l'isotope 238U, mais dont on modifie la proportion par des techniques d'enrichissement de l'uranium pour qu'il puisse servir de combustible pour la production d'énergie nucléaire et d'explosif pour la production de bombes atomiques.
Un autre radioisotope naturel est le radiocarbone, c'est-à-dire l'isotope 14 du carbone (14C). Ce dernier est constamment produit dans la haute atmosphère par des rayons cosmiques interagissant avec l'azote, et se détruit par désintégrations radioactives à peu près au même taux qu'il est produit, de sorte qu'il se produit un équilibre dynamique qui fait que la concentration du 14C reste plus ou moins constante au cours du temps dans l'air et dans les organismes vivants qui l'ingèrent (photosynthèse, nutrition, etc.). Une fois l'organisme mort, la concentration en 14C diminue dans ses tissus, et permet de dater le moment de la mort. Cette datation au radiocarbone est un outil de recherche très prisé en archéologie et permet de dater avec une bonne précision des objets organiques dont l'âge ne dépasse pas 50 000 ans.
Transformations nucléaires
La « désintégration » (en physique, elle correspond à la transformation de la matière en énergie) d'un noyau radioactif peut entraîner l'émission de rayonnement α, β- ou β+. Ces désintégrations sont souvent accompagnées de l'émission de photons de haute énergie ou rayons gamma, dont les longueurs d'onde sont généralement encore plus courtes que celles des rayons X, étant de l'ordre de 10−11 m ou inférieures. Cette émission gamma (γ) résulte de l'émission de photons lors de transitions nucléaires : du réarrangement des charges internes du noyau nouvellement formé, ou bien de la couche profonde du cortège électronique perturbé, à partir de niveaux d'énergie excités avec des énergies mises en jeu de l'ordre du MeV.
Atomes et noyaux radioactifs
Comme tous les atomes, un atome radioactif est composé d'un noyau lui-même composé de nucléons : neutrons et protons et d'un cortège d'électrons circulants à bonne distance du noyau en nombre égal à celui des protons. L'atome radioactif est équilibré en charge électrique.
Un atome radioactif contient un noyau instable dont le nombre de nucléons ou la composition relative en protons et neutrons ne correspond pas à une situation stable. Le noyau de l'atome radioactif cherche à rallier la configuration stable la plus proche de sa composition en émettant des particules.
Situations d'instabilité du noyau d'un atome radioactif
Par rapport au noyau de l'atome stable le plus voisin, le noyau de l'atome radioactif peut se trouver dans l'une des trois situations suivantes :
- en excès de nucléons ;
- en excès de neutrons ;
- en excès de protons.
Si le noyau est en excès de nucléons, il émet des particules alpha, c'est-à-dire un groupe de 4 nucléons = 2 neutrons + 2 protons. Au cours de son transit vers l'extérieur de l'atome au travers du cortège électronique la particule alpha chargée positivement capte (ou non) deux électrons. Si cela n'a pas été le cas elle capte deux électrons auprès des atomes voisins et les deux électrons excédentaires de l'atome initial compensent le bilan électrique total qui reste neutre. C'est le rayonnement alpha. L'énergie du rayonnement est majoritairement constituée par l'énergie cinétique de la particule alpha qui est une particule massive, sachant que dans l'expulsion de cette particule la quantité de mouvement est également conservée, une énergie cinétique non négligeable est communiquée au reste du noyau en désintégration.
Si le noyau est en excès de neutrons, il transforme un neutron en proton et émet un électron ; cet électron chargé négativement traverse le cortège électronique de l'atome et continue sa route. C'est le rayonnement bêta. Cette façon de faire est plus « économique » que celle consistant à émettre un neutron, puisqu'on gagne sur les deux plateaux de la balance pour rallier la proportion stable neutron/proton. Le bilan électrique global reste équilibré puisque la charge négative de l'électron émis est compensée par la charge positive augmentée du noyau. L'énergie du rayonnement est constituée par l'énergie cinétique de l'électron expulsé dont la masse est faible devant celle du noyau en désintégration et par un rayonnement électromagnétique associé au réarrangement du cortège électronique autour du noyau désintégré.
Si le noyau est en excès de protons, de façon similaire à l'excès de neutrons, il transforme un proton en neutron en émettant un positron (un anti-électron). Au cours de son transit vers l'extérieur le positron finit par interagir avec un électron, provoquant l'annihilation du couple électron/positron en une paire de photons γ. C'est un exemple de rayonnement électromagnétique pur.
Cas rarissimes
En cas rarissime de « super-excès » de neutrons le noyau peut émettre directement des neutrons (particule non chargée donc capable de traverser le cortège électronique) comme typique les fragments de fission émetteurs de neutrons retardés.
Rayonnement électromagnétique
Les transmutations ci-dessus s'accompagnent généralement d'un réarrangement du cortège électronique qui se traduit par l'émission par l'atome d'un rayonnement électromagnétique (des photons) d'énergie variable.
Situation stable - vallée de stabilité
La situation stable des noyaux des atomes peut se définir de façon simple de la façon suivante :
- d'une part la proportion de neutrons et protons = N/Z ne s'écarte pas fortement d'une valeur dépendant du nombre total de nucléons A dans les conditions suivantes :
- si A ≤ 45, N/Z = 1
- si A > 45, N/Z = 1,8 - 50,4/(A + 18) ; par exemple pour A = 90, N/Z = 1,33 ; pour A = 206, N/Z = 1,575[Note 1]
- d'autre part le nombre total de nucléons n'excède pas 208.
Particules émises par les corps radioactifs
Les corps radioactifs dont la période est supérieure à quelques minutes :
- n'émettent aucun neutron ni proton qui sont pourtant les nucléons de base constitutifs des noyaux des atomes ;
- mais uniquement en termes de particules des électrons ou des particules alpha (4 nucléons) ;
- accompagnés d'un rayonnement électromagnétique s'il y a réarrangement concomitant du cortège électronique autour du noyau.
Un corps radioactif peut voir son nombre de nucléons changer/diminuer uniquement par groupe de 4 nucléons (deux protons + 2 neutrons) en émettant une particule alpha (un noyau d'hélium).
Par exemple, les produits de fission radioactifs se trouvent tous en excès de neutrons immédiatement après leur naissance par fission. Quelques minutes après l'instant de la fission, ils sont tous devenus des corps radioactifs qui rallient la stabilité :
- sans modification de leur nombre initial total de nucléons ;
- uniquement en émettant des électrons et en transformant par le fait leurs neutrons excédentaires en protons ;
- ceci accompagné éventuellement d'un rayonnement électromagnétique.
Transformations isobariques
Une transformation isobarique correspond à la transmutation d'un noyau avec la conservation du nombre de masse A. La transformation isobarique est le cas le plus courant de radioactivité bêta et gamma. Les seules transmutations non isobariques s'effectuent par groupe de 4 nucléons ; c'est le rayonnement alpha. Seul dans le cas rarissime des fragments de fission émetteurs de neutrons retardés, un noyau pourtant composé de protons et de neutrons ne peut perdre de nucléons en émettant des protons ou des neutrons. Un noyau ne peut perdre des nucléons que par groupe de quatre en émettant une particule alpha donc un noyau d'hélium.
Émissions bêta
Émission bêta moins

La radioactivité bêta moins (β-) affecte les nucléides X présentant un excès de neutrons. Elle se manifeste lors de réactions isobariques par la transformation dans le noyau d'un neutron en proton, le phénomène s'accompagnant de l'émission d'un électron (ou particule bêta moins) et d'un antineutrino électronique νe :
À l'intérieur du noyau, un neutron se transforme (la radioactivité β- concerne en effet les noyaux trop riches en neutrons) :
Émission bêta plus
La radioactivité bêta plus (β+) ne concerne que les nucléides présentant un excès de protons. Elle se manifeste par la transformation dans le noyau d'un proton en neutron, le phénomène s'accompagnant de l'émission d'un positron (ou positon, encore appelé particule bêta plus = anti-électron) et d'un neutrino électronique νe :
L'émission d'un rayonnement β+ par un noyau n'est possible que si l'énergie disponible est supérieure à 1,022 MeV. Car le bilan énergétique, qui est la différence entre l'énergie initiale et l'énergie finale donne :, où est négligeable, puisque de l'ordre de quelques eV.
, avec et les énergies des atomes X et Y.
.
La réaction n'est donc possible que si c'est-à-dire que si .
Capture électronique
La capture électronique (ε), capture par le noyau de l'un des électrons du cortège électronique, ne concerne que des nucléides qui présentent un excès de protons et dont l'énergie disponible (dans la réaction potentielle) n'est pas nulle.
Très rarement, ce sont deux électrons du cortège qui sont capturés :
Émission alpha
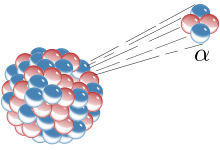
On parle[2] de radioactivité alpha (α) pour désigner l'émission d'un noyau d'hélium ou hélion :
- .
Ces hélions, encore appelés particules alpha, ont une charge 2e, et une masse de 4,001 505 8 unités de masse atomique.
Loi de désintégration radioactive
Un radioisotope quelconque a autant de chances de se désintégrer à un moment donné qu'un autre radioisotope de la même espèce, et la désintégration ne dépend pas des conditions physico-chimiques dans lesquelles le nucléide se trouve. En d'autres termes, la loi de désintégration radioactive est une loi statistique.
Soit le nombre de radionucléides d'une espèce donnée présents dans un échantillon à un instant quelconque. Comme la probabilité de désintégration d'un quelconque de ces radionucléides ne dépend pas de la présence des autres espèces de radionucléides ni du milieu environnant, le nombre total de désintégrations pendant un intervalle de temps est proportionnel au nombre de radionucléides de même espèce présents et à la durée de cet intervalle :
- .
Le signe moins (–) vient de ce que diminue au cours du temps, la constante (caractéristique du radionucléide étudié) étant positive.
En intégrant l'équation différentielle précédente, on trouve la loi de décroissance exponentielle du nombre de radionucléides présents dans le corps à un instant quelconque, en appelant le nombre des radionucléides présents à l'instant :
- .
La demi-vie est la durée au bout de laquelle la moitié d'un échantillon radioactif est désintégrée, le nombre de noyaux fils atteignant la moitié du nombre de noyaux pères. On montre que :
- .
- Première démonstration
Par définition de
- Seconde démonstration
Interaction entre les rayonnements et la matière
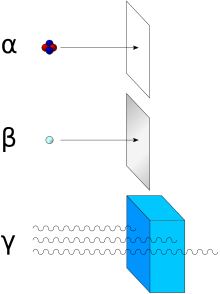
Les particules α sont arrêtées par une feuille de papier.
Les particules β sont arrêtées par une feuille d'aluminium.
Le rayonnement γ est atténué (mais jamais arrêté) par de grandes épaisseurs de matériaux denses (écran en plomb, par exemple).
Action locale des rayonnements
Les rayonnements ionisants provoquent tous au sein de la matière des ionisations et des excitations. La façon dont se produisent ces ionisations dépend du type de rayonnement considéré :
- rayonnement α : un noyau atomique instable émet une particule lourde chargée positivement constituée de deux protons et de deux neutrons (noyau d'hélium 4). En traversant la matière, cette particule interagit principalement avec le cortège électronique des atomes du matériau traversé, ce qui les excite ou les ionise. Ce mécanisme se produit sur une très courte distance car la section efficace d'interaction est élevée : le pouvoir de pénétration des rayonnements alpha est faible (une simple feuille de papier ou 4 à 5 cm d'air les arrêtent totalement) et par conséquent le dépôt d'énergie par unité de longueur traversée sera élevé. Cette énergie dissipée dans la matière traversée se traduira par des excitations et des ionisations et donne lieu à des rayonnements secondaires.
- rayonnement β- : un noyau atomique instable émet une particule légère et chargée négativement (un électron) qu'une feuille d'aluminium peut arrêter. Cependant ce rayonnement interagit avec la matière en provoquant des excitations et des ionisations par diffusion. Le parcours des électrons dans la matière est plus important que celui des particules alpha (de l'ordre de quelques mètres maximum dans l'air). La perte d'énergie du rayonnement bêta par unité de longueur traversée sera, toute autre chose étant égale, moindre que celle du rayonnement alpha. Il en sera donc de même du nombre d'excitation et d'ionisation produite par unité de longueur. Dans certains cas (électron de forte énergie et matériau traversé de masse atomique élevée) l'émission d'un rayonnement de freinage électromagnétique est possible.
- rayonnement β+ : un noyau atomique instable émet une particule légère et chargée positivement (un positron) qui interagit, après avoir été ralenti, avec un électron du milieu provoquant son annihilation et la production de deux rayons gamma de 511 keV chacun.
- rayonnement γ : un noyau atomique qui ne souffre pas d'un déséquilibre baryonique, mais qui se trouve dans un état d'énergie instable, émet un photon très énergétique, donc très pénétrant, pour atteindre un état d'énergie stable ; il faut environ 1 à 5 centimètres de plomb pour l'absorber[3]. Il n'y a guère de différence entre les rayons X durs et le rayonnement γ — seul leur origine les différencie. En général, l'émission de rayons γ suit une désintégration α ou β, car elle correspond à un réarrangement des nucléons, et notamment à une réorganisation de la charge électrique à l'intérieur du nouveau noyau. On rencontre donc fréquemment un noyau radioactif émettant simultanément plusieurs types de rayonnements : par exemple, l'isotope 239 du plutonium (239Pu) est un émetteur α–γ, l'isotope 59 du fer (59Fe) est un émetteur β–γ. Le rayonnement gamma est un faisceau de photons sans charge électrique ni masse. En traversant la matière, il provoque trois types d'interactions :
- l'effet photoélectrique ;
- la création de paires ;
- l'effet Compton.
- Ces mécanismes produiront, in fine, des excitations et ionisations dans le matériau traversé. Le rayonnement gamma et les neutrons ont un fort pouvoir de pénétration dans la matière, plusieurs décimètres de béton pour le rayonnement γ ; un écran en plomb d'une épaisseur de 50 mm arrête 90 % du rayonnement γ (« écran dixième »).
- Rayonnement neutronique : la fission nucléaire et la fusion nucléaire produisent des neutrons en quantités importantes. Ces neutrons se diffusent dans l'environnement du réacteur. Ils nécessitent des protections neutroniques et des compteurs dosimétriques spécialisés.
La nature des lois physiques permettant de calculer les parcours ou l'atténuation des rayonnements dans la matière est différente selon les rayonnements considérés :
- les rayonnements gamma et les flux neutroniques ne sont jamais complètement arrêtés par la matière. C'est pourquoi le flux de photons émergeant d'un écran sera faible, voire quasi-indétectable, mais jamais nul. Voir Couche de demi-atténuation ;
- les lois physiques qui traduisent le parcours des rayonnements alpha et bêta montrent qu'au-delà d'une certaine distance, il est impossible que des particules puissent être retrouvées : le rayonnement incident peut donc être complètement bloqué par un matériau qui joue le rôle d'écran. Voir Parcours d'une particule.
Les défauts cristallins induits par ces rayonnements peuvent servir à dater la formation des minéraux riches en éléments radioactifs comme l'uranium et le thorium, s'ils ne sont pas trop nombreux (c'est-à-dire, s'ils peuvent être repérés individuellement), grâce aux traces de fission qu'ils laissent dans les cristaux.
Action globale
- Quand un minéral riche en éléments radioactifs s'est formé depuis un temps significatif comparé aux demi-vies de ces éléments, l'accumulation des défauts induits peut transformer le matériau cristallin en un matériau amorphe ; c'est ce qu'on appelle la métamictisation. C'est notamment le cas de certains zircons vieux de plus de 500 Ma.
- L'accumulation des perturbations locales est délétère pour les organismes vivants, soit à long terme par le développement d'un cancer (Marie Curie, notamment, est morte d'une leucémie radio-induite), soit à plus court terme, en cas d'exposition intense ou prolongée, sous la forme d'un syndrome d'irradiation aiguë (bombardements atomiques d'Hiroshima et Nagasaki, catastrophe nucléaire de Tchernobyl).
- L'énergie libérée par la radioactivité est partiellement consommée par les transformations locales induites par le rayonnement, mais l'essentiel est en définitive transformé en chaleur[4]. La chaleur libérée par la radioactivité est fondamentale pour :
- l'activité géologique des planètes telluriques (la Terre et Vénus jusqu'à aujourd'hui, Mars et peut-être la Lune dans le passé). Il s'agit surtout de l'énergie libérée par la décomposition radioactive de l'uranium (isotopes 235U et 238U), du thorium (232Th) et du potassium (via son isotope radioactif 40K) ;
- la différenciation des petits corps formés suffisamment tôt, en comparaison des demi-vies d'isotopes de courte demi-vie mais initialement abondants, comme 26Al et 60Fe.
Mesure de la radioactivité (grandeurs et unités)
Grandeurs objectives
Ces grandeurs objectives sont mesurables à l'aide d'appareils de physique (compteurs, calorimètres, horloges).
- L'activité d'une source radioactive se mesure en becquerels (Bq), unité correspondant au nombre de désintégrations par seconde, nommée en hommage à Henri Becquerel. On utilise quelquefois (en biologie par exemple) le nombre de désintégrations par minute.
- L'activité massique ou volumique est plus souvent utilisée. Elle correspond à l'activité rapportée à la masse (Bq/kg) ou au volume de l'échantillon mesuré (Bq/L ou Bq/m3).
- Le curie (Ci) était autrefois utilisé : il se définit comme l'activité d'un gramme de radium, soit 37 GBq (37 × 109 désintégrations par seconde), donc 37 Bq = 1 nCi.
- Le coulomb par kilogramme (C/kg) peut également être utilisé : il mesure l'exposition aux rayonnements X et gamma (la charge d'ions libérée dans la masse d'air). L'ancienne unité équivalente était le röntgen qui correspond au nombre d'ionisations par kilogramme d'air.
- Pour le radon, l'énergie alpha potentielle volumique (EAPV) peut être mesurée en joules par mètre cube (J/m3). Cela correspond à l'énergie des particules alpha émises dans un certain volume par les descendants du radon.
Conversion des différentes unités objectives :
Grandeurs subjectives
Ce sont des grandeurs non mesurables directement. Elles sont estimées à partir de mesures et de coefficients de pondération définis par la CIPR.
- La dose absorbée par la cible est définie comme l'énergie reçue par unité de masse de la cible, en joules par kilogramme, c'est-à-dire en grays (Gy) dans le système SI. L'ancienne unité était le rad. 1 Gy = 100 rad. On définit également un débit de dose, c'est-à-dire l'énergie absorbée par kilogramme et par unité de temps, mesurée en grays par seconde (Gy/s).
- La dose équivalente, H, pour laquelle chaque rayonnement doit être pondéré pour tenir compte de sa nocivité respective. L'unité du Système International (SI) est le sievert (Sv). Lorsque le rad était utilisé comme unité de dose absorbée, l'unité de dose équivalente était le rem, acronyme de « röntgen equivalent man ».
- La dose efficace, E, est la somme pondérée des doses équivalentes aux organes et tissus T irradiés. Elle rend compte du risque d'apparition de cancer. L'unité utilisée est également le sievert.
Chiffres à considérer avec précaution (non sourcés) :
Le facteur de risque d'induction de cancer est estimé à 4 % par Sv pour une population de travailleurs et à 5 % par Sv pour la population en général. À titre de comparaison, les personnes vivant en Europe occidentale reçoivent une dose annuelle naturelle de 3 mSv dont la moitié est due au radon.
- L'équivalent de dose ambiant, H*(10), est une grandeur opérationnelle exprimée en mSv. C'est une mesure approchante de la dose efficace externe, utilisée pour les mesures de l'environnement.
- L'équivalent de dose individuel, Hp.2 810), est une grandeur opérationnelle exprimée en mSv. C'est une mesure approchante de la dose efficace externe, utilisée pour les mesures de l'exposition des personnes aux radiations ionisantes dans le cadre de leur profession.
Conversion des différentes unités subjectives :
- 1 rad = 0,01 Gy
- 1 Gy = 100 rad
- 1 rem = 0,01 Sv = 10 mSv
- 1 Sv = 100 rem
Les réseaux de mesures
Des réseaux de mesures (plus ou moins organisés, complets et accessibles au public, selon les pays) couvrent une partie du territoire de nombreux pays, pour mesurer les variations de radioactivité dans l'eau, l'air, la flore, la faune (domestique ou sauvage, dont espèces-gibier[5]), les aliments, etc.
En France, depuis février 2010, l'ASN a réuni l'essentiel de ces réseaux (l'équivalent d'environ 15 000 mesures mensuelles depuis début 2009) en un seul portail, le Réseau national de mesures de la radioactivité de l'environnement[6], « […] de manière à faciliter l'accès […] aux résultats des mesures tout en renforçant l’harmonisation et la qualité des mesures effectuées par les laboratoires ». Un site Internet du Réseau national de mesure de la radioactivité dans l’environnement (RNM)[7], est également ouvert depuis le 1er janvier 2010, notamment alimenté par l'IRSN[8].
Origines de la radioactivité
| Nature de la source | Exposition humaine à la radioactivité selon l'OMS[9] | ||
|---|---|---|---|
| mSv par personne et par an | Radioactivité naturelle en % | Radioactivité artificielle en % | |
| Radon (gaz radioactif naturel dense souvent présent dans les rez-de-chaussées) | |||
| Irradiation d'origine médicale (radiographies, scanners, radiothérapies, etc.) | |||
| Éléments absorbés par alimentation (essentiellement du potassium 40 contenu naturellement dans les aliments) | |||
| Rayonnement cosmique | |||
| Rayonnement interne | |||
| Autres origines artificielles sauf énergie nucléaire civile (industries minières diverses, retombées atmosphériques des essais nucléaires militaires, instruments de mesure, certaines méthodes de mesure industrielles (telles le contrôle de soudures par gammagraphie), etc.) | |||
| Énergie nucléaire civile | |||
| Total | |||
Selon une étude de Billon S. et Al[10], l'exposition naturelle à la radioactivité représenterait environ 2,5 mSv sur un total de 3,5. Cette dose peut varier de 1 à 40 mSv, selon l'environnement géologique et les matériaux d'habitation. Il existe aussi le rayonnement interne du corps : la radioactivité naturelle des atomes du corps humain se traduit par environ 8 000 désintégrations par seconde (8 000 Bq). Ce taux est principalement dû à la présence de carbone 14 et de potassium 40 dans notre organisme.
On parle de « radioactivité naturelle » pour désigner les sources non produites par les activités humaines, comme celle issue du radon, de la terre, ou du rayonnement cosmique. A contrario, on parle de « radioactivité artificielle » pour désigner la radioactivité due à des sources produites par les activités humaines : réalisation d'examens médicaux (tels les radiographies, tomodensitométries, scintigraphies, radiothérapies), éléments transuraniens synthétiques, concentrations artificiellement élevées de matières radioactives ou production artificielle de rayons gamma (dans un accélérateur de particules, par exemple). Physiquement, il s'agit exactement du même phénomène.
Radioactivité naturelle
La principale source de radioactivité est représentée par les radioisotopes existants dans la nature et produits lors des explosions des supernovas. On trouve des traces de ces éléments radioactifs et de leurs descendants dans tout notre environnement : un roc de granite contient des traces d'uranium qui, en se désintégrant, émettent du radon.
Les isotopes qui ont subsisté depuis la formation de notre système solaire sont ceux dont la période radioactive est très longue : pour l'essentiel, l'uranium et le thorium. Du fait de leur durée de vie très longue, leur activité massique est nécessairement très faible, et ces composés naturels ne constituent généralement pas un danger important en termes de radiotoxicité justifiant des mesures de radioprotection.
Le rayonnement tellurique dû aux radionucléides présents dans les roches (uranium, thorium et descendants) est d'environ 0,50 mSv par an en France[10]. Il peut cependant être bien plus important dans certaines régions où la roche est très concentrée en uranium (régions granitiques telles la Forêt-Noire en Allemagne, la Bretagne et le Massif central en France) ou en thorium (région du Kérala en Inde).
Au rayonnement dû aux éléments de longue durée de vie s'ajoute celui des radioisotopes qui forment leur chaîne de désintégration. Ces éléments sont généralement à demi-vie beaucoup plus courte, mais de ce fait, ils ne sont présents qu'en quantité très faible : les lois de la décroissance radioactive font qu'à l'« équilibre séculaire », leur activité est la même que celle de l'élément père.
Parmi ces descendants il faut citer la présence d'un gaz radioactif dense : le radon. Du fait de sa volatilité, il est susceptible de migrer dans l'atmosphère et est ainsi responsable à lui seul de la plus grande part de l'exposition humaine moyenne à la radioactivité : 42 % du total. Il est issu de la désintégration de l'uranium naturellement contenu dans les sols. Dans les régions où la concentration en uranium dans la roche est élevée, il est souvent présent dans les habitations peu ventilées, ou construites sur des sols à fort dégagement de radon (rez-de-chaussée, maisons, caves). Il entraîne alors une exposition interne conséquente à cause de ses descendants à période radioactive courte (dont fait notamment partie le polonium).
D'autre part, la Terre est en permanence soumise à un flux de particules primaires de haute énergie en provenance essentiellement de l'espace et (en bien moindre mesure) du Soleil : les rayons cosmiques. Le vent solaire, et le champ magnétique qu'il entraîne, dévient une partie des rayons cosmiques « interstellaires » ; le champ magnétique terrestre (la ceinture de Van Allen) dévie la majeure partie de ceux approchant la Terre. L’atmosphère n'absorbant qu’une partie de ces particules de haute énergie, une fraction de celle-ci atteint le sol, voire pour les plus énergétiques, traverse les premières couches rocheuses.
La part due au rayonnement cosmique représente environ 32 nGy/h[11] au niveau de la mer. Cette valeur varie en fonction de la latitude et de l'altitude, elle double à 1 500 m d'altitude.
Ce rayonnement extraterrestre, par un phénomène de spallation à partir des noyaux plus lourds présents dans la haute atmosphère, entraîne la production de rayonnements et de particules ionisantes secondaires ou tertiaires (neutrons, électrons, alpha, ions, etc.). Ce phénomène est à l'origine, entre autres, de la production de radionucléides cosmiques sur notre planète tels le carbone 14 et le tritium. Ces isotopes ont une demi-vie beaucoup trop courte pour avoir été présents depuis la formation de la Terre, mais sont en permanence reconstitués.
Radioactivité artificielle
L'activité humaine est une autre source majeure de rayonnements ionisants. Principalement, pour 20 % du total des expositions humaines à la radioactivité, par les activités médicales : production de radionucléides par cyclotron (pour les scintigraphies et TEP par exemple). Le reste, représentant 3 % du total des expositions humaines, est produit, par ordre d'importance, par :
- diverses industries minières, centrales au charbon ;
- l'armée : retombées d'essais nucléaires, bombes nucléaires ;
- l'énergie nucléaire civile (0,3 % du total des expositions) : émissions, fuites et production de déchets radioactifs ;
- accidents : catastrophe nucléaire de Tchernobyl, accident nucléaire de Fukushima ;
- la recherche : recherche en physique des particules (par exemple au CERN en Suisse ou au GANIL en France).
C'est l'imagerie médicale au moyen de rayons X qui produit la plus grande part de l'exposition artificielle aux rayonnements ionisants. On ne parle cependant pas de radioactivité car les rayons X ne sont pas issus de réactions nucléaires mais d'excitation électronique de l'atome.
Radioprotection
Substance radioactive
Une substance radioactive doit être repérée par le symbole ☢ (Unicode 2622, UTF-8 E2 98 A2).
- Une « substance radioactive » au sens réglementaire est une substance qui contient des radionucléides, naturels ou artificiels, dont l'activité ou la concentration justifie un contrôle de radioprotection[12].
En ce qui concerne les expositions planifiées à une source radiologique artificielle, un contrôle de radioprotection doit être établi dès lors que le débit de dose maximal susceptible d'être reçu par une personne présente est supérieur à 2.5 μSv/h[13]. A contrario, si le débit de dose maximal subi est indiscutablement inférieur à cette valeur, la substance ou le produit ne relèvent pas de la législation sur la radioprotection, et ne justifient pas l'application des mesures de radioprotection correspondantes.
Gestion des risques sanitaires

Les conséquences de la radioactivité sur la santé sont complexes. Le risque pour la santé dépend non seulement de l'intensité du rayonnement et la durée d'exposition, mais également du type de tissu concerné — les organes reproducteurs sont 20 fois plus sensibles que la peau (loi de Bergonié et Tribondeau ou loi de la radiosensitivité). Les effets sont différents selon le vecteur de la radioactivité :
- exposition à des rayonnements ionisants par une source radioactive à distance ;
- contamination radioactive si par exemple l'on ingère ou inhale un produit radioactif.
Les normes internationales, basées sur les conséquences épidémiologiques de l'explosion des bombes d'Hiroshima et Nagasaki, partent du principe que le risque pour la santé est proportionnel à la dose reçue et que toute dose de rayonnement comporte un risque cancérigène et génétique (CIPR 1990).
La réglementation pour la protection contre les radiations ionisantes est basée sur trois recommandations fondamentales :
- justification : on ne doit adopter aucune pratique conduisant à une irradiation, à moins qu'elle ne produise un bénéfice suffisant pour les individus exposés ou pour la société, compensant le préjudice lié à cette irradiation ;
- optimisation : l'irradiation doit être au niveau le plus bas que l'on peut raisonnablement atteindre ;
- limitation de la dose et du risque individuels : aucun individu ne doit recevoir des doses d'irradiation supérieures aux limites maximum autorisées.
De récentes études de l'IRSN s'intéressent aux effets de la contamination radioactive chronique, qui même à des faibles doses, pourraient ne pas être négligeables, et pourraient provoquer différentes pathologies atteignant certaines fonctions physiologiques (système nerveux central, respiration, digestion, reproduction)[14]. Mais cette vision est contestée, et d'autres acteurs, dont notamment l'Académie de médecine, estiment au contraire que ces craintes sont inutiles[15].
Dose radiative
Le principe retenu en radioprotection est de maintenir l'exposition au niveau le plus bas qu'il est raisonnablement possible d'atteindre (principe ALARA). Pour faciliter cette optimisation, les sites français exposés aux radiations ionisantes sont organisés en zones dont l'accès est plus ou moins restreint. Ces zones sont délimitées par les débits de doses suivants[16] :
- zone bleue : d'environ 2,5 à 7,5 μSv h−1 ;
- zone verte : de 7,5 à 25 μSv h−1 ;
- zone jaune : de 25 μSv h−1 à 2 mSv h−1 ;
- zone orange : de 2 à 100 mSv h−1 ;
- zone rouge : > 100 mSv h−1.
L'environnement naturel émet un rayonnement variant de 0,2 μSv h−1 à 1 μSv h−1, avec une moyenne de 0,27 μSv h−1 (soit 2,4 mSv an−1 habitant−1). Le débit de dose dont on est certain qu'il produit des effets biologiques dangereux se situe à partir de 1 mSv h−1, c'est-à-dire en « zone jaune ». Les effets varient selon le temps auquel on y est soumis. Les effets statistiquement observables apparaissent pour des doses cumulées supérieures à 100 mSv, soit un stationnement de plus de 50 h (une semaine à plein temps) en zone jaune. Cette exposition peut être atteinte en 1 h en « zone orange ».
Dose équivalente

La dose équivalente est la mesure de dose cumulée d'exposition continue aux radiations ionisantes durant une année, avec des facteurs de pondération. Jusqu'en 1992, les doses équivalentes n'étaient pas mesurées de la même façon en Europe et aux États-Unis ; aujourd'hui ces doses sont standardisées.
La dose cumulée d'une source radioactive artificielle devient dangereuse à partir de 500 mSv (ou 50 rem), dose à laquelle on constate les premiers symptômes d'altération sanguine. En 1992, la dose efficace (E) maximale pour une personne travaillant sous rayonnements ionisants était fixée à 15 mSv sur les 12 derniers mois en Europe (CERN et Angleterre) et à 50 mSv sur les 12 derniers mois aux États-Unis. Depuis août 2003, la dose efficace maximale est passée à 20 mSv sur les 12 derniers mois.
Lors d'un scanner médical, le patient peut par exemple recevoir une dose moyenne de 0,05 mSv (examen local), de 25 mSv (scanner du crâne) ou de 150 mSv (scanner du corps entier). Pour éviter tout symptôme d'altération sanguine, on se limite à un maximum de trois examens d'organe par an.
Radioprotection
Irradiation
En France, la dose annuelle d'origine artificielle autre que les applications médicales maximale est fixée à 20 mSv (2 rem) pour les travailleurs et à 1 mSv (0,1 rem) pour la population.
Les facteurs qui protègent des radiations sont :
- Distance (la variation du débit de dose (DDD) est inversement proportionnelle au carré de la distance à la source) ;
- Activité (en centrale nucléaire, on effectue diverses opérations pour enlever les sources des conduits) ;
- Temps (la dose est proportionnelle au temps ; rester le moins longtemps près de la source) ;
- Écran (plomber, recouvrir d'acier, bétonner, immerger la source, par exemple).
Certains comportements sont susceptibles d'entraîner une surexposition à la radioactivité : un patient qui passe 5 radiographies aux rayons X peut subir une dose de 1 mSv ; les passagers et le personnel navigant des avions de ligne, ainsi que les astronautes en orbite, peuvent subir une dose voisine lors d'une éruption solaire très intense. S'ils répètent ces voyages ou effectuent des missions de longues durées, une exposition prolongée accroît le risque d'irradiation.
Alimentation
Le phénomène de radioactivité étant au départ mystérieux parce que mal compris, certaines eaux minérales ou de source en firent quelque temps un argument de vente sur leurs étiquettes : Bussang (Vosges) déclarée d'intérêt public en 1866, Villeminfroy (Haute-Saône) autorisée en 1859, Teissières (Cantal) autorisée en 1847 et « approuvée par l'Académie de médecine », et beaucoup d'autres dont les images d'étiquettes sont visibles sur la Toile[17]. Leurs radioactivités — faibles, mais réelles — étaient de l'ordre de celles que l'on trouve naturellement dans quelques régions granitiques, sans réel danger, mais sans effet thérapeutique non plus.
La Communauté européenne a fixé des doses de radioactivité à ne pas dépasser dans les aliments : le lait ne doit pas dépasser 500 Bq/l pour l'iode 131. Dans certains länder allemands, les normes sont beaucoup plus sévères (100 Bq/l en Sarre, 20 Bq/l en Hesse et Hambourg).
Radioécologie
Mi-2011 après l'accident nucléaire de Fukushima et à l’occasion d'une Conférence internationale[18] de radioécologie et de radioactivité environnementale le 20 juin 2011 à Hamilton (Canada)[19], huit organismes de recherche européens, avec le soutien de la Commission européenne, ont créé une Alliance européenne en radioécologie[20] pour mieux intégrer la recherche en radioécologie[21]. Ces organismes sont le BfS (Allemagne), le NERC (Royaume-Uni), le CIEMAT (Espagne), l'IRSN (France), le NRPA (Norvège), le SCK/CEN (Belgique), le SSM (Suède), et le STUK (Finlande)[19]. La commission soutient aussi le projet STAR porté par l'Alliance européenne en radioécologie, l'université des sciences de la vie de Norvège et l'université de Stockholm sur les thèmes de « la formation, la gestion et la dissémination de la connaissance ainsi que de la recherche en radioécologie », en focalisant d'abord leurs efforts sur les sujets suivants :
- « l’intégration des méthodes d’évaluation du risque radiologique pour l’homme et les écosystèmes » ;
- « la recherche sur l’effet des faibles doses sur les écosystèmes » ;
- « l’étude des conséquences des pollutions mixtes, qui associent les substances radioactives et chimiques ».
Contamination radioactive
En zone contaminée par des poussières radioactives, on se protège par une hygiène très stricte : confinements ; tenue étanche ventilée (TEV), heaume ventilé avec surtenue, et/ou autres protections ; nettoyage des surfaces de travail ; précautions pour éviter de soulever la poussière.
Les mesures sont réalisées au moyen de contaminamètres équipés de sonde α ou β [unités de mesure : Bq/m3 (pour la contamination volumique) ou Bq/cm2 (pour la contamination surfacique).
Notes et références
Notes
- La formule donne un résultat par excès pour N/Z, elle est perfectible.
Références
- Bernard Fernandez, De l'atome au noyau : Une approche historique de la physique atomique et de la physique nucléaire, Ellipses, , 597 p. (ISBN 978-2729827847), partie I, chap. 4 (« L'émanation du thorium »).
- J.P. Sarmant, Dictionnaire Hachette de Physique, Hachette, Paris, 1988 (ISBN 2-01-007597-8).
- Eugène Hecht, Physique, De Boeck, 1999, p. 1 099.
- (en) Thomas Ruedas, « Radioactive heat production of six geologically important nuclides », G3, (DOI 10.1002/2017GC006997).
- U. Fielitz, Radioaktivität in Wildtieren, Abshlussbericht zum Forschungsvorhaben 4017 des BMU, Universität Goettingen. Goettingen : Goettingen University, 1994, 120 p.
- Réseau national de mesures de la radioactivité de l'environnement.
- Site Internet du Réseau national de mesure de la radioactivité dans l’environnement (RNM).
- Bilan IRSN 2009 de la surveillance radiologique de l’environnement en France : vers une évolution de la stratégie de surveillance, 2011/02/03.
- Jean-Marc Jancovici : à propos de quelques objections fréquentes sur le nucléaire civil.
- S. Billon et al., « French population exposure to radon, terrestrial gamma and cosmics ray », Radiation Protection Dosimetry, 2005, Vol. 113 no 3.
- (en) [PDF] UNSCEAR 2000.
- Code de l'environnement, Article L542-1-1.
- Arrêté du 15 mai 2006 relatif aux conditions de délimitation et de signalisation des zones surveillées et contrôlées et des zones spécialement réglementées ou interdites compte tenu de l'exposition aux rayonnements ionisants, ainsi qu'aux règles d'hygiène, de sécurité et d'entretien qui y sont imposées [1].
- Lefigaro.fr.
- Faibles doses de radioactivité : une révolution dans la radioprotection par Emmanuel Grenier (Source : Fusion no 77, 1999).
- Circulaire DGT/ASN no 01 du 18 janvier 2008.
- Eaux minérales et autres produits vendus comme radioactifs.
- Site internet de la Conférence internationale de radioécologie et de radioactivité.
- Conférence internationale de radioécologie et de radioactivité environnementale le 20 juin 2011 à Hamilton (Canada).
- Site internet de l'Alliance européenne en radioécologie.
- IRSN, L’Alliance européenne en radioécologie : une initiative pour une meilleure intégration des recherches menées en radioécologie en Europe, 2011/06/20.
Voir aussi
Articles connexes
- Liste des unités de mesure de radioactivité
- Radioisotope
- Table des isotopes
- Tableau périodique des éléments
- Période radioactive | Décroissance radioactive
- Période biologique
- Rayonnement ionisant
- Radioprotection
- Radioactivité alpha | Radioactivité bêta | Radioactivité gamma
- Radiotoxicologie
- Faibles doses d'irradiation
- Elaphomyces granulatus (champignon bioaccumulateur et bioconcentrateur, à l'origine de la contamination de sangliers)
- Cassure chromosomique
- Organisme radiorésistant
- Agence nationale pour la gestion des déchets radioactifs
- Physique de la radioactivité
Principaux isotopes radioactifs
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1 | H | He | |||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| 6 | Cs | Ba | * |
Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | * * |
Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | |||||||||||||||||||
* |
La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | |||||
* * |
Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | |||||
| Pb | Un isotope au moins de cet élément est stable | ||||||||||||||||||
| Cm | Un isotope a une période d'au moins 4 millions d'années | ||||||||||||||||||
| Cf | Un isotope a une période d'au moins 800 ans | ||||||||||||||||||
| Md | Un isotope a une période d'au moins 1 journée | ||||||||||||||||||
| Bh | Un isotope a une période d'au moins 1 minute | ||||||||||||||||||
| Og | Tous les isotopes connus ont une période inférieure à 1 minute | ||||||||||||||||||
- américium : 241Am
- antimoine : 125Sb
- carbone : 14C
- césium : 134Cs, 135Cs et 137Cs
- chlore : 36Cl
- cobalt : 60Co
- curium : 242Cm et 244Cm
- iode : 129I, 131I et 133I
- krypton : 85Kr et 89Kr
- phosphore : 32P
- plutonium : 239Pu et 241Pu
- polonium : 210Po
- potassium : 40K
- radium : 226Ra et 242Ra
- ruthénium : 106Ru
- sélénium : 75Se
- soufre : 35S
- strontium : 90Sr
- thorium : 234Th
- tritium : 3H
- uranium : 235U et 238U
Organisations
- Commission internationale de protection radiologique (CIPR)
- Institut de radioprotection et de sûreté nucléaire (IRSN)
- Société française de radioprotection (SFRP)
- Commission de recherche et d'information indépendantes sur la radioactivité (CRIIRAD)
- Agence nationale pour la gestion des déchets radioactifs (ANDRA)
Liens externes
- Mesures de la radioactivité dans l’environnement publiées par l'ASN et l'IRSN.
- Déchets-radioactifs.com. Site d'information pédagogique sur la radioactivité, les déchets radioactifs et leur gestion (site édité par l'Andra).
- LaRadioactivite.com (un site expliquant ce qu'est la radioactivité, réalisé par des chercheurs du CNRS).
- Articles de février et mars 1896 d'Henri Becquerel, et analyse de ces articles sur le site BibNum.
- « La transformation radioactive », article de 1903 de Rutherford & Soddy en ligne et analysé sur BibNum.
- La découverte de la radioactivité artificielle, texte de 1935 de Frédéric Joliot-Curie, et analyse sur le site BibNum
- (en) Liste d'accidents (Johnston's Archive).
- La radioactivité de Homer à Oppenheimer http://www.andra.fr/laradioactivite/ – le site de l'exposition itinérante proposée par l'Andra.











































