Mésitylène
| Mésitylène | |||

| |||
| Identification | |||
|---|---|---|---|
| Synonymes |
1,3,5-triméthylbenzène |
||
| No CAS | |||
| No ECHA | 100.003.278 | ||
| No CE | 203-604-4 | ||
| Apparence | liquide incolore, d'odeur caractéristique[1]. | ||
| Propriétés chimiques | |||
| Formule | C9H12 [Isomères] |
||
| Masse molaire[3] | 120,191 6 ± 0,008 g/mol C 89,94 %, H 10,06 %, |
||
| Diamètre moléculaire | 0,637 nm[2] | ||
| Propriétés physiques | |||
| T° fusion | −45 °C[1] | ||
| T° ébullition | 164,72 °C[4] | ||
| Solubilité | 0,02 g·l-1 dans l'eau (25 °C) | ||
| Paramètre de solubilité δ | 18,0 MPa1/2 (25 °C)[5] | ||
| Masse volumique | 0,865 2 g·cm-3[6]
|
||
| T° d'auto-inflammation | 550 °C[1] | ||
| Point d’éclair | 50 °C (coupelle fermée)[1] | ||
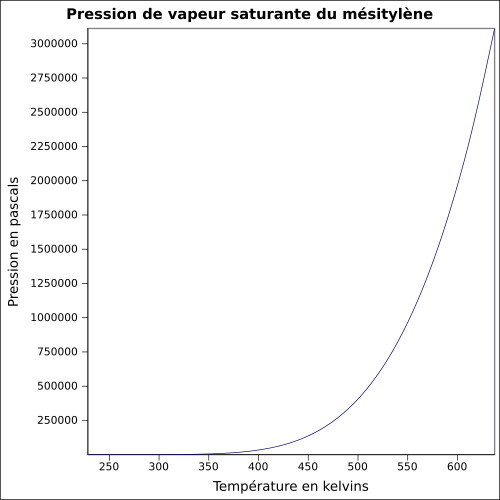
| Pression de vapeur saturante | à 20 °C : 0,25 kPa[1]
|
||
| Point critique | 364,14 °C[4] | ||
| Thermochimie | |||
| Cp | |||
| Propriétés optiques | |||
| Indice de réfraction | 1,4968[2] | ||
| Précautions | |||
| SGH[9] | |||
| H226, H335 et H411 |
|||
| SIMDUT[10] | |||
 B3, |
|||
| NFPA 704 | |||
| Transport | |||
|
|||
| Inhalation | maux de tête, mal de gorge, vertiges, vomissements | ||
| Peau | irritant | ||
| Yeux | irritant | ||
| Autre infos | polluant marin | ||
| Écotoxicologie | |||
| LogP | 3,42[1] | ||
| Seuil de l’odorat | bas : 0,006 ppm haut : 2,4 ppm[11] |
||
| Composés apparentés | |||
| Isomère(s) | Hémimellitène Pseudocumène |
||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Le mésitylène est un composé organique aromatique de formule chimique C9H12. Il est constitué d'un noyau benzénique substitué par trois groupements méthyles en positions 1, 3 et 5 : c'est en fait l'isomère 1,3,5 du triméthylbenzène. Il est fabriqué par distillation de l'acétone en présence d'acide sulfurique, ce dernier agissant comme catalyseur et agent de déshydratation. C'est un composé couramment utilisé comme solvant dans la recherche et l'industrie.
Propriétés[modifier | modifier le code]
Le mésitylène est un liquide incolore, facilement inflammable. Il est très peu soluble dans l'eau. En revanche, sa solubilité dans le benzène, l'éther et les alcools est assez élevée. Il est naturellement présent en faibles quantités dans le pétrole et le goudron de houille.
Sécurité[modifier | modifier le code]
Au-dessus de 40 °C, le mésitylène forme un mélange explosif avec l'air. Il réagit violemment avec les oxydants forts avec un risque d'explosion. Par inhalation, il cause des maux de tête et une irritation de la gorge. En concentrations élevées, ses vapeurs ont une action anesthésiante. Le mésitylène est irritant pour la peau, les yeux et l'appareil respiratoire.
Voir aussi[modifier | modifier le code]
Lien externe[modifier | modifier le code]
Références[modifier | modifier le code]
- 1, 3, 5 - TRIMETHYL BENZENE, Fiches internationales de sécurité chimique
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Iwona Owczarek et Krystyna Blazej, « Recommended Critical Temperatures. Part II. Aromatic and Cyclic Hydrocarbons », J. Phys. Chem. Ref. Data, vol. 33, no 2, , p. 541 (DOI 10.1063/1.1647147)
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 978-0-387-69002-5 et 0-387-69002-6, lire en ligne), p. 294
- (en) J. G. Speight, Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, , 16e éd., 1623 p. (ISBN 0-07-143220-5), p. 2.289
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 3, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-859-4)
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Triméthyl-1,3,5 benzène » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- « Trimethyl benzene isomers », sur hazmap.nlm.nih.gov (consulté le )