Tréhalose
| Tréhalose | ||

| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | 2-(hydroxyméthyl)-6-[3,4,5- trihydroxy-6-(hydroxyméthyl) tétrahydropyran-2-yl]oxy- tétrahydropyran-3,4,5-triol |
|
| Synonymes |
α-D-glucopyranosyl; |
|
| No CAS | (anhydre) | |
| No ECHA | 100.002.490 | |
| PubChem | 162349 | |
| Apparence | poudre blanche cristalline[réf. nécessaire] | |
| Propriétés chimiques | ||
| Formule | C12H22O11 [Isomères] |
|
| Masse molaire[1] | 342,296 5 ± 0,014 4 g/mol C 42,11 %, H 6,48 %, O 51,42 %, |
|
| Propriétés physiques | ||
| T° fusion | 203 °C[2] | |
| T° ébullition | Se décompose[2] | |
| Solubilité | 68,9g/100g eau à 20 °C[2] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
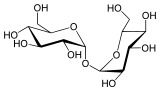
Le tréhalose (α-D-glucopyranosyl-α-D-glucopyranoside ou alpha,alpha-tréhalose, ou α-D-glucopyranosyl-α-D-glucopyranoside, dihydrate) est un sucre, et plus précisément un diholoside (ou disaccharide) non-réducteur.
À la différence du saccharose composé d'une molécule de glucose liée à une molécule de fructose, le tréhalose est composé de deux molécules de glucose liées par une liaison α,α-1,1 (ou «1,1-α-glycosidique ») particulièrement stable.
Description et usages[modifier | modifier le code]
C'est un sucre, quasiment inodore, composé de cristaux blancs ou presque blancs, au goût sucré mais au pouvoir sucrant environ moitié de celui du sucre ordinaire, le saccharose.
Il présente des propriétés physico-chimiques différentes des autres sucres, qui le font utiliser par l’industrie agroalimentaire, mais aussi pharmaceutique et cosmétique ainsi que dans les boissons ou aliments « énergétiques » pour les sportifs, comme additif agent protecteur de levures boulangères, ou comme agent antirouille. Il pourrait dans un proche avenir être utilisé comme agent conservateur de vaccins et cryoprotecteur pour des organes en attente de transplantation[3] (avec un usage limité par le fait qu'en l’absence d'un transporteur spécifique, il ne peut théoriquement pénétrer ni franchir les membranes cellulaires ; mais, en laboratoire on a pu protéger des cellules de pancréas ou de fœtus humain lors d'une congélation. Dans ce dernier cas lors de la phase de congélation, juste avant le changement de phase, les membranes deviennent moins imperméables, permettant au tréhalose de pénétrer dans la cellule et de la protéger[4]). Ce sucre pourrait aussi contribuer à de nouvelles pistes thérapeutiques[5],[6].
Source[modifier | modifier le code]
On le trouve naturellement dans certaines plantes, champignons (dont levures) et aussi dans l'hémolymphe de beaucoup d'insectes ou dans les fluides corporels de nématodes, ce qui explique qu'il puisse être trouvé en faible quantité dans divers aliments commercialisés tels que le pain, la bière et le vin, le miel, divers champignons, etc.[7].
Avant 1995 ses coûts élevés de synthèse industrielle ne permettaient pas son utilisation dans l'industrie alimentaire, puis des innovations technologiques ont réduit ses coûts d'un facteur 100 environ, et il est alors devenu un additif alimentaire très utilisé.
Synthèse[modifier | modifier le code]
Le transfert du glucose à partir de l'uridine diphosphate glucose vers le glucose-6-phosphate forme le tréhalose-9-phosphate, qui sous l'action d'une phosphatase, libère le phosphate pour donner le tréhalose[8].
Rôle dans la nature[modifier | modifier le code]
On pense que cette molécule serait impliquée dans la capacité qu'auraient certaines plantes ainsi que certains animaux à résister à des périodes prolongées de dessiccation[9] (état de cryptobiose) comme chez certaines bryophytes et chez les tardigrades.
On pense que ce sucre forme une phase de gel pendant que les cellules se déshydratent, ce qui empêche la rupture des organites de la cellule. La réhydratation permet alors une reprise de l'activité cellulaire normale, en effet les dommages qui suivent normalement un cycle de déshydratation/réhydratation, sont généralement mortels pour la cellule.
Il serait protecteur contre le stress oxydatif[10].
Digestion[modifier | modifier le code]
Le tréhalose est hydrolysé par la tréhalase dans l'intestin grêle en deux molécules de glucose qui seront normalement absorbées et métabolisées.
Application alimentaire[modifier | modifier le code]
Son pouvoir sucrant (sucrosité relative) est de 40 à 45 % de celui du saccharose[2],[11]. Il présente un avantage technologique et industriel : il est très peu hygroscopique et plus stable chimiquement et thermiquement, ce qui devrait lui permettre d'allonger la durée de conservation d’aliments pulvérulents tels que laits en poudre, soupe sèche, ou certaines confiseries ou pâtisseries (glaçages…).
Selon les résultats toxicologiques disponibles pour l'homme, la tolérance au tréhalose semble bonne, et ne pose pas de problème au niveau de la consommation attendue dans l'alimentation. Certaines études ont été évaluées par la FAO (Organisation des Nations unies pour l'alimentation et l'agriculture) et par un Comité mixte d'experts des additifs alimentaires de l'OMS (Organisation mondiale de la santé) ; (JECFA, 2001), qui n'ont pas jugé nécessaire de proposer une valeur d'apport quotidien admissible (AQA) pour le tréhalose[12].
Au vu de ces données, la Direction des aliments de Santé Canada a en conclu à l'innocuité nutritionnelle du tréhalose, mais demande à Hayashibara International Inc. et Cargill, Inc. de rédiger et mettre en œuvre, de manière volontaire, un plan d'éducation et de communication visant à informer les diabétiques, les éducateurs en diabète ou autres professionnels de santé du fait que ce produit est un vrai sucre. Ce plan devra être discuté avec Santé Canada et le Ministère devra être informé des progrès dans sa mise en œuvre par ces deux entreprises.
Il est autorisé sur le marché européen depuis 2001[13]. La commission européenne en a demandé une évaluation en tant qu'« aliments et ingrédients auxquels a été appliqué un procédé de production qui n’est pas couramment utilisé[14] ». Comme tous les glucides, il fait l’objet en Europe de conditions particulières d’emploi[15] ; la dénomination « tréhalose » doit obligatoirement figurer sur l’étiquette ou dans la liste des ingrédients, et une mention obligatoire doit préciser sur l’étiquetage la présence du tréhalose vendu tel quel, ou des aliments en contenant, que « le tréhalose est une source de glucose ». « Cette mention doit être indiquée dans une note de bas de page bien visible, à laquelle renvoie un astérisque (*) placé à côté de la dénomination «tréhalose». Cette mention apparaît dans une police de caractères ayant au moins la même taille que celle utilisée pour la liste des ingrédients même ».
Production[modifier | modifier le code]
Le tréhalose a d'abord été extrait d'une levure (production approuvée en 1991 au Royaume-Uni — hors aliments pour bébé), mais la production est restée faible. Puis, un procédé de fabrication à partir d’amidon liquéfié, par un procédé enzymatique en plusieurs étapes, a été breveté par la société japonaise Hayashibara de Okayama, au Japon.
Santé[modifier | modifier le code]
Certains individus ne produisent pas l'enzyme tréhalase normalement présente dans les intestins et les reins chez l'homme, ou son activité peut être inhibée. Dans ces cas, une malabsorption peut produire des symptômes comparables à ceux produits par l'absorption de lactose chez les intolérants au lactose, ou aux alcools de sucre chez la plupart des individus. Le détenteur du brevet estime qu'il y a moins de personnes déficientes en tréhalase que de personnes déficientes en lactase.
L'ajout apparemment anodin de tréhalose comme additif alimentaire à divers aliments a favorisé la virulence épidémique de souches épidémiques spécifiques de Clostridium difficile apparues en Amérique du nord (États-Unis puis Canada) et dans plusieurs pays européens depuis 2001[16] (453000 cas d'infections aux États-Unis, dont 29000 décès dans les 30 jours après le diagnostic)[17],[18]. La mortalité constatée dans plusieurs centres hospitaliers américains semble être comprise entre 4.2 à 6.9%[19] et la surveillance instaurée au Québec indique même des pourcentages de 12 % en 2018-2019[20], voir beaucoup plus pour les patients âgés dans une étude au CHU de Nice[21]. Presque toutes ces souches hautement pathogènes (RT027 et RT078 notamment) viennent d'une même lignée de C. difficile [ribotype 027 (RT0272)] qui a gagné une grande partie du monde[22] et certaines sont capables d'utiliser de faibles doses de tréhalose comme source unique de carbone pour leur métabolisme[23]. Les chercheurs en font donc un facteur clé dans le franchissement d'un seuil épidémique pour ces bactéries, connues depuis les années 80[24].
Il a été montré en 2018 que le Tréhalose sanguin pouvait limiter le développement du diabète de type 2 chez la souris via l'activation d'un gène augmentent la sensibilité de l'insuline (comme le ferait les thiazolidinediones)[25]. Cependant, dans les faits, il serait potentiellement dégradé en glucose avant de parvenir au foie.
Métrologie[modifier | modifier le code]
Il est nécessaire de pouvoir doser ce « nouveau » sucre dans l'alimentation en raison de l'existence de personnes intolérantes à ce produit.
Les trois premières méthodes de dosage (dans l'organisme ou dans un aliment ou une boisson) étaient lourdes et coûteuses, parfois peu sélectives, et impropres aux analyses à haut-débit d’échantillons de petits volumes.
Une méthode brevetée en 2006[26] utilise un OGM (une bactérie Pseudomonas fluorescens génétiquement modifiée) comme biosenseur. Un gène de cette bactérie est activé par le contact avec ce sucre, et active un autre gène qui synthétise une enzyme capable de transformer un substrat en un produit détectable par colorimétrie ou chimiluminescence. Un spectrophotomètre ou un luminomètre, ou l'œil mesure alors une intensité de couleur ou lumière qui correspond à la dose dans l’échantillon. Cette méthode permet de détecter des doses faibles de tréhalose (jusqu’à 10−4 M) et ne nécessite que de très petit volume (10 µl suffisent).
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) T Higashiyama, « Novel functions and applications of trehalose. », Pure Appl. Chem., vol. 74, no 7, , p. 1263-1269 (lire en ligne) [PDF]
- Pascale Borensztein Inserm U. 474 médecine/sciences 2000 ; 16 : 1265 Le tréhalose : un cryoprotecteur très efficace ? (médecine/sciences 2000 ; 16 : 1265)
- Beattie GM, Crowe JH, Lopez AD, Cirulli V, Ricordi C, Hayek A. Trehalose: a cryoprotectant that enhances recovery and preserves function of human pancreatic islets after long-term storage. Diabetes 1997 ; 46 : 519-23.
- page INRA sur la quantification rapide du tréhalose
- Eroglu A, Russo MJ, Bieganski R, et al. Intracellular trehalose improves the survival of cryopreserved mammalian cells. Nat Biotechnol 2000 ; 18 :163-7.
- Document canadien (Informations sur les aliments nouveaux) de Santé Canada
- Chen Q, Haddad GG, Role of trehalose phosphate synthase and trehalose during hypoxia: from flies to mammals, J Exp Biol, 2004;207:3125–3129
- Tapia H, Young L, Fox D, Bertozzi CR, Koshland D, Increasing intracellular trehalose is sufficient to confer desiccation tolerance to Saccharomyces cerevisiae, Proc Natl Acad Sci U S A, 2015;112:6122–6127
- Benaroudj N, Lee DH, Goldberg AL, Trehalose accumulation during cellular stress protects cells and cellular proteins from damage by oxygen radicals, J Biol Chem, 2001;276:24261–24267
- (en) Tsuneyuki Oku & Sadako Nakamura, « Digestion, absorption, fermentation, and metabolism of functional sugar substitutes and their available energy. », Pure Appl. Chem., vol. 74, no 7, , p. 1253–1261 (lire en ligne) [PDF]
- Food and Nutrition Paper 5 Rev.2 — Guide to specifications for general notices, general analytical techniques, identification tests, test solutions andother reference materials (CMEAA)1991, 322 pp., (en).
- Décision de la Commission du 25 septembre 2001 relative à l'autorisation de mise sur le marché du tréhalose en tant que nouvel aliment ou nouvel ingrédient alimentaire, en application du règlement (CE) no 258/97 du Parlement européen et du Conseil [notifiée sous le numéro C(2001) 2687
- Article 1.2.f du règlement (CE) n°258/97
- Note du Syndicat national des producteurs d'additifs et d'ingrédients de la chaîne alimentaire relative à l'autorisation européenne d'utilisation]
- (en) J. Collins, C. Robinson, H. Danhof et C. W. Knetsch, « Dietary trehalose enhances virulence of epidemic Clostridium difficile », Nature, (DOI 10.1038/nature25178).
- M Butler, A Olson, D Drekonja, A Shaukat, N Schwehr, N Shippee et TJ Wilt, « Early Diagnosis, Prevention, and Treatment of Clostridium difficile: Update », AHRQ Comparative Effectiveness Reviews., , vi,1 (PMID 27148613)
- Fernanda C. Lessa, Yi Mu, Wendy M. Bamberg, Zintars G. Beldavs, Ghinwa K. Dumyati, John R. Dunn, Monica M. Farley, Stacy M. Holzbauer, James I. Meek, Erin C. Phipps, Lucy E. Wilson, Lisa G. Winston, Jessica A. Cohen, Brandi M. Limbago, Scott K. Fridkin, Dale N. Gerding et L. Clifford McDonald, « Burden of Infection in the United States », New England Journal of Medicine, vol. 372, no 9, , p. 825–834 (PMID 25714160, DOI 10.1056/NEJMoa1408913)
- « Clostridioides (Clostridium) Difficile Colitis: Practice Essentials, Background, Pathophysiology », sur Medscape, (consulté le )
- « Diarrhées associées au Clostridium difficile : résultats de surveillance 2018-2019 », sur INSPQ (consulté le )
- Claire Chennesseau, Déterminer les facteurs de risque de mortalité à 3 mois des patients âgés de plus de 75 ans atteints d’une infection à Clostridium Difficile, hospitalisés au Centre Hospitalier Universitaire de Nice, , 59 p. (lire en ligne)
- He, M. et al. Emergence and global spread of epidemic healthcare-associated Clostridium difficile |Nature Genet. 45, 109–113 (2013). |résumé
- Ballard Jd (2018) Pathogens boosted by food additive ; Epidemic strains of the bacterium Clostridium difficile have now been found to grow on unusually low levels of the food additive trehalose, providing a possible explanation for C. difficile outbreaks since 2001 (Le tréhalose alimentaire accroît la virulence de l'épidémie de Clostridium difficile)| News and views | Nature| 03 Janvier 2018
- (en) « Dietary sugar linked to increasing bacterial epidemics », sur EurekAlert! (consulté le )
- (en-US) « Natural sugar defends against metabolic syndrome, in mice | The Source | Washington University in St. Louis », The Source, (lire en ligne, consulté le )
- Méthode élaborée par l'INRA (de Rennes et Nancy) avec l’université flamande de Bruxelles, déposé en Europe par Pascale Frey-Klett et A. Sarniguet sous le titre Genetically engineered Pseudomonas fluorescens strains as biosensor for trehalose detection and quantification in a sample (brevet n°06290811.6 déposé le 18 mai 2006)
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- (en) Avis de la Food Standard Agency du
- (fr) Avis de l’Agence française de sécurité sanitaire des aliments du
- (fr) Avis de l’Agence française de sécurité sanitaire des aliments du
