Chlorure cyanurique
| Chlorure cyanurique | |

| |
| Identification | |
|---|---|
| Nom UICPA | 2,4,6-trichloro-1,3,5-triazine |
| Synonymes |
Trichlorotriazine |
| No CAS | |
| No ECHA | 100.003.287 |
| No CE | 203-614-9 |
| PubChem | 7954 |
| Apparence | poudre cristalline blanche |
| Propriétés chimiques | |
| Formule | C3Cl3N3 [Isomères] |
| Masse molaire[1] | 184,411 ± 0,009 g/mol C 19,54 %, Cl 57,67 %, N 22,79 %, |
| Propriétés physiques | |
| T° fusion | 146 °C[2] |
| T° ébullition | 194 °C[2] |
| Solubilité | décomposition violente dans l'eau[2] |
| Masse volumique | 1,92 g·cm-3 à 20 °C[2] |
| T° d'auto-inflammation | > 650 °C[2] |
| Point d’éclair | > 190 °C[2] |
| Pression de vapeur saturante | 0,025 mbar à 20 °C 2,7 mbar à 70 °C[2] |
| Précautions | |
| NFPA 704 | |
| Directive 67/548/EEC | |
| Transport | |
| Écotoxicologie | |
| DL50 | 10 mg·kg-1 (souris, i.p.) 18 mg·kg-1 (souris, i.v.) 350 mg·kg-1 (souris, oral) |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le chlorure cyanurique est un composé chimique de formule (NCCl)3. C'est un dérivé chloré de la 1,3,5-triazine. C'est un trimère du chlorure de cyanogène[3].
Propriétés[modifier | modifier le code]
Le chlorure cyanurique se présente sous la forme d'une poudre cristalline blanche à l'odeur de dichlore ou d'acide chlorhydrique. À l'air sec, même par température élevée il est stable, mais dès la présence d'humidité, il s'hydrolyse en acide cyanurique et acide chlorhydrique. La vitesse de cette hydrolyse dépend fortement de la température et du pH. Dans une solution tamponnée à pH = 7 d'eau glacée, il est stable pendant plusieurs heures, mais dès que la température dépasse 10 °C, l'hydrolyse se produit, d'autant plus rapidement que la température augmente, aidée par le fait qu'elle est autocatalysée par l'acide chlorhydrique.
Synthèse[modifier | modifier le code]
Le chlorure cyanurique est préparé en deux étapes.
- La première étape est la chloration du cyanure d'hydrogène en chlorure de cyanogène
- HCN + Cl2 → ClCN + HCl
- la deuxième étape consiste en la trimérisation du chlorure de cyanogène en chlorure cyanurique
- 3 ClCN → (ClCN)3
En 2005, approximativement 200 000 tonnes de chlorure cyanurique furent produites[4].
Utilisation[modifier | modifier le code]
Pesticides, colorants[modifier | modifier le code]
Environ 70 % du chlorure cyanurique sert à synthétiser des pesticides de la classe des triazines, en particulier l'atrazine. Ces réactions reposent sur la bonne labilité des atomes de chlore, substitués par des amines :
- (ClCN)3 + ( RNH2) 2 → (RNHCN)(ClCN)2 + RNH3+Cl−
Le chlorure cyanurique est aussi utilisé comme précurseur de colorants et d'agents de réticulation. La plus grande classe de colorants concernés est les triazines-stilbènes sulfonatés utilisés comme agents azurants[4].
Synthèse organique[modifier | modifier le code]
Le chlorure cyanurique est utilisé comme réactif pour convertir les alcools et les acides carboxyliques en respectivement chlorure d'alkyle et chlorure d'acyle[5] :
Il est aussi utilisé comme déshydratant et pour « activer » les acides carboxyliques afin de les réduire en alcools. Lorsqu'il est chauffé en présence de diméthylformamide (DMF) on obtient le réactif de Gold, Me2NCH=NCH=NMe2+Cl−, une source polyvalente pour les aminalkylations et un précurseur d'hétérocycles[6],[7].
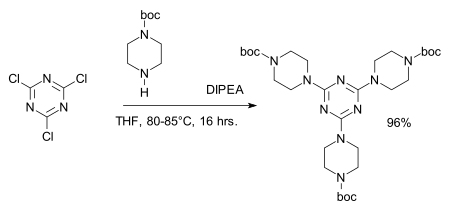
Les atomes de chlore du chlorure cyanurique sont facilement remplaçables par des amines pour former par exemple la mélamine qui peut à son tour être utilisée dans la synthèse de dendrimères[8],[9]:
ou dans la synthèse de ligands récepteurs d'adénosine expérimentaux[10]:
Notes et références[modifier | modifier le code]
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Cyanuric chloride » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée du numéro CAS « 108-77-0 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 01/08/09 (JavaScript nécessaire)
- Cyanuric chloride at Chemicalland21.com
- Klaus Huthmacher, Dieter Most « Cyanuric Acid and Cyanuric Chloride» Ullmann's Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. (ISBN 3527310975)
- (en) K. Venkataraman, and D. R. Wagle, « Cyanuric chloride : a useful reagent for converting carboxylic acids into chlorides, esters, amides and peptides », Tet. Lett., vol. 20, no 32, , p. 3037–3040 (DOI 10.1016/S0040-4039(00)71006-9)
- Probst, D. A. ; Hanson, P. R. ; Barda, D. A. « Cyanuric Chloride » in Encyclopedia of Reagents for Organic Synthesis, 2004, John Wiley & Sons. DOI 10.1002/047084289X.rn00320
- John T. Gupton ; Steven A. Andrews, β-Dimethylaminomethylenation: N,N-Dimethyl-N'-p-tolylformamidine, Org. Synth., coll. « vol. 7 », , p. 197
- (en) Abdellatif Chouai and Eric E. Simanek, « Kilogram-Scale Synthesis of a Second-Generation Dendrimer Based on 1,3,5-Triazine Using Green and Industrially Compatible Methods with a Single Chromatographic Step », J. Org. Chem., vol. 73, , p. 2357-2366 (DOI 10.1021/jo702462t)
- Reagent : DIPEA, amine protective group : BOC
- Modèle:Ref patent (Reagent number two : noréphédrine, base DIPEA)