Éthane
| Éthane | |
| Identification | |
|---|---|
| Nom UICPA | éthane |
| Synonymes |
diméthyle |
| No CAS | |
| No ECHA | 100.000.741 |
| No CE | 200-814-8 |
| PubChem | 6324 |
| SMILES | |
| InChI | |
| Apparence | gaz comprimé liquefié, incolore, inodore à l'etat pur[1]. |
| Propriétés chimiques | |
| Formule | C2H6 [Isomères] |
| Masse molaire[2] | 30,069 ± 0,002 g/mol C 79,89 %, H 20,11 %, |
| Propriétés physiques | |
| T° fusion | −183,3 °C[3] |
| T° ébullition | −88,6 °C[3] |
| Solubilité | 60,2 mg·l-1 (eau,25 °C) 460 ml·l-1 (éthanol,4 °C) |
| Paramètre de solubilité δ | 12,3 MPa1/2 (25 °C)[5] |
| Masse volumique | 1,355 1 kg·m-3 (0 °C, 1 013 mbar, gaz) 0,544 1 kg·l-1 (−88,6 °C, 1 013 mbar, liquide)[3] |
| T° d'auto-inflammation | 515 °C[3] |
| Point d’éclair | −135 °C[3] |
| Limites d’explosivité dans l’air | 2,4–14,3 %vol 31–182 g·m-3[3] |
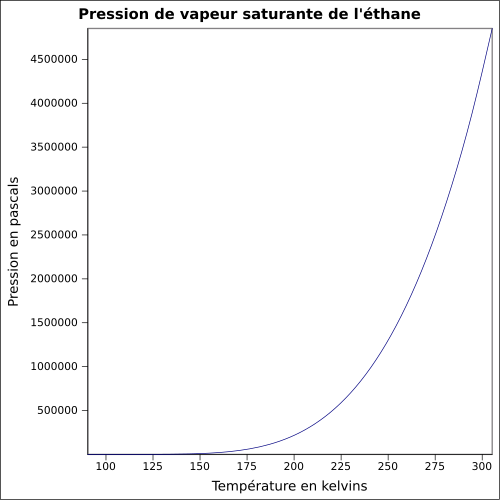
| Pression de vapeur saturante | 37,8 bar à 20 °C 46,9 bar à 30 °C[3] |
| Viscosité dynamique | 63,4 mPo à −78,5 °C[4] |
| Point critique | 32,15 °C 49 bar 0,147 l·mol-1 [7] |
| Point triple | −182,15 °C 0,011 bar [7] |
| Vitesse du son | 1 326 m·s-1 (liquide,−88,6 °C) 312 m·s-1 (gaz,27 °C,1 atm)[8] |
| Thermochimie | |
| S0liquide, 1 bar | 126,7 J·mol-1·K-1[7] |
| ΔfH0gaz | −84,0 kJ·mol-1[7] |
| ΔfusH° | 0,583 kJ·mol-1 à −182,81 °C[7] |
| ΔvapH° | 9,76 kJ·mol-1 à 25 °C 14,703 kJ·mol-1 à −89,05 °C[7] |
| Cp | 52,49 J·mol-1·K-1 (25 °C, gaz) 68,68 J·mol-1·K-1 (−173,15 °C, liquide)[7] |
| PCI | −1 560,7 kJ·mol-1[7] |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 11,56 ± 0,02 eV (gaz)[10] |
| Cristallographie | |
| Classe cristalline ou groupe d’espace | P21/n [11] |
| Paramètres de maille | a = 4,226 Å b = 5,623 Å |
| Volume | 190,10 Å3 [11] |
| Précautions | |
| SGH[12] | |
| H220 |
|
| SIMDUT[13] | |
  A, B1, |
|
| NFPA 704 | |
| Transport[3] | |
| Écotoxicologie | |
| LogP | 1,81[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'éthane est un hydrocarbure de la famille des alcanes de formule brute C2H6. C'est un gaz combustible, incolore et inodore que l'on peut trouver dans le gaz naturel et aussi dans les gaz du pétrole.
Utilisation
L'éthane est le réactif de base pour la synthèse de l'éthylène via le vapocraquage, de monochloro-, du 1,1-dichloro-, et du 1,1,1-trichloroéthane par chloration. En combinant la chloration avec l'oxychloration, le chlorure de vinyle peut être synthétisé et la réaction de l'éthane avec l'acide nitrique en phase gazeuse permet la formation du nitrométhane et du nitroéthane[15].
L'éthane est un constituant du gaz de pétrole liquéfié qui est un combustible utilisé comme remplaçant du gaz naturel pour des applications particulières.
Propriétés physico-chimiques
L'éthane se décompose à partir d'une température de 500 °C. Sa solubilité dans l'eau et dans l'alcool est meilleure que celle du méthane puisque, à 20 °C, celle-ci est de 4,7 cm-3 pour 100 cm-3 d'eau et de 150 cm-3 pour 100 cm-3 d'alcool.
Production et synthèse
L'éthane est principalement issu de la purification du gaz naturel ou extrait du gaz de pétrole liquéfié, une fraction du pétrole[15].
Transport
Il est actuellement transporté liquéfié, mais pourrait aussi un jour l'être sous forme d'hydrate d'éthane (clathrate) [16]
Écologie
Sur Terre, on mesure des dégagements de l'ordre de quinze mégatonnes de ce gaz dans l'atmosphère par an :
- deux à quatre mégatonnes sont libérées par les volcans de boue, sources géothermales, bassins pétroliers et microfuites de gaz au fond des océans ;
- une dizaine de mégatonnes proviennent des feux de forêt, de l’activitié biologique des océans, de la faune et des êtres humains[17].
- une quantité à ce jour non mesurée provient de fuites de forages, canalisation ou installations pétrogazières
Notes et références
- ETHANE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée « Ethane » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 19 avril 2009 (JavaScript nécessaire)
- « ETHANE », sur Hazardous Substances Data Bank (consulté le )
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 0387690026, lire en ligne), p. 294
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- (en) « Ethane », sur NIST/WebBook, consulté le 11 février 2010
- (en) William M. Haynes, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 91e éd., 2610 p. (ISBN 9781439820773, présentation en ligne), p. 14-40
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co., (ISBN 0-88415-857-8)
- (en) David R. Lide, Handbook of chemistry and physics, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- « Ethane », sur www.reciprocalnet.org (consulté le )
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Éthane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « éthane », sur ESIS, consulté le 15 février 2009
- Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke, Ullmann's Encyclopedia of Industrial Chemistry, Hydrocarbons, Wiley-VCH Verlag GmbH & Co,
- R. Kumar, P. Linga, I. Moudrakovski, J. A. Ripmeester, and P. Englezos, Structure and kinetics of gas hydrates from methane/ethane/propane mixtures relevant to the design of natural gas hydrate storage and transport facilities. AlChE J. 2008; 54 (8), 2132–2144.
- Sciences & Vie, On sait ce que la Terre dégaze d’hydrocarbures, nº 1098, mars 2009, p. 34.