Phénol (composé)
| Phénol | |

| |
| Identification | |
|---|---|
| Nom UICPA | Phénol |
| Synonymes |
Acide phénique |
| No CAS | |
| No ECHA | 100.003.303 |
| No CE | 203-632-7 |
| DrugBank | DB03255 |
| FEMA | 3223 |
| SMILES | |
| InChI | |
| Apparence | cristaux incolores à jaunes ou rose clair, d'odeur caractéristique[1] |
| Propriétés chimiques | |
| Formule | C6H6O [Isomères] |
| Masse molaire[4] | 94,111 2 ± 0,005 5 g/mol C 76,57 %, H 6,43 %, O 17 %, |
| pKa | pKa(PhOH2+/PhOH) = -6,4 pKa(PhOH/PhO-) = 9,95 |
| Moment dipolaire | 1,224 ± 0,008 D[2] |
| Diamètre moléculaire | 0,557 nm[3] |
| Propriétés physiques | |
| T° fusion | 43 °C[1] |
| T° ébullition | 182 °C[1] |
| Solubilité | 98 g·l-1 d'eau |
| Paramètre de solubilité δ | 25,1 J1/2·cm-3/2 (40 °C)[3] ; 11,4 cal1/2·cm-3/2[5] |
| Masse volumique | 1,073 g·cm-3[6]
|
| T° d'auto-inflammation | 715 °C[1] |
| Point d’éclair | 79 °C (coupelle fermée)[1] |
| Limites d’explosivité dans l’air | 1,36–10 %vol[1] |
| Pression de vapeur saturante | à 20 °C : 47 Pa[1]
|
| Point critique | 61,3 bar, 694,2 K[8] |
| Thermochimie | |
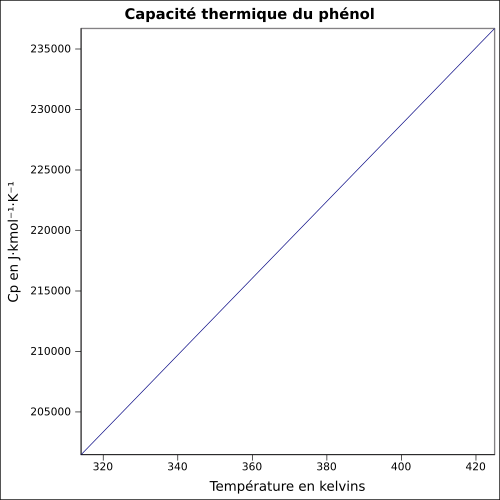
| Cp | |
| Cristallographie | |
| Classe cristalline ou groupe d’espace | P1121[10] |
| Paramètres de maille | a = 6,050 Å b = 8,925 Å |
| Volume | 788,01 Å3[10] |
| Propriétés optiques | |
| Indice de réfraction | 1,5427[3] |
| Précautions | |
| SGH[12] | |
| H301, H311, H314, H331, H341 et H373 |
|
| SIMDUT[13] | |
  D1A, E, |
|
| NFPA 704 | |
| Transport[14] | |
| Classification du CIRC | |
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme[11] | |
| Écotoxicologie | |
| LogP | 1,46[1] |
| Seuil de l’odorat | bas : 0,004 5 ppm haut : 1 ppm[15] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le phénol, appelé aussi hydroxybenzène, acide phénique, ou encore acide carbolique, est composé d'un noyau phénylène et d'une fonction hydroxyle. C'est la plus simple molécule de la famille des phénols.
Représentations
-
Modèle compact
-
Modèle boules et bâtonnets
Origine
Découvert à l'état impur par Johann Rudolf Glauber en 1650 à partir de la distillation du goudron de houille. Il le décrit comme « une huile vive et rouge de sang qui assèche et guérit tous les ulcères humides ». En 1834, Friedrich Ferdinand Runge parvient à l'isoler et le nomme alors acide carbolique. Il fut synthétisé et manufacturé en 1889 par la firme BASF.
Énol
Le phénol est aussi un énol (dérivé alcoolique possédant une fonction alcène). Il est la forme tautomère de la cyclohexa-2,4-diènone. Mais contrairement à la majorité des énols, il est la forme la plus stable comparé à sa cétone tautomère, stabilité due en majorité à la présence d'un cycle aromatique non présent dans la cétone correspondante.
Propriétés physiques

Le phénol a une constante molale cryoscopique de 6,84 °C∙kg/mol et une constante molale ébullioscopique de 3,54 °C∙kg/mol.
De couleur blanche à l'état pur, il a tendance à s'oxyder légèrement au contact de l'air pour donner des traces de quinones qui le colorent en rose, puis en rouge.
Production
En 2005, le phénol a été produit à hauteur de 8,8 millions de tonnes dans le monde, dont environ 26 % aux États-Unis et 2 % en France. Le principal producteur est Ineos Phenol[16] (Royaume-Uni) avec une capacité de production de 1,6 million de tonnes[17].
Le phénol est produit aujourd'hui à plus de 85 % par le procédé au cumène. Ce procédé, mis au point en 1944 par Hock et Lang, est utilisé depuis les années 1950[17]. Son avantage réside dans la simplicité de sa mise en œuvre, son bon rendement (90 %) et le fait d'obtenir phénol et acétone à partir du cumène, disponible en grande quantité par pétrochimie. Il consiste en une oxydation du cumène par l'air fournissant l'hydroperoxyde de cumène en tant qu'intermédiaire qui, en milieu aqueux acide, donne du phénol et de l'acétone.
Utilisation
- Les deux tiers de la production de phénol sont utilisés pour produire des plastiques (polycarbonates, résines époxyde).
- Intermédiaire important pour de nombreuses synthèses de produits pharmaceutiques. Voir Phénol (groupe).
- En parfumerie : thymol, estragol, eugénol, vanilline, etc.
- En médecine, il est surtout utilisé comme antiseptique puissant.
- En biologie moléculaire, le phénol est utilisé pour éliminer les protéines dans les protocoles d'extraction d'acides nucléiques.
- Préparation de la phénolphtaléine, un indicateur pH-métrique bien connu des chimistes.
- Par action du chlore gazeux sur le phénol, on obtient des chlorophénols, tels le 2,4,6-trichlorophénol.
- Utilisé en entomologie pour la conservation des planches d'insectes contre les moisissures.
- En alimentation, pour la conservation de la viande.
- Le phénol est utilisé pour la production de papier.
Sécurité
Le phénol est fortement corrosif pour les organismes vivants. Une solution aqueuse à 1 % suffit à provoquer des irritations sévères.
Les brûlures au phénol sont très douloureuses et longues à guérir. De plus, elles peuvent être suivies de complications graves pouvant mener à la mort de par la toxicité de ce composé et sa capacité à pénétrer dans l’organisme en traversant la peau.
Durant la Seconde Guerre mondiale, des prisonniers d'Auschwitz ont été exécutés par une piqûre de phénol dans le cœur. Maximilien Kolbe a été tué par une injection de phénol dans le bras après quatorze jours de détention sans nourriture.
Articles connexes
- Crésol, phénol substitué par un groupe méthyle
- Pyrocatéchol, phénol substitué par un groupe hydroxyle en position ortho
- Résorcine, phénol substitué par un groupe hydroxyle en position méta
- Hydroquinone, phénol substitué par un groupe hydroxyle en position para
- Pyrogallol et Phloroglucinol, deux isomères trihydroxybenzène
- Liste d'acides
Notes et références
- PHENOL, Fiches internationales de sécurité chimique
- (en) David R. Lide, Handbook of chemistry and physics, CRC, , 89e éd., 2736 p. (ISBN 142006679X et 978-1420066791), p. 9-50
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Royaume-Uni, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Șerban Moldoveanu, Sample preparation in chromatography, Elsevier, , 930 p. (ISBN 0444503943), p. 258
- (en) J. G. Speight, Norbert Adolph Lange, Lange's handbook of chemistry, McGraw-Hill, , 16e éd., 1623 p. (ISBN 0071432205), p. 2.289
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 2, Huston, Texas, Gulf Pub. Co., (ISBN 0-88415-858-6)
- (en) « Phenol », sur www.reciprocalnet.org (consulté le )
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Évaluations Globales de la Cancérogénicité pour l'Homme, Groupe 3 : Inclassables quant à leur cancérogénicité pour l'Homme », sur http://monographs.iarc.fr, CIRC, (consulté le )
- Numéro index (en) dans le tableau 3.1 de l'annexe VI du règlement CE no 1272/2008 (16 décembre 2008)
- « Phénol » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Entrée « Phenol » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 25 août 2009 (JavaScript nécessaire)
- (en) « Phenol », sur hazmap.nlm.nih.gov (consulté le )
- (en) Site institutionnel
- Données sur la production industrielle de phénol, Société chimique de France, 8e éd., 2009