Isoflavone

Les isoflavones sont une sous-famille des flavonoïdes très étudiée pour leurs propriétés pseudo-œstrogéniques. Ce sont les isomères de flavones, avec une structure quasi identique, la seule différence étant la position du groupe phényle, lié au carbone 3 au lieu du carbone 2 pour les flavones.
Principales isoflavones
| Nom | Structure | R5 | R6 | R7 | R8 | R3' | R4' | R5' | CAS | Nom IUPAC |
|---|---|---|---|---|---|---|---|---|---|---|
| Isoflavone | 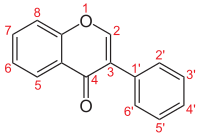 |
H | H | H | H | H | H | H | 3-phénylchromén-4-one | |
| Biochanine A | OH | H | OH | H | H | OCH3 | H | 5,7-dihydroxy-3-(4-methoxyphenyl)chromen-4-one | ||
| Calycosine | H | H | OH | H | OH | OCH3 | H | 7-hydroxy-3-(3-hydroxy-4-méthoxyphenyl)chromén-4-one | ||
| Daidzéine | H | H | OH | H | H | OH | H | 7-hydroxy-3-(4-hydroxyphényl)chromén-4-one | ||
| Formononétine | H | H | OH | H | H | OCH3 | H | 7-hydroxy-3-(4-méthoxyphényl)chromén-4-one | ||
| Génistéine | OH | H | OH | H | H | OH | H | 5,7-dihydroxy-3-(4-hydroxyphényl)-4H-chromén-4-one | ||
| Glycitéine | H | OCH3 | OH | H | H | OH | H | 7-hydroxy-3-(4-hydroxyphényl)-6-méthoxy-4-chroménone | ||
| Irigénine | OH | OCH3 | OH | H | OH | OCH3 | OCH3 | 5,7-dihydroxy-3-(3-hydroxy-4,5-diméthoxyphényl)-6-méthoxychromén-4-one | ||
| 5-O-méthylgénistéine | OCH3 | H | OH | H | H | OH | H | 7-hydroxy-3-(4-hydroxyphényl)-5-méthoxychromén-4-one | ||
| Orobol | OH | H | OH | H | OH | OH | H | 3-(3,4-dihydroxyphényl)-5,7-dihydroxychromén-4-one | ||
| Pratenséine | OH | H | OH | H | OH | OCH3 | H | 5,7-dihydroxy-3-(3-hydroxy-4-méthoxyphényl)chromén-4-one | ||
| Prunétine | OH | H | OCH3 | H | H | OH | H | 5-hydroxy-3-(4-hydroxyphényl)-7-méthoxychromén-4-one | ||
| Psi-tectorigénine | OH | H | OH | OCH3 | H | OH | H | 5,7-dihydroxy-3-(4-hydroxyphényl)-8-méthoxychromén-4-one | ||
| Rétusine | H | H | OH | OH | H | OCH3 | H | 7,8-dihydroxy-3-(4-méthoxyphényl)chromén-4-one | ||
| Santal | OH | H | OCH3 | H | OH | OH | H | 5-hydroxy-3-(3,4-dihydroxyphenyl)-7-méthoxychromén-4-one | ||
| Tectorigénine | OH | OCH3 | OH | H | H | OH | H | 5,7-dihydroxy-3-(4-hydroxyphényl)-6-méthoxychromén-4-one |
Occurrence naturelle
Les isoflavones sont présentes chez toutes les plantes mais seules les plantes de la famille des Fabaceae (« légumineuses ») contient des quantités significatives d'isoflavones. Des analyses dans de nombreuses espèces ont montré que les plus hauts niveaux en génistéine et daidzéine — les isoflavones le plus courantes dans la nature — se trouve dans les psoralea (Psoralea corylifolia). De nombreuses légumineuses, incluant le soja (Glycine max L.), le haricot vert (Phaseolus vulgaris L.), les pousses de luzerne (Medicago sativa L.), le haricot mungo (Vigna radiata L.), le voème (Vigna unguiculata L.), les racines de kudzu (Pueraria lobata L.), ainsi que la fleur et la pousse de trèfle des prés (Trifolium pratense L.) ont été étudiées pour leur activité œstrogénique[1]. Les aliment hautement transformés fait à partir de légumineuses, tels que le tofu, retiennent la plus grande partie de leur contenu en isoflavones, à l'exception du miso fermenté qui lui contient des niveaux plus élevés.
On peut citer parmi les autres sources alimentaires en isoflavones le pois chiche (biochanine A), la luzerne (formononétine) et l'arachide (génistéine).
Dans les tissus végétaux, les isoflavones les plus fréquemment rencontrés sont les hétérosides d'isoflavones ou leur conjugués malonate ou acétyl respectifs, ce qui les rend encore plus soluble dans l'eau (voir isoflavone-7-O-bêta-glucoside 6"-O-malonyltransférase). Ces dernières formes sont toutefois instables et sont donc transformées, par exemple par décarboxylation. Souvent, lorsque les légumineuse doivent faire face à une infection viral ou fongique, la forme soluble dans l'eau sert pour le transport et est hydrolysée en aglycone correspondant sur le site cible[2].
L'actéine et le cimicifucoside sont deux isoflavones à triterpènes présentes dans Actaea racemosa[3].
Il existe une base de données des teneurs en isoflavones de nombreux produits alimentaires[4].
Biosynthèse
Les isoflavones sont biosynthétisées via une branche de la voie générale des phénylpropanoïdes, voie qui produit notamment les flavonoïdes chez les plantes supérieures. Cette voie débute à partir d'un acide aminé, la phénylalanine qui es transformée en acide cinnamique ou l'un de ses dérivés, lui-même transformé en dérivé de l'acide paracoumarique qui donne une chalcone, précurseurs de la plupart des flavonoïdes. Dans la nature, les principales isoflavones, présentes dans le soja, sont la génistéine et la daidzéine. La première est produite à partir de la naringinine, une flavanone (flavonoïde), qui est convertie par l'action de deux enzymes spécifiques, l'isoflavone synthase et une déshydratase. De façon similaire, la naringinine chalcone est convertie daidzéine par l'action successives de trois enzymes spécifiques, la chalcone reductase, la chalcone isomerase de type II et l'isoflavone synthase.
Intérêt biologique
Plantes
Les plantes utilisent les isoflavones et leur dérivés comme phytoalexine afin de se protéger de champignons pathogènes et d'autres microbes. Le soja utilise également les isoflavones pour stimuler les rhizobium afin de former des nodosités fixatrices d'azote.
Nutrition humaine
Les isoflavones présentant un intérêt nutritionnel sont les dérivés hydroxylés de l'isoflavone, cette dernière n'en ayant pas. Du fait de leur relative rareté, à l'exception du soja, la consommation d'isoflavones est négligeable en Europe, à l'exception des consommateurs de lait de soja (certains nourrissons, etc.), mais les apports alimentaires en sont très importants dans les pays d'Extrême-Orient (environ 30-40 mg/jour). L'effet estrogénique ne semble pas systématique[5], les études apportant des résultats nuancés, mais les isoflavones montrent des interactions métaboliques nombreuses[6].
Les isoflavones du soja ont des effets bénéfiques sur
- le fonctionnement du cœur
- la souplesse du système sanguin.
- La génistéine est un antioxydant (le principal dans le soja), faiblement œstrogénique (1/100ème de la force œstrogénique de l’hormone œstrogène même). Contrairement à la daidzéine, la génistéine se montre (expérimentalement et par injection) capable de fortement assouplir les vaisseaux sanguins (vasodilatation augmentée d'un facteur 2 à 3 dans l'avant-bras après injection)[7].
- le maintien du capital osseux des femmes post-ménopausées
Cependant certains effets indésirables doivent être mentionnés[8]:
- action indirecte sur la thyroïde entraînant une relative hypothyroïdie.
- chez l'homme, diminution de la testostérone (ou action antagoniste) conduisant à une diminution de la libido.
Au niveau des autorités sanitaires, il semble difficile d'encourager la consommation de phyto-estrogènes alors qu'on commence à faire la chasse aux perturbateurs endocriniens comme le bisphénol A. D'où la recommandation de l'AFSSA (ANSES) sur la présence de soja dans les préparations pour nourrissons. (voir paragraphe suivant)
Précautions pour les enfants et femmes enceintes ou allaitantes
L'AFSSA a émis les recommandations suivantes[9] :
- les préparations aux protéines de soja ne devraient pas être données aux enfants avant 3 ans si celles-ci ne sont pas à teneur réduite en isoflavones.
Compte tenu de leur composition, les tonyus (jus de soja) sont contre-indiqués pour l'alimentation des nourrissons et des enfants en bas-âge (de la naissance à trois ans). - La femme enceinte et allaitante doit éviter une consommation élevée d'isoflavones, notamment sous la forme de compléments alimentaires.
Les études animales[réf. nécessaire] montrent en effet que les phases précoces du développement des organes sexuels (pendant la gestation et la lactation) sont particulièrement sensibles à l'exposition aux phyto-œstrogènes.
Des anomalies morphologiques pouvant entraîner une diminution de la fertilité mais aussi une plus grande sensibilité aux carcinogènes sont observées.
La consommation de préparations à base de protéines de soja devrait donc, dans le cas des nourrissons et des femmes enceintes, être inférieure à 1 mg·L-1 de préparation reconstituée (en équivalents aglycone46, soit environ 0,15 mg·kg-1 de poids corporel).
Notes et références
- (en) Boue, S., Wiese, T., Nehls, S., Burow, M., Elliott, S., Carter-Wientjes, C., Shih, B., McLachlan, J., Cleveland, T., « Evaluation of the Estrogenic Effects of Legume Extracts Containing Phytoestrogens », Journal of Agriculture and Food Science, vol. 53, no 8, , p. 2193–2199 (DOI 10.1021/jf0211145)
- (en) Long-ze Lin et al., « LC-ESI-MS Study of the Flavonoid Glycoside Malonates of Red Clover (Trifolium pratense) », Journal of Agricultural and Food Chemistry, vol. 2, no 48, , p. 354–365 (DOI 10.1021/jf991002)
- Gérard Chenuet et al., Phytothérapie : la santé par les plantes, Vidal - Sélection du reader's digest, , 320 p. (ISBN 978-2-7098-1851-3)
- (en)[PDF] Base de données isoflavones de l'USDA
- [1]
- (en) Revue des interactions connues sur le site www.goodearthnaturalfoods.net
- Circulation, 2001 ; 103 :258-262 cité par Nutranews0501
- (en) Effets indésirables des isoflavones
- Rapport de l'AFSSA sur les phyto-œstrogènes
