Détresse respiratoire
| Causes | Pneumopathie, insuffisance cardiaque, syndrome de détresse respiratoire aiguë, décompensation de BPCO. |
|---|---|
| Symptômes | Dyspnée, cyanose. |
| Traitement | Oxygénothérapie et traitement de la cause. |
|---|---|
| Spécialité | Médecine d'urgence, pneumologie et réanimation. |
| CISP-2 | R99 |
|---|---|
| CIM-10 | J96.0 |
| DiseasesDB | 6623 |
| eMedicine | 167981 |
| MeSH | D012131 |
La détresse respiratoire est une insuffisance respiratoire survenant de manière brutale et se manifestant par une dyspnée importante (essoufflement). Le système respiratoire ne parvient alors plus à assurer les échanges gazeux normaux d'oxygène et de dioxyde de carbone. C'est une urgence médicale qui peut engager le pronostic vital du patient, et entraîne environ un tiers des hospitalisations en unité de réanimation.
Il existe deux grands types de détresse respiratoire : hypoxémique, lorsque seule la pression partielle de dioxygène dans le sang artériel est abaissée, et hypercapnique, lorsque se surajoute une élévation de la pression partielle en dioxyde de carbone.
Le diagnostic de détresse respiratoire est avant tout clinique : peu d'examens complémentaires sont nécessaires, et ceux-ci sont dominés par la mesure du contenu en oxygène du sang par un saturomètre, l'étude des gaz du sang par un prélèvement artériel et la radiographie pulmonaire. D'autres examens vont cependant permettre d'affiner le diagnostic étiologique et d'identifier le processus causant la défaillance.
Adultes comme enfants peuvent souffrir d'une détresse respiratoire. Chez l'adulte, les infections pulmonaires, les décompensations de bronchite chronique, le syndrome de détresse respiratoire aiguë (SDRA) et l'insuffisance cardiaque, figurent parmi les causes les plus fréquentes. Chez le jeune enfant, les bronchiolites et les infections pulmonaires bactériennes sont les plus impliquées. Chez le nouveau-né, le SDRA et l'inhalation de méconium sont principalement en cause.
Le traitement des détresses respiratoires est basé en premier lieu sur l'apport supplémentaire d'oxygène inhalé. Ceci peut être réalisé dans un premier temps par des lunettes à oxygène, un masque à haute concentration ou un système d'oxygénothérapie nasale à haut débit. Si ce traitement est insuffisant, une assistance ventilatoire est mise en place. Celle-ci peut être non invasive, par un masque naso-buccal apportant de l'air sous pression au patient, ou invasive, par intubation trachéale. En dernier recours, dans certains cas, une oxygénation par membrane extracorporelle (ECMO) peut être mise en route. La cause de la détresse respiratoire est traitée en parallèle.
Le traitement est suivi principalement par les symptômes, le saturomètre et l'analyse des gaz du sang artériel.
Le pronostic des détresses respiratoires est très variable selon la cause. La létalité globale est d'environ 30 %, et plus élevée pour les patients aux âges extrêmes de la vie, chez ceux porteurs d'importantes comorbidités, et ceux présentant une plus grande gravité initiale. Chez les patients survivants, la récupération de la fonction pulmonaire est longue, mais les séquelles respiratoires généralement modérées. La qualité de vie peut cependant rester altérée pendant plusieurs années.
Épidémiologie[modifier | modifier le code]
L'incidence des détresses respiratoires est, en Europe de l'Ouest, entre 78 et 150 pour 100 000 habitants[1],[2].
Une étude réalisée en 2002 auprès d'environ 1 500 patients adultes admis en unité de réanimation dans seize pays[3] a retrouvé que 32 % étaient admis pour une détresse respiratoire. Parmi les patients admis pour d'autres raisons, 35 % ont présenté une détresse respiratoire au cours de l'évolution de leur pathologie initiale.
Concernant les enfants, il s'agit d'un motif fréquent d'admission en réanimation pédiatrique, concernant jusqu'à deux tiers des patients[4]. Dans une étude britannique sur les motifs d'admission en unités de soins intensifs pédiatriques[5], les causes respiratoires concernaient 20 % des enfants en 1982, 19 % en 1995, et 27 % en 2006.
Définition et physiopathologie[modifier | modifier le code]
Généralités[modifier | modifier le code]
Une défaillance respiratoire aiguë survient lorsque le système respiratoire, de manière brutale[6], ne parvient plus à assurer les échanges gazeux de dioxygène et de dioxyde de carbone[7],[8]. Elle est définie habituellement par l'analyse des gaz dissous dans le sang artériel. Une pression partielle artérielle en oxygène (PaO2) inférieure à 60 mmHg (soit 8,0 kPa) est la valeur seuil retenue pour définir l'état d'hypoxémie[7],[9]. Celle-ci se reflète par une baisse de l'oxymétrie de pouls, avec une saturation en oxygène périphérique (SpO2) entre 80 et 94 %[10].
Types de détresse respiratoire[modifier | modifier le code]
On distingue généralement[7],[8],[11] :
- L'insuffisance respiratoire hypoxémique, dite de « type 1 » ;
- L'insuffisance respiratoire hypercapnique, dite de « type 2 » ;
- Certains médecins[12] distinguent également les insuffisances respiratoires aiguës, dite de « type 3 » (en contexte péri-opératoire) et de « type 4 » (survenant au cours d'un état de choc hémodynamique).
Insuffisance respiratoire hypoxémique[modifier | modifier le code]
L'insuffisance respiratoire hypoxémique peut survenir dans plusieurs circonstances entraînant une défaillance du poumon lui-même[7] : inadéquation du rapport ventilation/perfusion, apparition d'un effet shunt, altération de la diffusion alvéolo-capillaire, ou hypoventilation alvéolaire.
Insuffisance respiratoire hypercapnique[modifier | modifier le code]
L'insuffisance respiratoire hypercapnique survient lors d'anomalies de la mécanique de la ventilation empêchant l'élimination du CO2. L'hypoxémie est alors accompagnée d'une hypercapnie, définie par une PaCO2 supérieure à 45 mmHg (soit 6,0 kPa)[7]. L'accumulation du CO2 abaisse le pH sanguin ; une acidose respiratoire s'installe lorsqu'il devient inférieur à 7,35[9].
Cas particulier des enfants[modifier | modifier le code]
Les enfants, en particulier les plus jeunes, sont plus susceptibles de présenter une détresse respiratoire que les adultes[4],[9]. En effet, les sections plus réduites de leurs voies respiratoires augmentent la résistance à l'écoulement de l'air, et facilite l'obstruction bronchique par les sécrétions ou l’œdème. La moindre rigidité de leur paroi thoracique participe également à l'augmentation du travail ventilatoire. Le diaphragme et les muscles respiratoires accessoires contiennent également moins de fibres musculaires lentes que ceux de l'adulte, ce qui facilite l'épuisement respiratoire. Enfin, les très jeunes enfants ont un système nerveux immature qui les prédispose à l'apnée et à la bradypnée.
Signes cliniques[modifier | modifier le code]
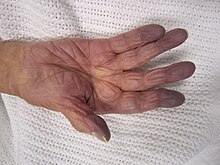
Le diagnostic de détresse respiratoire est avant tout clinique, et peut être établi directement au lit du patient[9]. Le tableau clinique combine les conséquences directes de l'atteinte de l'appareil respiratoire, et les mesures de compensation mises en œuvre par l'organisme.
Les signes de lutte[6] sont dominés par une augmentation de la fréquence respiratoire (polypnée) pouvant être associée à un tirage des muscles respiratoires.
Les signes de gravité[6], aussi appelés signes de faillite, varient selon les organes atteints. Ils traduisent le retentissement global de la détresse respiratoire et indiquent le plus souvent la nécessité d'une assistance ventilatoire. Au plan respiratoire, la respiration abdominale paradoxale et la cyanose sont les signes majeurs. Cette dernière peut manquer en cas d'anémie majeure, si le taux d'hémoglobine est inférieur à 5 g·dl-1. Au plan neurologique, l'hypercapnie, lorsqu'elle est présente, entraîne un astérixis et des troubles de la vigilance et du comportement (agitation ou coma)[9]. Enfin, au plan circulatoire, le cœur pulmonaire aigu est une défaillance cardiaque droite. Il est accompagné d'un pouls paradoxal, et peut s'associer à une défaillance cardiovasculaire allant jusqu'à l'état de choc.
Lorsqu'une hypercapnie est présente[6], le tableau peut se compléter de sueurs abondantes.
Les patients, adultes comme enfants, porteurs de maladies neuromusculaires, peuvent présenter peu de signes cliniques[9] ; dans ces populations, la détresse respiratoire doit être facilement évoquée et une gazométrie artérielle réalisée. Chez les personnes âgées, les signes cliniques moins francs peuvent mener à une errance diagnostique[13].
Examens complémentaires[modifier | modifier le code]

Les mesures des constantes physiologiques (fréquence cardiaque et respiratoire, tension artérielle, saturation en oxygène) complètent l'examen clinique et permettent d'évaluer rapidement la gravité de la situation. Peu d'examens complémentaires sont nécessaires à l'établissement du diagnostic de détresse respiratoire[9]. Dans l'urgence, la radiographie thoracique et la gazométrie sanguine artérielle sont les seuls examens requis pour en faire le diagnostic[6]. Selon les premiers éléments d'orientation, d'autres examens pourront cependant être réalisés pour préciser la cause de la détresse respiratoire. Ils ne doivent cependant pas retarder la mise en route du traitement.
Le bilan sanguin standard peut orienter vers une cause : hyperleucocytose en cas d'infection bactérienne, élévation de la CRP en cas d'inflammation, augmentation des D-dimères en cas d'embolie pulmonaire, de la BNP en cas d'insuffisance cardiaque.
L'échographie cardiaque et pleurale peuvent être utiles pour différencier les causes d'insuffisance respiratoire hypoxémique[14]. La tomodensitométrie (TDM) thoracique peut rechercher une embolie pulmonaire, des signes de fibrose, ou préciser de manière plus fine des lésions visualisées sur la radiographie pulmonaire. En contexte infectieux (fièvre ou crachats purulents), une analyse des crachats, ainsi que des hémocultures peuvent permettre de rechercher les germes responsables. Une grippe est systématiquement recherchée en période épidémique chez le patient fébrile.
La fibroscopie bronchique peut être indiquée lorsque la cause de la détresse respiratoire n'est pas évidente[15]. Elle permet de réaliser des prélèvements à visée bactériologique, mais aussi d'explorer la morphologie de l'arbre bronchique en réalisant des biopsies au besoin, et de faire un lavage bronchoalvéolaire.
Démarche diagnostique[modifier | modifier le code]

Les causes de détresse respiratoire sont nombreuses[6]. Le diagnostic étiologique repose sur l'examen clinique, complété de la radiographie thoracique et de l'analyse de la gazométrie artérielle[9],[16].
La première étape diagnostique est la vérification de la liberté des voies aériennes supérieures. Ce diagnostic est clinique. L'inhalation d'un corps étranger est la cause la plus fréquente chez l'enfant et la personne âgée souffrant de troubles de déglutition, mais toute pathologie ORL entraînant une obstruction laryngée ou trachéale est susceptible d'être en cause. Une tumeur du larynx, une sténose trachéale serrée, une épiglottite, ou un œdème de Quincke peuvent ainsi être impliqués. Lorsque les voies aériennes sont libres, la radiographie pulmonaire et l'auscultation permettent de diagnostiquer les atteintes de la plèvre et du parenchyme pulmonaire. Au niveau pleural, tout épanchement de grande abondance (pneumothorax ou épanchement liquidien) est susceptible d'entraîner une détresse respiratoire. Au niveau pulmonaire, une atélectasie est l'absence de ventilation d'un territoire plus ou moins important, souvent par obstruction mécanique. Les pneumopathies, en particulier bactériennes, touchant un volume pulmonaire important sont une cause fréquente de détresse respiratoire, de même que l’œdème pulmonaire, qu'il soit d'origine cardiaque (œdème aigu du poumon) ou lésionnelle (syndrome de détresse respiratoire aiguë ou SDRA). Dans ce dernier cas, il est important de noter qu'une pneumopathie, qu'elle soit bactérienne ou virale (par exemple à Covid-19), est susceptible d'être à l'origine du SDRA. Enfin, les atteintes des pneumopathies interstitielles peuvent être à l'origine de la détresse respiratoire[17]. Chez les patients en cours de traitement pour une maladie cancéreuse, il est important de préciser la date de la dernière chimiothérapie et, le cas échéant, d'une greffe de moëlle osseuse[16]. En effet, ces traitements sont susceptibles d'entraîner une immunodépression, et les infections opportunistes doivent alors être recherchées[16].
Lorsque la radiographie et l'examen clinique sont peu contributifs, la gazométrie artérielle permet d'orienter le diagnostic[7]. La normalité de la capnie (pression de CO2) et du pH oriente vers une embolie pulmonaire ou un asthme aigu grave. L'embolie sera recherchée par une TDM thoracique ; l'examen clinique peut être très fruste, mais également comporter des signes d'insuffisance cardiaque droite et de cœur pulmonaire aigu, en particulier en cas d'embolie massive et proximale. Lorsque la gazométrie indique une acidose respiratoire, qui se manifeste par une élévation de la capnie et des bicarbonates, la détresse respiratoire résulte généralement de la décompensation d'une pathologie chronique. Il s'agit le plus souvent de l'exacerbation d'une bronchopneumopathie chronique obstructive (BPCO). Les atteintes neuromusculaires comme la myasthénie ou un syndrome de Guillain-Barré peuvent être en cause. La poliomyélite était une cause fréquente jusqu'à l'introduction du vaccin ; la ventilation pulmonaire des patients était alors assurée, passée la phase aiguë, par un poumon d'acier. Enfin, les atteintes pariétales peuvent également être responsables d'une détresse respiratoire. Les fractures multiples de côtes peuvent être en cause, en particulier chez les patients dont l'état ventilatoire de base est précaire. Les myopathies, qu'elles soient congénitales ou acquises, sont également parfois en cause, par une atteinte des muscles inspiratoires. Dans le cas de ces maladies chroniques, il faut rechercher l'élément ayant causé la décompensation : surinfection bronchique, embolie pulmonaire, pneumopathie, chirurgie thoracique ou insuffisance cardiaque gauche peuvent alors être également responsables de la détresse respiratoire. Les intoxications aux opiacés ou autres substances ayant un effet dépresseur respiratoire peuvent également être en cause[18].
Causes[modifier | modifier le code]
La détresse respiratoire est induite par un manque de surfactant pulmonaire (surfactant dont les protéines tensioactives non seulement facilitent les échanges d'oxygène et de CO2, mais protègent contre des viroses telles que la grippe A)[19]. Ce déficit en surfactant peut avoir de multiples causes, parfois exacerbées chez les hommes car la production du surfactant pulmonaire est liée au système hormonal et principalement commandée par le chromosome X (l'homme n'en a qu'un). Elle est par exemple inhibée par la dihydrotestostérone chez le fœtus mâle et femelle. Inversement un anti-androgène (ex : flutamide) supprime le dimorphisme sexuel dans la production de surfactants[20].
Chez l'adulte[modifier | modifier le code]
Chez l'adulte, en raison d'études très hétérogènes, les données manquent sur la répartition globale des différentes causes de détresse respiratoire.
Une étude de 1995 sur une cohorte allemande a retrouvé les infections pulmonaires (15 %, dont les pneumopathies d'inhalation) en étiologie la plus fréquente, suivie des causes cardiaques avec le choc cardiogénique (13 %) et l'insuffisance cardiaque gauche (7,6 %)[21].
Une cohorte scandinave étudiée en 1999 trouvait comme première cause les infections pulmonaires (23 %), suivies des atélectasies (15 %) et des décompensations de bronchopneumopathie chronique obstructive (13 %), puis de l'insuffisance cardiaque gauche (9 %) ; le choc cardiogénique n'étant impliqué que dans 5 % des cas[22].
L'analyse d'une cohorte brésilienne en 2011 réalisée dans des unités de soins intensifs médicaux et chirurgicaux a retrouvé, en première cause médicale de détresse respiratoire, le syndrome de détresse respiratoire aiguë (SDRA) (10 %) suivi des pneumopathies (8 %), des sepsis d'origine non pulmonaire (7 %), de l'insuffisance cardiaque (6 %) et des traumatismes thoraciques (6 %). La majorité des patients (38 %) avait en revanche développé une insuffisance respiratoire aiguë dans les suites immédiates d'une chirurgie[23].
La pneumonie bactérienne communautaire n'implique une hospitalisation que dans 20 % des cas ; dont seuls 10 % présenteront une détresse respiratoire[24]. Mais chez les patients immunodéprimés, la détresse respiratoire est le premier motif d'hospitalisation en soins intensifs et réanimation, majoritairement à cause d'infections pulmonaires ; il peut s'agir aussi bien de pneumopathies à germes communautaires classiques que d'infections opportunistes, en particulier fongiques[25]. Plus rarement, il peut s'agir d'un effet secondaire de certains traitements anti-cancéreux, en particulier de chimiothérapies et de certaines thérapies ciblées pouvant être responsables de pneumopathies d'hypersensibilité comme de pneumopathies interstitielles[25]. Chez les patients atteints d'un cancer évolutif, les pneumopathies bactériennes sont cependant les causes plus fréquentes (47 %), suivies des infections opportunistes (31 %), et dans 22 % des cas de causes non infectieuses[16].
Le SDRA concerne entre 1,7 et 19,5 % de l'ensemble des patients admis en unité de réanimation adulte, avec le plus souvent des chiffres rapportés aux environs de 7 %[2],[26].
Dans le cadre des pneumopathies interstitielles comme la fibrose pulmonaire idiopathique, une détresse respiratoire peut se présenter dans deux grands cas de figure[17]. Chez les patients déjà diagnostiqués, une exacerbation aiguë correspond à la dégradation, depuis moins d'un mois, de l'état respiratoire et des lésions constatées en imagerie, sans pathologie pulmonaire associée[17],[27]. La détresse respiratoire peut toutefois être le mode de découverte de la maladie interstitielle, en particulier pour les fibroses pulmonaires idiopathiques, les connectivites et vascularites avec atteinte pulmonaire, et les fibroses médicamenteuses[17].
Chez l'enfant[modifier | modifier le code]
La première cause de détresse respiratoire chez les nouveau-nés (prématurés en général) est la carence en surfactant pulmonaire[28]. Cette détresse peut être prévenue par la corticothérapie anténatale (qui est cependant plus efficace chez les filles que chez les garçons)[20] ; cette différence de production de surfactants pulmonaires fœtaux selon le sexe est aussi observée dans le modèle animal, a priori influencé par le récepteur des androgènes (RA)[20].
Ce traitement a fait nettement baisser le nombre de maladies des membranes hyalines et il a contribué à la diminution de la mortalité infantile (moindre morbidité et mortalité des prématurés).
Chez le nouveau-né proche du terme, la cause la plus fréquente de défaillance respiratoire est le SDRA, pour 43 % des patients, suivi de l'inhalation de méconium (9,7 %) et de la pneumopathie ou du sepsis (8,3 %)[29]. La tachypnée transitoire du nouveau-né n'est impliquée que dans 4 % des cas[29], mais particulièrement fréquent chez les enfants nés par césarienne, même chez les enfants nés à terme. En l'absence du passage du fœtus dans la filière génitale resserrée, les poumons ne sont en effet pas rincés du liquide pulmonaire fœtal qu'ils contiennent.
Plus rarement, certaines cardiopathies congénitales peuvent également entraîner une détresse respiratoire.
Chez le jeune enfant, les bronchiolites sont responsables de 26,7 % des détresses respiratoires, et les pneumopathies bactériennes de 15,8 %[4]. Les œdèmes pulmonaires lésionnels sont responsables, eux, d'environ 10 % des cas, le SDRA causant un peu plus de la moitié de ceux-ci[30].
L'asthme de l'enfant est de moins en moins responsable de détresse respiratoire en raison de l'apparition de nouveaux traitements de fond[4].
Prise en charge[modifier | modifier le code]
Il s'agit d'une urgence médicale. La détresse respiratoire nécessite une prise en charge hospitalière, avec un transport médicalisé. Suivant l'état du patient, il peut y avoir une admission directe en réanimation. Le patient doit être mis au repos, en position demi assise si possible. Une perfusion intraveineuse est mise en place.
En cas d'inhalation d'un corps étranger, et si le patient est asphyxique ou ne présente pas de toux efficace, la manœuvre de Heimlich doit être réalisée en urgence.
Oxygénothérapie[modifier | modifier le code]

En raison du caractère d'urgence vitale de la détresse respiratoire, le traitement est débuté dès la phase pré-hospitalière[6]. Après s'être assuré de la liberté des voies aériennes supérieures, le premier traitement à initier en urgence est l'oxygénothérapie[31]. Celle-ci peut être réalisée de plusieurs manières[31] suivant la gravité : lunettes, masque facial haute concentration, système de haut débit nasal.
Le principal facteur limitant de l'oxygénothérapie au masque haute concentration est le débit d'oxygène. Si celui-ci peut atteindre 15 l/min, son efficacité clinique est toutefois limitée par les débits ventilatoires que le patient est capable de mobiliser[31]. En effet, lorsque le débit inspiratoire de pointe est supérieur au débit d'oxygène fourni, le volume d'air inspiré est complété par l'air de la pièce.
Les systèmes d'oxygénothérapie nasale à haut débit, jusqu'à 60 l/min, contournent cette limite particulière en permettant au patient de n'inspirer que le mélange gazeux délivré[31]. Ils sont adjoints d'un humidificateur et d'un réchauffeur permettant une meilleure tolérance du gaz délivré. Leurs canules nasales sont également mieux tolérées par les patients que les masques faciaux à haute concentration[32]. Ces systèmes ont été d'abord utilisés en pédiatrie, mais sont désormais étendus aux adultes[33],[32],[34]. Réservés aux patients possédant une activité ventilatoire spontanée suffisante, ils peuvent permettre d'éviter le passage à une authentique assistance ventilatoire[31],[17]. Cependant, les nombreux biais des études réalisées chez l'adulte ne permettent pas d'évaluer l'efficacité du traitement par rapport à l'oxygénothérapie classique[35].
Assistance ventilatoire[modifier | modifier le code]
Une assistance ventilatoire est nécessaire lorsque la sévérité de la détresse respiratoire engage le pronostic vital, et que l'on observe un ou plusieurs signes de défaillance. Elle peut également être mise en route sur des critères gazométriques d'hypoxémie résistant à l'oxygénothérapie, ou d'acidose respiratoire causée par une hypercapnie surajoutée[6].
L'assistance ventilatoire peut être réalisée de deux manières : ventilation non invasive et intubation trachéale[6]. La ventilation non invasive peut être pratiquée aux urgences ou dans un service de soins intensifs. La ventilation invasive après intubation se fait en service de réanimation.
Ventilation non invasive[modifier | modifier le code]

La ventilation non invasive (VNI) comprend toutes les méthodes d'assistance ventilatoire mécanique n'ayant pas recours à l'abord endotrachéal, où un masque nasobuccal apporte de l'air sous pression positive. En soulageant la charge de travail des muscles du thorax, elle évite l'épuisement respiratoire[36],[37]. La pression expiratoire positive qu'elle délivre permet également le recrutement des alvéoles pulmonaires[37],[38].
La VNI est réservée aux défaillances respiratoires isolées chez des patients coopérants, et doit être démarrée de manière précoce, sans attendre l'installation de l'acidose[38],[39]. Elle est contre-indiquée chez les patients porteurs d'un traumatisme de la face ou des voies aériennes hautes, d'un traumatisme cérébral sévère, et en cas d'instabilité hémodynamique[40].
L'intérêt majeur des techniques de VNI est d'éviter les complications de l'intubation[40], et d'aider à rétablir une mécanique ventilatoire physiologique[7],[38]. Le taux d'échec, défini par la nécessité d'une intubation trachéale[41], est faible. La réussite d'un traitement par VNI se mesure par la diminution de la fréquence respiratoire, l'augmentation des volumes d'air inspiré, l'amélioration de la vigilance, une moindre utilisation des muscles inspiratoires accessoires, et au plan gazométrique par une correction de l'hypoxémie et de l'hypercapnie[40].
Le développement des techniques de VNI depuis les années 1990 a ainsi permis de réduire le nombre d'intubations[5]. Dans le SDRA, l'utilisation de la VNI évite environ 50 % des intubations[42]. La VNI est recommandée en première intention dans les décompensations de BPCO[43],[44], où elle permet de réduire de 65 % le nombre d'intubations, et de diminuer la mortalité de 46 %[36]. Dans l'œdème aigu du poumon, la VNI permet de réduire le risque relatif de mortalité intrahospitalière, le taux d'intubation, et la durée de séjour[45]. Elle est également d'une grande utilité dans la gestion des traumatismes fermés du thorax avec une importante réduction de mortalité (3 % contre 22 %[42]). En ce qui concerne les pathologies neuromusculaires, la VNI est souvent utilisée, mais le manque d'études randomisées limite la possibilité de recommandations[46]. Son utilisation dans l'asthme est, elle, controversée[47], et il est recommandé de ne pas l'utiliser en première intention dans les pathologies pulmonaires interstitielles en raison de l'aggravation souvent rapide des patients[48]. La VNI possède cependant une fonction préventive en post-opératoire après chirurgie abdominale sus-mésocolique, où elle permet de diminuer le nombre d'intubations[49]. Son utilisation préventive en chirurgie thoracique est elle peu prouvée[50].
L'utilisation d'une sédation légère afin d'améliorer la tolérance de la VNI, en particulier chez le nouveau-né, est délicate en raison du caractère dépresseur respiratoire des médicaments utilisés[42],[51]. L'absence de nécessité de sédation, contrairement à l'intubation, est d'ailleurs considérée comme l'un des avantages de la technique[36]. Lorsqu'une sédation légère est utilisée, le monitorage doit être plus rapproché[43]. Plusieurs facteurs de risque d'échec de la VNI ont été identifiés[36] : asynchronisme entre le patient et la machine, claustrophobie, présence de médicaments dépresseurs respiratoires, et manque d'habitude des équipes de soin.
Lorsque la ventilation non invasive n'est pas possible, ou qu'elle ne permet pas d'amélioration du patient, une intubation trachéale est nécessaire. La réévaluation de la VNI doit être précoce, 30 minutes à 2 heures après sa mise en route, afin de ne pas retarder une intubation devenue nécessaire[39],[40].
Ventilation invasive[modifier | modifier le code]

La ventilation invasive regroupe l'intubation trachéale et la trachéotomie, deux techniques dont la finalité est d'apporter le mélange gazeux directement dans la trachée du patient. Un patient présentant des troubles de la vigilance ou d'autre contre-indication de la VNI peut bénéficier d'une intubation dès la prise en charge[11]. Par ailleurs, en cas d'obstruction des voies aériennes supérieures, par exemple par une sténose laryngée ou trachéale, la ventilation invasive permet de s'affranchir de l'obstacle afin de ventiler efficacement le patient[11]. Dans le cadre particulier des pathologies interstitielles, dont les lésions sont considérées comme irréversibles, la nécessité de ventilation invasive est associée à une telle gravité de la maladie que certains recommandent de n'intuber que les patients pouvant potentiellement bénéficier d'une greffe pulmonaire[17],[52]. Chez ces patients, il est recommandé d'éviter autant que possible la ventilation invasive, potentiellement déraisonnable[40].
Divers modes de ventilation mécanique peuvent être utilisés, selon la présence ou non d'une sédation, mais aussi selon la maladie sous-jacente[11]. Les deux principaux modes utilisés sont la ventilation contrôlée et l'aide ventilatoire[11]. Dans l'aide ventilatoire, c'est l'inspiration spontanée du patient qui déclenche le cycle de la machine. Un seuil de fréquence est généralement fixé : lorsque le patient tarde à inspirer, la machine déclenche son cycle. Au contraire, dans la ventilation contrôlée, le respirateur délivre de manière fixe un volume ou une pression donnée à une fréquence déterminée ; cela nécessite une sédation du patient afin d'éviter qu'il ne lutte contre le respirateur. Dans ce cas, la sédation doit être interrompue régulièrement de manière à évaluer la capacité du patient à une ventilation spontanée[40],[53]. En cas d'atélectasie, des manœuvres de recrutement pulmonaire, consistant en une augmentation de la pression sur une durée longue, sont quelquefois recommandées (avec un niveau de preuve faible), voire envisagées à titre préventif[54],[55].
Si l'intubation se prolonge, une trachéotomie peut être réalisée[56]. Environ 12 % des patients ayant présenté une détresse respiratoire auront besoin d'une trachéotomie[2]. Le temps médian durant lequel la trachéotomie est laissée en place est de six jours[2].
La ventilation endotrachéale permet la protection des voies aériennes de l'inhalation de salive ou de liquide gastrique[11]. L'aspiration des sécrétions bronchiques est également facilitée[11].
De par leur caractère invasif, aussi bien l'intubation que la trachéotomie peuvent être sources de complications, en particulier de pneumopathie acquise sous ventilation mécanique[57]. Il s'agit des infections nosocomiales les plus fréquentes en réanimation[58].
De 7 à 28 % des enfants atteints de bronchiolite nécessitent une intubation[4]. Pour l'asthme de l'enfant, 5 à 17 % des crises d'asthme aigu grave requièrent une intubation[59].
Oxygénation par membrane extracorporelle (ECMO)[modifier | modifier le code]

Si malgré tout l'assistance ventilatoire ne permet pas d'assurer une oxygénation et une décarboxylation correctes, une oxygénation par membrane extracorporelle (ECMO) peut être mise en route en milieu de réanimation. Un circuit d'ECMO est composé des canules permettant de drainer puis réinjecter le sang du patient, d'une pompe, et d'une membrane permettant les échanges gazeux. Dans les défaillances respiratoires, une ECMO dite veino-veineuse est préférentiellement utilisée[60],[61]. Le sang est alors drainé depuis les veines caves ou l'oreillette droite du cœur, et réinjecté dans l'oreillette droite après oxygénation et décarboxylation. Deux canules différentes peuvent être mises en place, mais il existe également des canules à double courant, permettant de recueillir le sang à l'entrée de l'oreillette droite et de le réinjecter à proximité de la valve tricuspide. Il se mélange alors avec le flux sanguin qui n'a pas été intégré dans le circuit de la pompe.
Certains systèmes permettent de ne réaliser que la décarboxylation, l'échange du CO2 à travers la membrane étant plus facile que celui de l'oxygène. Cela est particulièrement utilisé dans les décompensations de BPCO et les asthmes graves, où l'hypercapnie peut être plus importante et plus néfaste que l'hypoxémie[60]. De manière plus exceptionnelle, l'ECMO peut être utilisée pour permettre d'attendre une transplantation pulmonaire dans les cas où celle-ci est indiquée[60],[17].
Chez les enfants, l'utilisation de l'ECMO dans les populations pédiatriques est débattue dans certaines indications[62], notamment le SDRA, où elle ne semble pas permettre d'améliorer la survie[63]. En revanche, chez le nouveau-né, son utilisation reste recommandée[62].
La durée d'utilisation d'une ECMO est généralement inférieure à 28 jours (84 à 88 % des patients[61],[64]), avec une durée médiane de sept[65] à huit jours[64]. Les pathologies respiratoires interstitielles requièrent généralement des durées d'assistance plus longues. Le motif le plus fréquent de retrait d'une ECMO est la récupération de la fonction respiratoire, pour 54 % des patients[61]. La survenue de complications peut cependant imposer l'arrêt de l'ECMO.
Bien que les complications neurologiques soient moins fréquentes dans l'ECMO veino-veineuse que dans les autres formes d'assistance circulatoire, elles atteignent malgré tout 8,5 % des patients adultes et jusqu'à 20 % des nouveau-nés[61],[66]. Ces complications neurologiques sont dominées par les hémorragies intracrâniennes (42 %), les accidents vasculaires cérébraux (20 %) et la mort encéphalique (23,5 %)[61],[67]. En effet, afin d'éviter que le sang ne coagule dans le circuit d'ECMO, une anticoagulation à dose curative est nécessaire. Des complications aussi bien thrombotiques qu'hémorragiques peuvent ainsi survenir.
Le taux de survie globale des patients ayant requis une ECMO pour une défaillance respiratoire est très hétérogène selon les études. Chez l'adulte, il est compris entre 32 et 90 %[60],[64],[61]. Chez le nouveau-né, la survie est comprise entre 18 et 50 %, tandis que chez l'enfant elle est de 22 à 66 %[61].

Sevrage ventilatoire[modifier | modifier le code]
Une fois l'épisode aigu passé, l'assistance ventilatoire doit être retirée dès que possible[40],[43].
Lorsqu'un patient est intubé, cette phase de sevrage ventilatoire peut être complexe. Une trachéotomie peut parfois être réalisée ; en diminuant le travail ventilatoire, elle facilite la tâche au patient. Il n'y a pas de recommandation sur le délai de mise en place d'une trachéotomie ; l'analyse doit se faire au cas par cas[43].
Avant le retrait de la ventilation invasive, un ou plusieurs tests de sevrage sont réalisés[40]. L'assistance mécanique est alors réduite au maximum, et la ventilation spontanée du patient est surveillée. La gazométrie, la stabilité hémodynamique et le confort du patient sont également monitorés. En cas d'échec de l'épreuve de sevrage, l'assistance ventilatoire doit être reprise pour au moins 24 heures[40].
Une fois le test de sevrage réussi, plusieurs mesures doivent être prises avant l'extubation. Le patient doit être capable de tousser seul de manière efficace, être bien réveillé, et avoir peu de sécrétions bronchiques[40].
Après l'extubation, un support par VNI peut être réalisé. Cela permet de diminuer le risque de nouvelle intubation[42],[39]. Ceci est particulièrement adapté chez les patients présentant des facteurs de risque d'échec d'extubation tels que l'hypercapnie, l'insuffisance cardiaque, et la toux inefficace[39], et même recommandé chez les patients BPCO[40]. La VNI est ensuite arrêtée lorsqu'il n'existe plus de signes cliniques ou gazométriques de défaillance respiratoire[42],[39].
Il est aussi possible d'utiliser l'oxygénothérapie nasale à haut débit au lieu de la VNI après l'extubation[68], en particulier chez l'enfant et le prématuré[33].
Autres traitements[modifier | modifier le code]
Selon la cause de la détresse respiratoire, d'autres traitements plus spécifiques seront introduits[40] : antibiothérapie en cas de pneumopathie bactérienne, corticothérapie... Un épanchement pleural abondant doit être drainé. Une embolie pulmonaire nécessite une anticoagulation, et parfois une fibrinolyse. L'asthme aigu grave sera, lui, traité par des bronchodilatateurs. Les patients porteurs d'un traumatisme thoracique bénéficient également d'une analgésie péridurale. Dans les décompensations de myasthénie, la plasmaphérèse ou le traitement par immunoglobulines sont nécessaires. Lorsqu'une dénutrition est constatée, elle doit être prise en charge selon les modalités habituelles.
La kinésithérapie respiratoire quotidienne est une part importante de la prise en charge[40],[69]. Chez les patients conscients, elle facilite le drainage bronchique et améliore les capacités respiratoires en diminuant l'atélectasie. Au plan plus général, la kinésithérapie permet également de lutter contre la neuropathie de réanimation, la perte d'autonomie, et les complications du décubitus comme les escarres.
La verticalisation et le lever au fauteuil (ou au minimum la surélévation de la tête du lit chez les patients sous ventilation invasive) sont couramment pratiquées[40].
Surveillance et suivi[modifier | modifier le code]
Depuis les années 1980, l'oxymétrie de pouls permet de suivre de manière non invasive la saturation en oxygène périphérique. Cependant, sa fiabilité s'affaiblit en cas de mauvaise perfusion tissulaire (par exemple lors d'un état de choc circulatoire), d'utilisation de traitements vasoconstricteurs comme la noradrénaline, ou encore d'hypothermie[4]. Les décisions thérapeutiques concernant l'assistance ventilatoire doivent donc être prises sur une mesure directe de la PaO2, du pH et de la PaCO2 par réalisation d'une gazométrie artérielle, qui demeure l'examen de référence[4],[70]. Si le sang capillaire peut être utilisé pour estimer ces valeurs, les échantillons de sang veineux périphérique sont eux inadaptés à ces mesures[70].
Le ratio PaO2/FiO2 est calculé en divisant la pression partielle artérielle en oxygène (PaO2) par la fraction d'oxygène dans l'air inspiré (FiO2). Il permet de suivre l'évolution des œdèmes pulmonaires lésionnels, en particulier les SDRA[4].
En cas d'assistance ventilatoire, en particulier d'intubation, il est possible de monitorer indirectement la capnie grâce à la capnographie[4]. Il s'agit de l'analyse des gaz expirés, permettant de quantifier le CO2 expiré.
Le suivi par radiographie pulmonaire quotidienne est débattu chez le patient sous ventilation mécanique, en raison de la mauvaise qualité des clichés réalisés en position couchée[15]. Il est cependant nécessaire de faire une radiographie après pose d'une sonde d'intubation ou d'un cathéter veineux central afin d'en vérifier la position, et elle garde une valeur d'examen de débrouillage au cours du suivi.
Pronostic[modifier | modifier le code]
Mortalité[modifier | modifier le code]
Le pronostic d'une défaillance respiratoire aiguë est très dépendant de la cause, ainsi que de la gravité initiale[30],[71].
La mortalité globale des adultes présentant une détresse respiratoire est de 31 %[3]. Les facteurs globaux de mauvais pronostic sont la présence de comorbidités importantes, et la dénutrition[72]. Dans les pathologies pulmonaires interstitielles, le pronostic est extrêmement sombre, avec une mortalité intra-hospitalière globale de 50 %, pouvant atteindre les 96 %[73], et une espérance de vie rarement supérieure à six mois[74]. Parmi les patients parvenant à quitter l'hôpital, 42 % meurent dans l'année qui suit[73]. La mortalité des adultes atteints de SDRA est de 35 à 45 %[75].
Chez l'enfant, la mortalité globale est très variable selon les séries, allant de 24 à 34 %[9]. En 2012, les infections pulmonaires ont été responsables de 2 % de la mortalité des enfants de moins de cinq ans aux États-Unis, contre 18 % dans le monde[4]. La mortalité globale des enfants ayant présenté un œdème pulmonaire lésionnel est cependant plus élevée, proche de celle des adultes (27 %[30]). Les facteurs de mauvais pronostic sont les âges extrêmes de la vie[4] et la présence de comorbidités[4],[71], en particulier de maladies respiratoires chroniques et d'immunodépression. Par exemple, la mortalité peut atteindre 90 % chez les jeunes patients atteints de leucémie[71].
Dans la population pédiatrique, la survie globale des patients ayant nécessité une ECMO est de 57 %, avec de grandes variations selon la cause de la détresse respiratoire : les patients atteints de coqueluche ne survivent que dans 39 % des cas, contre 83 % des patients asthmatiques[4].
Séquelles[modifier | modifier le code]
Les patients, adultes ou enfants, ayant présenté un épisode de détresse respiratoire sont plus à risque de développer une pathologie pulmonaire chronique, qu'elle soit obstructive (comme asthme, BPCO, emphysème pulmonaire) ou restrictive[4],[71].
La récupération de la fonction pulmonaire est lente, pouvant aller jusqu'à un an après la sortie d'hospitalisation[71],[76]. L'atteinte observée initialement peut consister en un syndrome obstructif, restrictif ou mixte, avec ou sans diminution de la diffusion alvéolo-capillaire[76],[77]. Elle est le plus souvent modérée, et peu de patients se plaignent de dyspnée[77].
Au plan nutritionnel, les patients ont perdu en moyenne 18 % de leur poids corporel à la sortie d'unité de surveillance continue, mais 71 % retrouvent leur poids de forme en un an[76]. Si la qualité de vie est altérée en sortie d'hospitalisation, elle tend à s'améliorer durant l'année suivante[76]. Cinq ans après un SDRA, les patients adultes ont une fonction pulmonaire subnormale[78]. Ils présentent cependant toujours une limitation à l'exercice et une qualité de vie altérée[78].
Chez l'enfant, les données manquent sur les séquelles cognitives à long terme[71].
Références[modifier | modifier le code]
- Klaus Lewandowski, « Contributions to the epidemiology of acute respiratory failure », Critical Care, vol. 7, no 4, , p. 288–290 (ISSN 1364-8535, PMID 12930552, lire en ligne, consulté le ).
- (en) The FINNALI-study group, Rita Linko, Marjatta Okkonen et Ville Pettilä, « Acute respiratory failure in intensive care units. FINNALI: a prospective cohort study », Intensive Care Medicine, vol. 35, no 8, , p. 1352–1361 (ISSN 0342-4642 et 1432-1238, DOI 10.1007/s00134-009-1519-z, lire en ligne, consulté le ).
- (en) Jean-Louis Vincent, Serdar Akça, Arnaldo de Mendonça et Philip Haji-Michael, « The Epidemiology of Acute Respiratory Failure in Critically Ill Patients », Chest, vol. 121, no 5, , p. 1602–1609 (DOI 10.1378/chest.121.5.1602, lire en ligne, consulté le ).
- Schneider et coll 2012..
- (en) Poongundran Namachivayam, Frank Shann, Lara Shekerdemian et Anna Taylor, « Three decades of pediatric intensive care: Who was admitted, what happened in intensive care, and what happened afterward*: », Pediatric Critical Care Medicine, vol. 11, no 5, , p. 549–555 (ISSN 1529-7535, DOI 10.1097/PCC.0b013e3181ce7427, lire en ligne, consulté le ).
- Collège des enseignants de pneumologie, « Détresse respiratoire de l'adulte » (consulté le ).
- Roussos et coll 2003..
- Michael E. Hanley et Roger C. Bone, « Acute respiratory failure », Postgraduate Medicine, vol. 79, no 1, , p. 166–176 (ISSN 0032-5481, DOI 10.1080/00325481.1986.11699244, lire en ligne, consulté le ).
- Friedman et coll 2018.
- Rajnish K. Gupta et David A. Ewards, « Surveillance de la dépression respiratoire due aux opiacés », sur Anesthesia Patient Safety Foundation, (consulté le ).
- Markou et coll 2004.
- (en) Bishwajit Bhattacharya et Kimberly Davis, « Assessment and Management of Acute Respiratory Distress in the ICU », dans Surgical Critical Care Therapy, Springer International Publishing, (ISBN 978-3-319-71711-1, DOI 10.1007/978-3-319-71712-8_15, lire en ligne), p. 161–169.
- (en) Jean-Yves Fagon, « Acute respiratory failure in the elderly », Critical Care, vol. 10, no 4, , p. 151 (PMID 16887005, PMCID PMC1751014, DOI 10.1186/cc4982, lire en ligne, consulté le ).
- (en) Hiroshi Sekiguchi, Louis A. Schenck, Ryohei Horie et Jun Suzuki, « Critical Care Ultrasonography Differentiates ARDS, Pulmonary Edema, and Other Causes in the Early Course of Acute Hypoxemic Respiratory Failure », Chest, vol. 148, no 4, , p. 912–918 (DOI 10.1378/chest.15-0341, lire en ligne, consulté le ).
- (en) Jonathan Dakin et Mark Griffiths, « The pulmonary physician in critical care 1: Pulmonary investigations for acute respiratory failure », Thorax, vol. 57, no 1, , p. 79–85 (PMID 11809996, PMCID PMC1746170, DOI 10.1136/thorax.57.1.79, lire en ligne, consulté le ).
- (en) David Schnell, Julien Mayaux, Jérôme Lambert et Antoine Roux, « Clinical assessment for identifying causes of acute respiratory failure in cancer patients », European Respiratory Journal, vol. 42, no 2, , p. 435–443 (ISSN 0903-1936 et 1399-3003, DOI 10.1183/09031936.00122512, lire en ligne, consulté le ).
- (en) Paola Faverio, Federica De Giacomi, Luca Sardella et Giuseppe Fiorentino, « Management of acute respiratory failure in interstitial lung diseases: overview and clinical insights », BMC Pulmonary Medicine, vol. 18, no 1, , p. 70 (ISSN 1471-2466, PMID 29764401, PMCID PMC5952859, DOI 10.1186/s12890-018-0643-3, lire en ligne, consulté le ).
- (en) Albert Dahan, Leon Aarts et Terry W. Smith, « Incidence, Reversal, and Prevention of Opioid-induced Respiratory Depression: », Anesthesiology, vol. 112, no 1, , p. 226–238 (ISSN 0003-3022, DOI 10.1097/ALN.0b013e3181c38c25, lire en ligne, consulté le ).
- (en) K L Hartshorn, E C Crouch, M R White et P Eggleton, « Evidence for a protective role of pulmonary surfactant protein D (SP-D) against influenza A viruses. », Journal of Clinical Investigation, vol. 94, no 1, , p. 311–319 (ISSN 0021-9738, PMID 8040272, PMCID PMC296311, DOI 10.1172/JCI117323, lire en ligne, consulté le )
- (en) Heber C. Nielsen, Howard M. Zinman et John S. Torday, « Dihydrotestosterone Inhibits Fetal Rabbit Pulmonary Surfactant Production », Journal of Clinical Investigation, vol. 69, no 3, , p. 611–616 (ISSN 0021-9738, PMID 6916770, PMCID PMC371018, DOI 10.1172/JCI110488, lire en ligne, consulté le )
- (en) Kuiama Lewandowski, Jutta Metz, Christel Deutschmann, Heinrich Preiss, Ralf Kuhlen, Antonio Artigas et Konrad J. Falke, « Incidence, severity, and mortality of acute respiratory failure in Berlin, Germany. », American Journal of Respiratory and Critical Care Medicine, vol. 151, no 4, , p. 1121–1125 (ISSN 1073-449X et 1535-4970, DOI 10.1164/ajrccm.151.4.7697241, lire en ligne, consulté le ).
- (en) Owe R. Luhr, Kristian Antonsen, Magnus Karlsson et Sidsel Aardal, « Incidence and Mortality after Acute Respiratory Failure and Acute Respiratory Distress Syndrome in Sweden, Denmark, and Iceland », American Journal of Respiratory and Critical Care Medicine, vol. 159, no 6, , p. 1849–1861 (ISSN 1073-449X et 1535-4970, DOI 10.1164/ajrccm.159.6.9808136, lire en ligne, consulté le ).
- (en) Suelene Aires Franca, Carlos Toufen, André Luiz D. Hovnanian et André Luís P. Albuquerque, « The epidemiology of acute respiratory failure in hospitalized patients: A Brazilian prospective cohort study », Journal of Critical Care, vol. 26, no 3, , p. 330.e1–330.e8 (DOI 10.1016/j.jcrc.2010.10.010, lire en ligne, consulté le ).
- (en) Simon V. Baudouin, « The pulmonary physician in critical care 3: Critical care management of community acquired pneumonia », Thorax, vol. 57, no 3, , p. 267–271 (PMID 11867834, PMCID PMC1746268, DOI 10.1136/thorax.57.3.267, lire en ligne, consulté le ).
- (en) Bruno L. Ferreyro et Laveena Munshi, « Causes of acute respiratory failure in the immunocompromised host: », Current Opinion in Critical Care, vol. 25, no 1, , p. 21–28 (ISSN 1070-5295, DOI 10.1097/MCC.0000000000000569, lire en ligne, consulté le ).
- (en) Jean-Louis Vincent, Yasser Sakr et Marco Ranieri, « Epidemiology and outcome of acute respiratory failure in intensive care unit patients: », Critical Care Medicine, vol. 31, no Supplement, , S296–S299 (ISSN 0090-3493, DOI 10.1097/01.CCM.0000057906.89552.8F, lire en ligne, consulté le ).
- (en) Harold R. Collard, Christopher J. Ryerson, Tamera J. Corte et Gisli Jenkins, « Acute Exacerbation of Idiopathic Pulmonary Fibrosis. An International Working Group Report », American Journal of Respiratory and Critical Care Medicine, vol. 194, no 3, , p. 265–275 (ISSN 1073-449X et 1535-4970, DOI 10.1164/rccm.201604-0801CI, lire en ligne, consulté le ).
- (en) Jeevarathi Gnanaratnem et Neil N. Finer, « Neonatal acute respiratory failure: », Current Opinion in Pediatrics, vol. 12, no 3, , p. 227–232 (ISSN 1040-8703, DOI 10.1097/00008480-200006000-00009, lire en ligne, consulté le ).
- (en) Reese H. Clark, « The Epidemiology of Respiratory Failure in Neonates Born at an Estimated Gestational Age of 34 Weeks or More », Journal of Perinatology, vol. 25, no 4, , p. 251–257 (ISSN 1476-5543, DOI 10.1038/sj.jp.7211242, lire en ligne, consulté le ).
- (en) Peter G. Dahlem, Willem M. C. van Aalderen, Marije E. Hamaker, Marcel G. W. Dijkgraaf et Albert P. Bos, « Incidence and short-term outcome of acute lung injury in mechanically ventilated children », European Respiratory Journal, vol. 22, no 6, , p. 980–985 (ISSN 0903-1936 et 1399-3003, DOI 10.1183/09031936.03.00003303, lire en ligne, consulté le ).
- (en) J.R. Masclans, P. Pérez-Terán et O. Roca, « The role of high-flow oxygen therapy in acute respiratory failure », Medicina Intensiva (English Edition), vol. 39, no 8, , p. 505–515 (DOI 10.1016/j.medine.2015.05.004, lire en ligne, consulté le ).
- (en) Jeffrey J. Ward, « High-Flow Oxygen Administration by Nasal Cannula for Adult and Perinatal Patients », Respiratory Care, vol. 58, no 1, , p. 98–122 (ISSN 0020-1324 et 1943-3654, DOI 10.4187/respcare.01941, lire en ligne, consulté le ).
- (en) Dominic Wilkinson, Chad Andersen, Colm PF O'Donnell et Antonio G De Paoli, « High flow nasal cannula for respiratory support in preterm infants », Cochrane Database of Systematic Reviews, (DOI 10.1002/14651858.CD006405.pub3, lire en ligne, consulté le ).
- (en) M. Nishimura, « High-Flow Nasal Cannula Oxygen Therapy in Adults: Physiological Benefits, Indication, Clinical Benefits, and Adverse Effects », Respiratory Care, vol. 61, no 4, , p. 529–541 (ISSN 0020-1324 et 1943-3654, DOI 10.4187/respcare.04577, lire en ligne, consulté le ).
- (en) Amanda Corley, Claire M Rickard, Leanne M Aitken et Amy Johnston, « High-flow nasal cannulae for respiratory support in adult intensive care patients », Cochrane Database of Systematic Reviews, (PMID 28555461, PMCID PMC6481761, DOI 10.1002/14651858.CD010172.pub2, lire en ligne, consulté le ).
- (en) Christian R Osadnik, Vanessa S Tee, Kristin V Carson-Chahhoud et Joanna Picot, « Non-invasive ventilation for the management of acute hypercapnic respiratory failure due to exacerbation of chronic obstructive pulmonary disease », Cochrane Database of Systematic Reviews, (PMID 28702957, PMCID PMC6483555, DOI 10.1002/14651858.CD004104.pub4, lire en ligne, consulté le ).
- (en) « International Consensus Conferences in Intensive Care Medicine: Noninvasive Positive Pressure Ventilation in Acute Respiratory Failure: Organized Jointly by the American Thoracic Society, the European Respiratory Society, the European Society of Intensive Care Medicine, and the Société de Réanimation de Langue Française, and approved by the ATS Board of Directors, December 2000 », American Journal of Respiratory and Critical Care Medicine, vol. 163, no 1, , p. 283–291 (ISSN 1073-449X et 1535-4970, DOI 10.1164/ajrccm.163.1.ats1000, lire en ligne, consulté le ).
- Giuseppe Bello, Paolo De Santis et Massimo Antonelli, « Non-invasive ventilation in cardiogenic pulmonary edema », Annals of Translational Medicine, vol. 6, no 18, , p. 355–355 (PMID 30370282, PMCID PMC6186545, DOI 10.21037/atm.2018.04.39, lire en ligne, consulté le ).
- (en) Dean R. Hess, « Noninvasive Ventilation for Acute Respiratory Failure », Respiratory Care, vol. 58, no 6, , p. 950–972 (ISSN 0020-1324 et 1943-3654, DOI 10.4187/respcare.02319, lire en ligne, consulté le ).
- Barbas et coll 2013.
- (en) Aylin Ozsancak Ugurlu et Mehmet Ali Habesoglu, « Epidemiology of NIV for Acute Respiratory Failure in COPD Patients: Results from the International Surveys vs. the “Real World” », COPD: Journal of Chronic Obstructive Pulmonary Disease, vol. 14, no 4, , p. 429–438 (ISSN 1541-2555 et 1541-2563, DOI 10.1080/15412555.2017.1336527, lire en ligne, consulté le ).
- (en) Josep Masip et Arantxa Mas, « Noninvasive ventilation in acute respiratory failure », International Journal of Chronic Obstructive Pulmonary Disease, , p. 837 (ISSN 1178-2005, PMID 25143721, PMCID PMC4136955, DOI 10.2147/COPD.S42664, lire en ligne, consulté le ).
- Davidson et coll 2016.
- Rochwerg et coll 2017.
- (en) Nicolas Berbenetz, Yongjun Wang, James Brown et Charlotte Godfrey, « Non-invasive positive pressure ventilation (CPAP or bilevel NPPV) for cardiogenic pulmonary oedema », Cochrane Database of Systematic Reviews, (PMID 30950507, PMCID PMC6449889, DOI 10.1002/14651858.CD005351.pub4, lire en ligne, consulté le ).
- (en) Fang Luo, Djillali Annane, David Orlikowski et Li He, « Invasive versus non-invasive ventilation for acute respiratory failure in neuromuscular disease and chest wall disorders », Cochrane Database of Systematic Reviews, (PMID 29199768, PMCID PMC6486162, DOI 10.1002/14651858.CD008380.pub2, lire en ligne, consulté le ).
- (en) Wei Jie Lim, Redhuan Mohammed Akram, Kristin V Carson et Satya Mysore, « Non-invasive positive pressure ventilation for treatment of respiratory failure due to severe acute exacerbations of asthma », Cochrane Database of Systematic Reviews, (DOI 10.1002/14651858.CD004360.pub4, lire en ligne, consulté le ).
- (en) Ganesh Raghu, Bram Rochwerg, Yuan Zhang et Carlos A. Cuello Garcia, « An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline: Treatment of Idiopathic Pulmonary Fibrosis. An Update of the 2011 Clinical Practice Guideline », American Journal of Respiratory and Critical Care Medicine, vol. 192, no 2, , e3–e19 (ISSN 1073-449X et 1535-4970, DOI 10.1164/rccm.201506-1063ST, lire en ligne, consulté le ).
- (en) Debora AS Faria, Edina MK da Silva, Álvaro N Atallah et Flávia MR Vital, « Noninvasive positive pressure ventilation for acute respiratory failure following upper abdominal surgery », Cochrane Database of Systematic Reviews, (DOI 10.1002/14651858.CD009134.pub2, lire en ligne, consulté le ).
- (en) Maria FS Torres, Gustavo JM Porfírio, Alan PV Carvalho et Rachel Riera, « Non-invasive positive pressure ventilation for prevention of complications after pulmonary resection in lung cancer patients », Cochrane Database of Systematic Reviews, (PMID 30840317, PMCID PMC6402531, DOI 10.1002/14651858.CD010355.pub3, lire en ligne, consulté le ).
- (en) Roberto Bellù, Koert A de Waal et Rinaldo Zanini, « Opioids for neonates receiving mechanical ventilation », Cochrane Database of Systematic Reviews, (DOI 10.1002/14651858.CD004212.pub3, lire en ligne, consulté le ).
- (en) Fahad M Al-hameed et Sat Sharma, « Outcome of Patients Admitted to Intensive Care Unit for Acute Exacerbation of Idiopathic Pulmonary Fibrosis », Canadian Respiratory Journal, vol. 11, no 2, , p. 117–122 (ISSN 1198-2241, DOI 10.1155/2004/379723, lire en ligne, consulté le ).
- (en) John P. Kress, Anne S. Pohlman, Michael F. O'Connor et Jesse B. Hall, « Daily Interruption of Sedative Infusions in Critically Ill Patients Undergoing Mechanical Ventilation », New England Journal of Medicine, vol. 342, no 20, , p. 1471–1477 (ISSN 0028-4793 et 1533-4406, DOI 10.1056/NEJM200005183422002, lire en ligne, consulté le ).
- Alhazzani, W. Møller, M. H. Arabi, M. Loeb et al., Surviving sepsis campaign: guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID-19) - Un-edited accepted proof, European Society of Intensive Care Medicine and the Society of Critical Care Medicine, (DOI 10.1007/s00134-020-06022-5, lire en ligne)
- Thomas Godet, Audrey Johanny et Emmanuel Futier, « Quand et comment je fais une manœuvre de recrutement alvéolaire au bloc opératoire ? », MAPAR,
- (en) Nora H. Cheung et Lena M. Napolitano, « Tracheostomy: Epidemiology, Indications, Timing, Technique, and Outcomes », Respiratory Care, vol. 59, no 6, , p. 895–919 (ISSN 0020-1324 et 1943-3654, DOI 10.4187/respcare.02971, lire en ligne, consulté le ).
- JL Trouillet, « Les pneumopathies acquises sous ventilation mécanique », sur Société française d'anesthésie-réanimation, (consulté le ).
- P. Seguin et K. Hervé, « Prévention des pneumopathies acquises sous ventilation mécanique », sur sofia.medicalistes.fr, .
- (en) Christopher L. Carroll, Sharon R. Smith, Melanie S. Collins et Anita Bhandari, « Endotracheal intubation and pediatric status asthmaticus: Site of original care affects treatment*: », Pediatric Critical Care Medicine, vol. 8, no 2, , p. 91–95 (ISSN 1529-7535, DOI 10.1097/01.PCC.0000257115.02573.FC, lire en ligne, consulté le ).
- (en) Robert H. Bartlett et Kristopher B. Deatrick, « Current and future status of extracorporeal life support for respiratory failure in adults: », Current Opinion in Critical Care, vol. 22, no 1, , p. 80–85 (ISSN 1070-5295, DOI 10.1097/MCC.0000000000000274, lire en ligne, consulté le ).
- (en) Viviane G. Nasr, Lakshmi Raman, Ryan P. Barbaro et Yigit Guner, « Highlights from the Extracorporeal Life Support Organization Registry: 2006–2017 », ASAIO Journal, vol. 65, no 6, , p. 537–544 (ISSN 1058-2916, DOI 10.1097/MAT.0000000000000863, lire en ligne, consulté le ).
- Simon Erickson, « Extra-corporeal membrane oxygenation in paediatric acute respiratory distress syndrome: overrated or underutilized? », Annals of Translational Medicine, vol. 7, no 19, , p. 512–512 (PMID 31728365, PMCID PMC6828785, DOI 10.21037/atm.2019.09.27, lire en ligne, consulté le ).
- (en) Ryan P. Barbaro, Yuejia Xu, Santiago Borasino et Edward J. Truemper, « Does Extracorporeal Membrane Oxygenation Improve Survival in Pediatric Acute Respiratory Failure? », American Journal of Respiratory and Critical Care Medicine, vol. 197, no 9, , p. 1177–1186 (ISSN 1073-449X et 1535-4970, PMID 29373797, PMCID PMC6019927, DOI 10.1164/rccm.201709-1893OC, lire en ligne, consulté le ).
- (en) Soo Jin Na, Jae-Seung Jung, Sang-Bum Hong et Woo Hyun Cho, « Clinical outcomes of patients receiving prolonged extracorporeal membrane oxygenation for respiratory support », Therapeutic Advances in Respiratory Disease, vol. 13, , p. 175346661984894 (ISSN 1753-4666 et 1753-4666, PMID 31090503, PMCID PMC6535699, DOI 10.1177/1753466619848941, lire en ligne, consulté le ).
- (en) Matthew L. Paden, Steven A. Conrad, Peter T. Rycus et Ravi R. Thiagarajan, « Extracorporeal Life Support Organization Registry Report 2012: », ASAIO Journal, vol. 59, no 3, , p. 202–210 (ISSN 1058-2916, DOI 10.1097/MAT.0b013e3182904a52, lire en ligne, consulté le ).
- (en) Nikkole M. Haines, Peter T. Rycus, Joseph B. Zwischenberger et Robert H. Bartlett, « Extracorporeal Life Support Registry Report 2008: Neonatal and Pediatric Cardiac Cases: », ASAIO Journal, vol. 55, no 1, , p. 111–116 (ISSN 1058-2916, DOI 10.1097/MAT.0b013e318190b6f7, lire en ligne, consulté le ).
- (en) Roberto Lorusso, Fabio Barili, Michele Di Mauro et Sandro Gelsomino, « In-Hospital Neurologic Complications in Adult Patients Undergoing Venoarterial Extracorporeal Membrane Oxygenation: Results From the Extracorporeal Life Support Organization Registry », Critical Care Medicine, vol. 44, no 10, , e964–e972 (ISSN 0090-3493, DOI 10.1097/CCM.0000000000001865, lire en ligne, consulté le ).
- (en) Yue-Nan Ni, Jian Luo, He Yu et Dan Liu, « Can high-flow nasal cannula reduce the rate of reintubation in adult patients after extubation? A meta-analysis », BMC Pulmonary Medicine, vol. 17, no 1, , p. 142 (ISSN 1471-2466, PMID 29149868, PMCID PMC5693546, DOI 10.1186/s12890-017-0491-6, lire en ligne, consulté le ).
- (en) William D Schweickert, Mark C Pohlman, Anne S Pohlman et Celerina Nigos, « Early physical and occupational therapy in mechanically ventilated, critically ill patients: a randomised controlled trial », The Lancet, vol. 373, no 9678, , p. 1874–1882 (DOI 10.1016/S0140-6736(09)60658-9, lire en ligne, consulté le ).
- (en) Gerald S. Zavorsky, Jiguo Cao, Nancy E. Mayo et Rina Gabbay, « Arterial versus capillary blood gases: A meta-analysis », Respiratory Physiology & Neurobiology, vol. 155, no 3, , p. 268–279 (DOI 10.1016/j.resp.2006.07.002, lire en ligne, consulté le ).
- (en) Michael W. Quasney, Yolanda M. López-Fernández, Miriam Santschi et R. Scott Watson, « The Outcomes of Children With Pediatric Acute Respiratory Distress Syndrome: Proceedings From the Pediatric Acute Lung Injury Consensus Conference », Pediatric Critical Care Medicine, vol. 16, , S118–S131 (ISSN 1529-7535, DOI 10.1097/PCC.0000000000000438, lire en ligne, consulté le ).
- (en) Maki Kobayashi, Yoko Shibata, Sumito Inoue et Akira Igarashi, « Predictors for mortality from respiratory failure in a general population », Scientific Reports, vol. 6, (ISSN 2045-2322, PMID 27180927, PMCID 4867438, DOI 10.1038/srep26053, lire en ligne, consulté le ).
- (en) Whitney D. Gannon, David J. Lederer, Mauer Biscotti et Azka Javaid, « Outcomes and Mortality Prediction Model of Critically Ill Adults With Acute Respiratory Failure and Interstitial Lung Disease », Chest, vol. 153, no 6, , p. 1387–1395 (PMID 29353024, PMCID PMC6026289, DOI 10.1016/j.chest.2018.01.006, lire en ligne, consulté le ).
- (en) Demosthene Bouros, Andrew G. Nicholson, Vlasis Polychronopoulos et Roland M. du Bois, « Acute interstitial pneumonia », European Respiratory Journal, vol. 15, no 2, , p. 412 (DOI 10.1034/j.1399-3003.2000.15b31.x, lire en ligne, consulté le ).
- (en) Jason Phua, Joan R. Badia, Neill K. J. Adhikari et Jan O. Friedrich, « Has Mortality from Acute Respiratory Distress Syndrome Decreased over Time?: A Systematic Review », American Journal of Respiratory and Critical Care Medicine, vol. 179, no 3, , p. 220–227 (ISSN 1073-449X et 1535-4970, DOI 10.1164/rccm.200805-722OC, lire en ligne, consulté le ).
- (en) Margaret S. Herridge, Angela M. Cheung, Catherine M. Tansey et Andrea Matte-Martyn, « One-Year Outcomes in Survivors of the Acute Respiratory Distress Syndrome », New England Journal of Medicine, vol. 348, no 8, , p. 683–693 (ISSN 0028-4793 et 1533-4406, DOI 10.1056/NEJMoa022450, lire en ligne, consulté le ).
- (en) Thomas A. Neff, Reto Stocker, Hans-Rudolf Frey et Sonja Stein, « Long-term Assessment of Lung Function in Survivors of Severe ARDSa », Chest, vol. 123, no 3, , p. 845–853 (DOI 10.1378/chest.123.3.845, lire en ligne, consulté le ).
- (en) Margaret S. Herridge, Catherine M. Tansey, Andrea Matté et George Tomlinson, « Functional Disability 5 Years after Acute Respiratory Distress Syndrome », The New England Journal of Medicine, vol. 364, no 14, , p. 1293–1304 (ISSN 0028-4793 et 1533-4406, DOI 10.1056/NEJMoa1011802, lire en ligne, consulté le ).
Voir aussi[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- Physiopathologie
- (en) Charis Roussos et Antonia Koutsoukou, « Respiratory failure », European Respiratory Journal, vol. 22, no Supplement 47, , p. 3s–14s (ISSN 0903-1936 et 1399-3003, DOI 10.1183/09031936.03.00038503, lire en ligne, consulté le ).
- (en) Nicolaos K. Markou, Pavlos M. Myrianthefs et George J. Baltopoulos, « Respiratory Failure: An Overview », Critical Care Nursing Quarterly, vol. 27, no 4, , p. 353–379 (ISSN 0887-9303, DOI 10.1097/00002727-200410000-00006, lire en ligne, consulté le ).
- La détresse respiratoire chez l'enfant
- (en) James Schneider et Todd Sweberg, « Acute Respiratory Failure », Critical Care Clinics, vol. 29, no 2, , p. 167–183 (DOI 10.1016/j.ccc.2012.12.004, lire en ligne, consulté le ).
- (en) Matthew L. Friedman et Mara E. Nitu, « Acute Respiratory Failure in Children », Pediatric Annals, vol. 47, no 7, , e268–e273 (ISSN 1938-2359, DOI 10.3928/19382359-20180625-01, lire en ligne, consulté le ).
- Recommandations des sociétés savantes
- (en) Carmen Sílvia Valente Barbas, Alexandre Marini Ísola, Augusto Manoel de Carvalho Farias et Alexandre Biasi Cavalcanti, « Brazilian recommendations of mechanical ventilation 2013. Part 2 », Revista Brasileira de Terapia Intensiva, vol. 26, no 3, (ISSN 0103-507X, PMID 25295817, PMCID PMC4188459, DOI 10.5935/0103-507X.20140034, lire en ligne, consulté le ).
- (en) Bram Rochwerg, Laurent Brochard, Mark W. Elliott et Dean Hess, « Official ERS/ATS clinical practice guidelines: noninvasive ventilation for acute respiratory failure », European Respiratory Journal, vol. 50, no 2, , p. 1602426 (ISSN 0903-1936 et 1399-3003, DOI 10.1183/13993003.02426-2016, lire en ligne, consulté le ).
- (en) A Craig Davidson, Stephen Banham, Mark Elliott et Daniel Kennedy, « BTS/ICS guideline for the ventilatory management of acute hypercapnic respiratory failure in adults », Thorax, vol. 71, no Suppl 2, , ii1–ii35 (ISSN 0040-6376 et 1468-3296, DOI 10.1136/thoraxjnl-2015-208209, lire en ligne, consulté le ).
Articles connexes[modifier | modifier le code]
- Causes fréquentes de détresse respiratoire
- Pneumopathie
- Insuffisance cardiaque et œdème aigu du poumon
- Exacerbation de BPCO
- Syndrome de détresse respiratoire aiguë
- Modalités thérapeutiques
- Oxygénothérapie nasale à haut débit
- Ventilation non invasive
- Ventilation invasive : intubation et trachéotomie
- Oxygénation par membrane extracorporelle
- Respirateur artificiel
Liens externes[modifier | modifier le code]
- Détresse respiratoire: information à l’attention des patients, Claudia Steurer-Stey, Revue Médicale Suisse (2015; volume 11, pages 1965-1966).
- Conduite à tenir devant une insuffisance respiratoire aiguë, collège nationale des enseignants de réanimation médicale.
- Revue générale de la ventilation artificielle, Bhakti K. Patel, Manuel Merck, avril 2018.
- Insuffisance ventilatoire, Bhakti K. Patel, Manuel Merck, avril 2018.