Neurostimulateur
Un neurostimulateur est un dispositif médical utilisé pour traiter la douleur chronique d'origine neurologique. Une neurostimulation, pulsion électrique générée par la machine, provoque une paresthésie (« fourmillement ») qui altère la perception de la douleur chez le patient. Un chirurgien l'implante au cours d'une intervention chirurgicale percutanée, ou par une laminectomie dans l'espace médullaire de la colonne vertébrale en cas de stimulation dite médullaire, ou près du nerf à stimuler. Un générateur de pulsions électriques est ensuite implanté dans l'abdomen ou dans le haut d'une fesse, et un fil connecte le boîtier avec ledit générateur.
Histoire[modifier | modifier le code]
Depuis la première implantation d'un neurostimulateur[1] plusieurs études ont démontré l'efficacité du neurostimulateur en allégeant la souffrance de patients, qu'ils soient atteints d'algoneurodystrophie, du syndrome post-laminectomie (en)[2], ou de neuropathie périphérique.
Neurostimulation[modifier | modifier le code]
La neurostimulation est une technique qui consiste à produire des excitations (potentiels d’action) sur les cellules nerveuses au moyen d’impulsions électriques. Cette technique est utilisée pour traiter des douleurs lorsque les excitations portent sur des fibres afférentes ou pour obtenir des réponses musculaires lorsque les excitations sont appliquées sur des motoneurones.
On parle également de neuromodulation lorsque la neurostimulation est appliquée au niveau médullaire[3]. La neurostimulation est appliquée au moyen de neurostimulateurs implantables (neurostimulation percutanée p-NS) de type pacemakers ou au moyen de dispositifs externes (neurostimulation transcutanée t-NS), avec des appareils de type TENS qui stimulent via des électrodes (auto-collantes) par voie transcutanée, aussi bien au niveau du corps qu'au niveau crânien (appareils de type Cefaly).
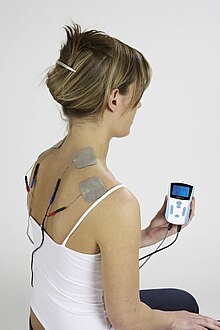
La neurostimulation transcutanée (TENS) fonctionne avec un courant électrique de faible tension transmis aux nerfs par des électrodes placées sur la peau. Son intensité et la fréquence des pulsations peuvent varier. Plusieurs paramètres de stimulation existent, variables en fonction de la fréquence des impulsions (de 1 Hz à 100 Hz), de l’intensité du courant électrique (0–50 mA) ou de la largeur de l’impulsion (50 à 500 μs).
Les modes de stimulation les plus courants sont :
- le mode TENS conventionnelle (C-TENS), également appelé « à effet gate control », associe une stimulation continue avec une fréquence de 80 à 100 Hz, des largeurs d’impulsion de 50 à 200 μs et des basses intensités. Ce mode permet de réaliser des paresthésies non douloureuses dans le territoire concerné. L’effet analgésique ne persiste pas après la stimulation ;
- le mode de stimulation discontinue « burst », également dit « acupuncture like » (AL-TENS) ou « endorphinique », associe des très basses fréquences (1 à 4 Hz), des largeurs d’impulsion comprises entre 100 et 400 μS et des hautes intensités. Ce mode provoque de faibles secousses musculaires. Il procure une analgésie rapide qui augmente durant la stimulation et persiste après l’arrêt de celle-ci.
Chirurgie[modifier | modifier le code]
Les complications le plus souvent liées à ce genre d'intervention peuvent inclure la migration du fil connecteur dans l'organisme, l'infection, l'hématome extra-dural, la paralysie, le perçage de la dura mater, et dans de rares cas, la mort. La possibilité de migration du fil diminue avec une laminectomie[4].
Une phase de test est généralement conduite avant d'implanter le dispositif permanent. Un fil temporaire extra-dural est utilisé, connecté à un générateur externe. Ce test dure de 1 à 3 semaines en général. Si le patient voit une réduction de la douleur d'au moins 50 %, il est candidat pour le dispositif permanent.
Précautions[modifier | modifier le code]
Les patients avec des neurostimulateurs ne peuvent pas être examinés avec l'imagerie par résonance magnétique (IRM) à cause de l'échauffement excessif des électrodes implantées, qui peuvent ainsi endommager la colonne vertébrale. En cas de nécessité absolue, l'examen est toujours possible après avoir coupé les électrodes avec la télécommande. D'autres moyens d'examen, non intrusifs, peuvent être utilisés à sa place, comme l'ultrason, la tomodensitométrie (CT-scan) ou les rayons X.
Ils doivent également éviter de s'exposer aux interférences électromagnétiques fortes, comme les transformateurs électriques, ainsi que le travail dangereux électrique, comme le soudage à l'arc.
Dispositifs utilisés[modifier | modifier le code]
- Le Conventional Implantable Pulse Generator (cIPG) consiste en une pile et des contrôles électriques. Quand la pile est usée, elle est remplacée lors d'une autre intervention chirurgicale.
- Le Rechargeable Implantable Pulse Generator (rIPG) consiste en une pile rechargeable et des contrôles électriques. La pile est rechargée au moyen d'un dispositif externe porté par le patient quelques heures au moins toutes les deux à trois semaines.
- Le dispositif à onde radio consiste en un récepteur implanté et un transmetteur porté comme un téléphone portable, qui envoie des ondes radio au récepteur qui, à son tour, stimule les neurones. Ce dispositif est généralement utilisé chez les patients nécessitant moins de stimulation.
On fournit au patient une télécommande pour allumer et éteindre l'appareil quand il le souhaite. Selon le type de dispositif et l'avis du médecin, la télécommande peut aussi changer le niveau de stimulation désiré. Le médecin dispose d'une machine qui peut modifier la configuration de la télécommande.
Tension[modifier | modifier le code]
Les neurostimulateurs implantables existent en versions à courant constant, à tension variable (Advanced Bionics ou St. Jude Medical), et en version à courant variable, tension constante (Medtronic). Les producteurs des appareils ne s'accordent pas sur l'efficacité relative de leurs configurations respectives.
Les neurostimulateurs transcutanés (de type TENS) sont aussi à courant constant, et à intensité variable, intégrant plusieurs programmes, fonctionnant sur piles (Cefar (es)) ou sur accumulateurs rechargeables (Schwa-Medico).
Autres usages[modifier | modifier le code]
Les neurostimulateurs internes ou externes sont utilisés pour traiter des patients atteints de migraines fortes et chroniques. En dispositif interne, les électrodes sont implantées sous la peau dans la région suboccipitale bilatérale[5]. En neurostimulation externe de type TENS, une électrode est positionnée sur le front pour agir sur la branche supérieure du nerf trijumeau[6].
Autre[modifier | modifier le code]
Parmi les patients célèbres implantés avec des neurostimulateurs on trouve Jerry Lewis (qui est porte-parole de Medtronic)[7], et Michael Roman, amputé d'une jambe à la suite d'une infection et souffrant de douleurs chroniques, et qui a relance sa carrière de pilote de racecar après l'implantation.
Notes et références[modifier | modifier le code]
- (en) Shealy CN, Mortimer JT, Reswick, JB « Electrical Inhibition of pain by stimulation of the dorsal columns: Preliminary Clinical Report » Anesth Analg. 1967;46:489-91.
- (en) North RB, Ewend MG, Lawton MT, Kidd DH, Piantadosi S. « Failed back surgery syndrome: 5-year follow-up after spinal cord stimulator implantation » Neurosurgery 1991;28(5):692-9.
- « Douleur : la neurostimulation sur mesure », sur Sciences et Avenir, (consulté le )
- (en) Villavicencio AT, Leveque JC, Rubin L, BulsaraK, Gorecki JP. « Laminectomy versus percutaneous electrode placement for spinal cord stimulation » Neurosurgery 2000;46(2):399-405; discussion 405-6.
- (en) Matharu MS, Bartsch T, Ward N, Frackowiak RS, Weiner R, Goadsby PJ. « Central neuromodulation in chronic migraine patients with suboccipital stimulators: a PET study » Brain 2004;127(Pt 1):220-30.
- (en) Schoenen J, Vandersmissen B, Jeangette S, Herroelen L, Vandenheede M, Gérard P, and Magis D, « Migraine prevention with a supraorbital transcutaneous stimulator: A randomized controlled trial » Neurology 2013;80:697-704.
- (en) Jerry Lewis: My Journey Through Pain
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Bibliographie[modifier | modifier le code]
- (en) Mailis-Gagnon A, Furlan AD, Sandoval JA, Taylor R (2004) « Spinal cord stimulation for chronic pain » Cochrane Database Syst Rev. (3): CD003783. .
- (en) North RB, Kidd DH, Farrokhi F, Piantadosi SA (2005) « Spinal cord stimulation versus repeated lumbosacral spine surgery for chronic pain: a randomized, controlled trial » Neurosurgery 56(1):98-106; discussion 106-7. .
- Siani F. - Boucand M.H - Les mécanismes de la douleur. La neurostimulation transcutanée - le TENS, 2006. Association Française des Syndromes d’Ehlers-Danlos A.F.S.E.D
