Alcool allylique
| Alcool allylique | |
| |
| Identification | |
|---|---|
| Nom UICPA | prop-2-én-1-ol |
| Synonymes |
1-propén-2-ol; alcool allyle; 2-propén-1-ol; 2-propénol |
| No CAS | |
| No ECHA | 100.003.156 |
| No CE | 203-470-7 |
| No RTECS | BA5075000 |
| PubChem | 7858 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore mobile avec une odeur forte ressemblant à celle de la moutarde[1] |
| Propriétés chimiques | |
| Formule | C3H6O [Isomères] |
| Masse molaire[4] | 58,079 1 ± 0,003 1 g/mol C 62,04 %, H 10,41 %, O 27,55 %, |
| pKa | 15.5 (25 °C) [2] |
| Moment dipolaire | 1,77 D [3] |
| Diamètre moléculaire | 0,490 nm [3] |
| Propriétés physiques | |
| T° fusion | −129 °C [2] |
| T° ébullition | 97 °C [2] |
| Solubilité | 1 000 g·l-1 (eau, 20 °C) [2] |
| Paramètre de solubilité δ | 24,1 MPa1/2 (25 °C)[5] |
| Masse volumique | 0,854 0 g·cm-3 à 20 °C[1] |
| T° d'auto-inflammation | 378 °C[1] |
| Point d’éclair | 21 °C[1] |
| Pression de vapeur saturante | 26,1 mmHg (25 °C) [2] |
| Viscosité dynamique | 1,218 mPa s à 25 °C 0,759 mPa s à 50 °C 0,505 mPa s à 75 °C[1] |
| Point critique | 269,85 °C [6] |
| Thermochimie | |
| Cp | |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 9,67 ± 0,05 eV (gaz)[8] |
| Propriétés optiques | |
| Indice de réfraction | 1,4113 [3] 1,412 [9] |
| Précautions | |
| SGH[10],[9] | |
| H225, H301, H311, H315, H319, H331, H335 et H400 |
|
| SIMDUT[11] | |
  B2, D1A, D2B, |
|
| NFPA 704 | |
| Transport | |
| Écotoxicologie | |
| DL50 | 96 mg·kg-1 (souris, oral) 78 mg·kg-1 (souris, i.v.) 60 mg·kg-1 (souris, i.p.) [2] |
| Seuil de l’odorat | bas : 1,4 ppm haut : 2,1 ppm[12] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
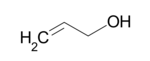
Un alcool allylique est un composé organique portant un groupement hydroxyle en position allylique. L'alcool allylique (2-propèn-1-ol) C3H6O ou H2C=CH-CH2-OH est un liquide incolore à odeur piquante (point d'ébullition 97 °C). On le trouve dans les fruits en décomposition.
On le prépare industriellement par hydrolyse à la soude du chlorure d'allyle, obtenu par chloration radicalaire du propène. Il est utilisé comme matière première de résines, de plastifiants. Il fait partie de la liste EPA des substances extrêmement dangereuses
Notes et références[modifier | modifier le code]
- Fiche PubChem 7858
- (en) « Alcool allylique », sur ChemIDplus, consulté le 8 février 2009
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 0387690026, lire en ligne), p. 294
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, Huston, Texas, Gulf Pub. Co., (ISBN 0-88415-857-8)
- (en) David R. Lide, Handbook of chemistry and physics, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- Fiche Sigma-Aldrich du composé Allyl alcohol ≥99%, consultée le 26/06/2015.
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Alcool allylique » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Allyl alcohol », sur hazmap.nlm.nih.gov (consulté le )









