Éthionamide
| Éthionamide | ||

| ||
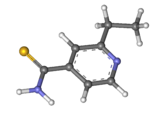 | ||
| Représentations plane et 3D de l'éthionamide | ||
| Identification | ||
|---|---|---|
| DCI | 2-ethylpyridine-4-carbothioamide | |
| Nom UICPA | 2-ethylpyridine-4-carbothioamide | |
| No CAS | ||
| No ECHA | 100.007.846 | |
| No CE | 208-628-9 | |
| Code ATC | J04AD03 | |
| DrugBank | DB00609 | |
| PubChem | CID 2761171 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | C8H10N2S |
|
| Masse molaire[1] | 166,243 ± 0,013 g/mol C 57,8 %, H 6,06 %, N 16,85 %, S 19,29 %, 166.244 g/mol |
|
| Données pharmacocinétiques | ||
| Demi-vie d’élim. | 2 à 3 heures | |
| Considérations thérapeutiques | ||
| Classe thérapeutique | agent antituberculeux | |
| Voie d’administration | Orale | |
| Grossesse | catégorie C | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
L'éthionamide (ou « ETH ») est un antibiotique découvert en 1936[2] utilisé contre Mycobacterium tuberculosis.
La voie synthèse [3][modifier | modifier le code]

Mécanisme d'action[modifier | modifier le code]
Comme l'isoniazide (INH), l'éthionamide cible l'InhA, une enzyme du système FAS II de Mycobacterium tuberculosis nécessaire à l'élongation des acides gras qui participent à la synthèse des acides mycoliques qui sont des constituants nécessaires de la paroi de cette mycobactérie. Toutefois, ces deux molécules (INH et ETH) ne sont que des pro-drogues ; elles nécessitent une étape d'activation oxydante induite par une enzyme. Deux enzymes peuvent jouer ce rôle :
- La catalase-peroxydase KatG du MTB dans le cas de l'isoniazide (INH)[4]. L'espèce active (radical isonicotinoyle) peut alors agir via une chaine de réaction qui conduit à la destruction de la paroi de M. tuberculosis ;
- La flavine monooxygénase EthA, qui aboutit au même résultat, mais par un processus différent.
C’est en 2000 que DeBarber et al.[5] et Baulard et al.[6] ont mis en évidence l’implication de la monooxygénase EthA, codée par le gène ethA, dans l’activation de l’éthionamide. Ainsi, ces équipes ont montré qu’une surproduction d’EthA chez M. smegmatis conduit à une sensibilité accrue de ces souches à l’ETH. Inversement, des souches cliniques isolées de patients d’Afrique du Sud possédant des mutations au niveau du gène ethA perdent leur sensibilité à l’ETH.
Il a été proposé de créer des molécules hybrides INH-ETH[7].
Enjeux[modifier | modifier le code]
La tuberculose due à Mycobacterium tuberculosis (MTB) compte encore parmi les maladies infectieuses difficiles à combattre dans le monde et elle est une des causes principales de décès par maladie infectieuse dans certains pays.
L'isoniazide (INH) et la rifampicine qui sont les deux antibiotiques de première intention ne sont plus toujours efficaces et des phénomènes croissants d'antibiorésistance et de problèmes nosocomiaux ou chez les patients immunodéprimés par le VIH/SIDA[8]. Pour les limiter et les contourner, d'autres molécules sont utilisées en seconde ligne, dont l’éthionamide (ETH).
L'éthionamide fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[9].
Références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- "Ethionamide" . TB Online. Global Tuberculosis Community Advisory Board. Consulté 2012-08-18.
- The Organic Chemistry of Drug Synthesis, Volume 1. Daniel Lednicer, Lester A. Mitscher. (ISBN 978-0-471-52141-9), 496 pages, February 1977
- Joseph A. DeVito and Sheldon Morris, Exploring the Structure and Function of the Mycobacterial KatG Protein Using trans-Dominant Mutants, Antimicrob Agents Chemother. Jan 2003; 47(1): 188–195., https://www.ncbi.nlm.nih.gov/pmc/articles/PMC148984/, doi: 10.1128/AAC.47.1.188-195.2003
- DeBarber, A. E.; Mdluli, K.; Bosman, M.; Bekker, L.-G.; Barry, C. E., Ethionamide activation and sensitivity in multidrug-resistant Mycobacterium tuberculosis. Proceedings of the National Academy of Sciences 2000, 97 (17), 9677-9682.
- Baulard, A. R.; Betts, J. C.; Engohang-Ndong, J.; Quan, S.; McAdam, R. A.; Brennan, P. J.; Locht, C.; Besra, G. S., Activation of the Pro-drug Ethionamide Is Regulated in Mycobacteria. Journal of Biological Chemistry 2000, 275 (36), p. 28326-28331.
- Deraeve C () Conception et synthèse d’antituberculeux hybrides isoniazide-éthionamide et étude de leur activation par oxydation biomimétique (Proposition de sujet de thèse), PDF, 2 pages
- Gandhi, N. R., Shah, N. S., Andrews, J. R., Vella, V., Moll, A. P., Scott, M.... & Friedland, G. H. (2010). HIV coinfection in multidrug-and extensively drug-resistant tuberculosis results in high early mortality. American journal of respiratory and critical care medicine, 181(1), 80-86 (résumé)
- WHO Model List of Essential Medicines, 18th list, avril 2013
Voir aussi[modifier | modifier le code]
Articles connexes[modifier | modifier le code]
Articles externes[modifier | modifier le code]
- « Éthionamide : substance active à effet thérapeutique », sur VIDAL (consulté le )
Bibliographie[modifier | modifier le code]
- Flipo, M. (2013) Développement de boosters d’éthionamide comme nouvelle approche dans le traitement de la tuberculose. De l’identification de la cible à la découverte d’un candidat médicament ; Séminaires & Conférences Chimie, École Doctorale 459, , Université Montpellier II (résumé de cours).
- Bastian I & Colebunders R (1999) Treatment and prevention of multidrug-resistant tuberculosis. Drugs, 58(4), 633-661 (résumé).
- Mitnick C & Horsburgh Jr CR (2010). Encouraging news for multidrug-resistant tuberculosis treatment. American journal of respiratory and critical care medicine, 182(11), 1337-1338 ([ résumé]).

